| 酸碱中和滴定 题目答案及解析
稿件来源:高途
| 酸碱中和滴定题目答案及解析如下,仅供参考!
选修四
第三章 水溶液中的离子平衡
第二节 水的电离和溶液的酸碱性
酸碱中和滴定
用$\rm 0.1\;\rm mol ⋅ L^{-1}NaOH$溶液分别滴定$\rm 20.00\;\rm mL$浓度均为$\rm 0.1\;\rm mol ⋅ L^{-1}$的醋酸$\rm ($曲线$\rm 1)$和盐酸$\rm ($曲线$\rm II)$溶液,得到溶液$\rm pH$随加入$\rm NaOH$溶液体积而变化的两条滴定曲线。
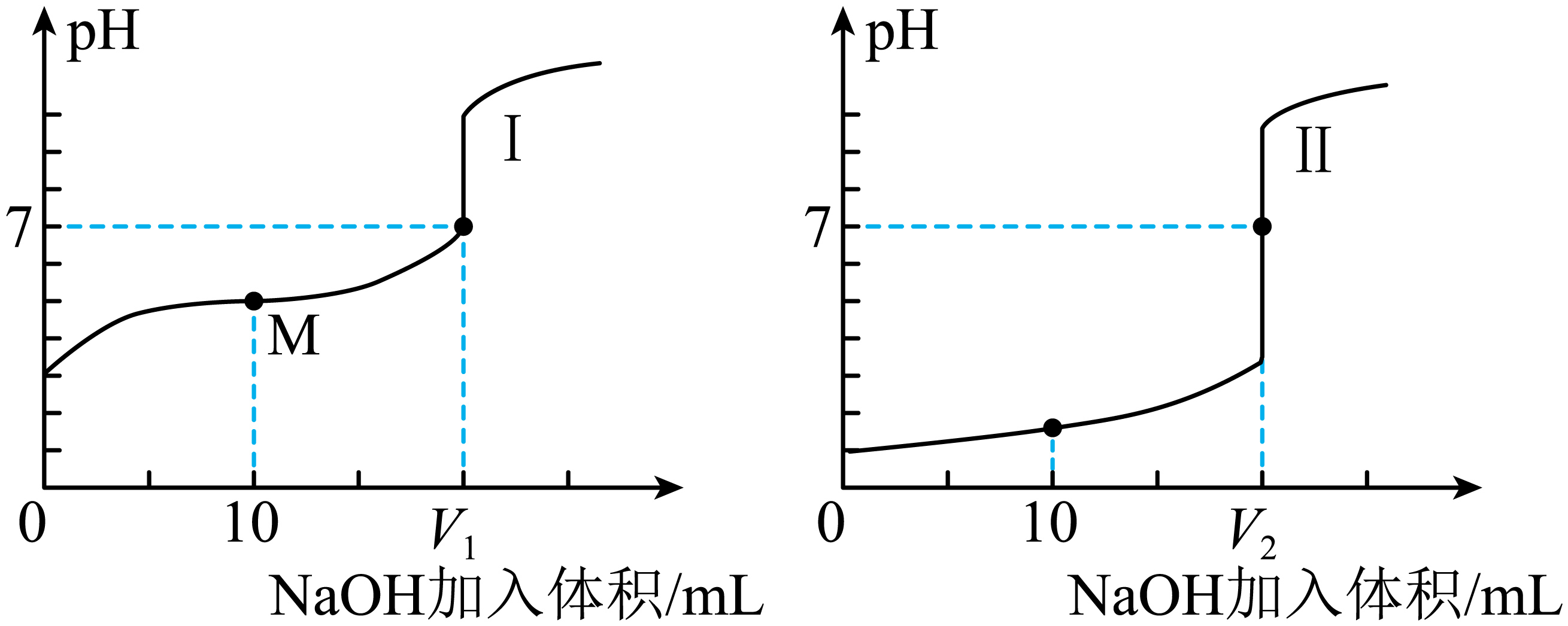
在上述滴定实验中,不需要使用的仪器是$\rm (\quad\ \ \ \ )$。
滴定管
","锥形瓶
","胶头滴管
","电子天平
"]滴定实验需要使用多种仪器,包括滴定管、锥形瓶、移液管等,故选:$\rm CD$;
酸碱滴定法选择指示剂时可以不考虑因素是$\rm (\quad\ \ \ \ )$。
指示剂突跃的范围
","指示剂的变色范围
","指示剂的颜色变化
","指示剂相对分子质量的大小
"]$\rm A$.指示剂的选择还应考虑滴定过程中$\rm pH$值的变化范围,即滴定突跃的范围。这个范围决定了指示剂变色的有效性,因此选择指示剂时需要考虑到这一点,需要考虑,$\rm A$不选;
$\rm B$.理想的指示剂应具有较窄的变色范围,这样$\rm pH$的微小变化就能引起颜色的明显改变,从而便于观察和判断滴定的终点,需要考虑,$\rm B$不选;
$\rm C$.选择指示剂时,应考虑溶液颜色变化的可观察性。通常,由浅变深的颜色变化更容易观察,因此在选择指示剂时应考虑其在滴定终点时能使溶液颜色由浅变深,需要考虑,$\rm C$不选;
$\rm D$.指示剂的相对分子质量大小不是选择指示剂时的决定性因素,$\rm D$选;
故选:$\rm D$。
滴定过程中眼睛应注视 。一手控制 ,一手 。某次实验滴定终点时滴定管中液面位置如图所示,则此时的读数为 $\rm \;\rm mL$。
![]()
锥形瓶内溶液颜色的变化 控制滴定管活塞 握持锥形瓶 $\\rm 18.60$
"]]滴定过程中眼睛应注视锥形瓶内溶液颜色的变化。一手控制滴定管活塞,一手握持锥形瓶。某次实验滴定终点时滴定管中液面位置如图所示,则此时的读数为$\rm 18.60mL$。
将上述同浓度、同体积的盐酸与醋酸分别与足量的镁条反应,测得密闭容器中压强随时间的变化曲线如图所示。下列说法正确的是$\rm (\quad\ \ \ \ )$。
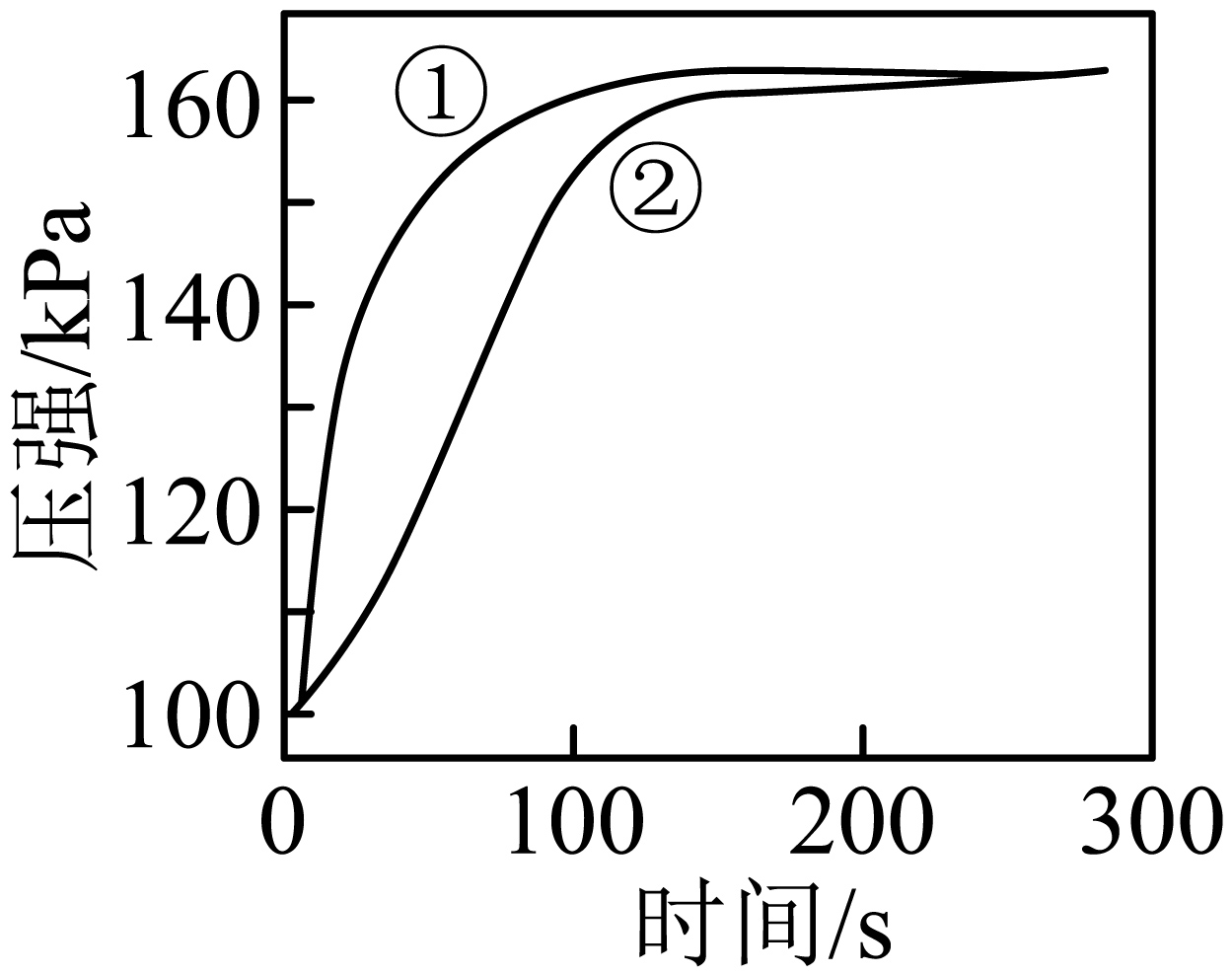
反应开始前$\\rm c(H^{+})$:盐酸$\\rm =$醋酸
","反应过程中醋酸中$\\rm c(H^{+})$下降更快
","曲线②表示盐酸与镁条反应
","反应结束时两容器内$\\rm n(H_{2})$相等
"]$\rm HCl$为强酸,完全电离,醋酸为弱酸,部分电离,同浓度、同体积的盐酸与醋酸,反应开始前$\rm c(H^{+})$:盐酸$\rm \gt $醋酸,故$\rm A$错误;
$\rm B$.反应过程中盐酸中$\rm c(H^{+})$比醋酸中$\rm c(H^{+})$大,盐酸反应速率快,$\rm c(H^{+})$下降更快,故$\rm B$错误;
$\rm C$.反应过程中盐酸中$\rm c(H^{+})$比醋酸中$\rm c(H^{+})$大,盐酸反应速率快,根据图像,曲线②表示醋酸与镁条反应,故$\rm C$错误;
$\rm D$.根据图像可知,反应结束时两容器内$\rm n(H_{2})$与酸的强弱无关,产生的$\rm n(H_{2})$相等,,故$\rm D$正确;
故选:$\rm D$。
| 酸碱中和滴定题目答案及解析(完整版)
