| 盐溶液微粒间的三大守恒原理的理解及应用 题目答案及解析
稿件来源:高途
| 盐溶液微粒间的三大守恒原理的理解及应用题目答案及解析如下,仅供参考!
选修四
第三章 水溶液中的离子平衡
第三节 盐类的水解
盐溶液微粒间的三大守恒原理的理解及应用
$\rm 298K$时,向$\rm 20.0\;\rm mL\;\rm 0.10\;\rm mol ⋅ L^{-1}H_{2}A$溶液中滴加$\rm 0.10\;\rm mol ⋅ L^{-1}NaOH$溶液,滴定曲线如图所示。下列说法不正确的是$\rm (\qquad)$
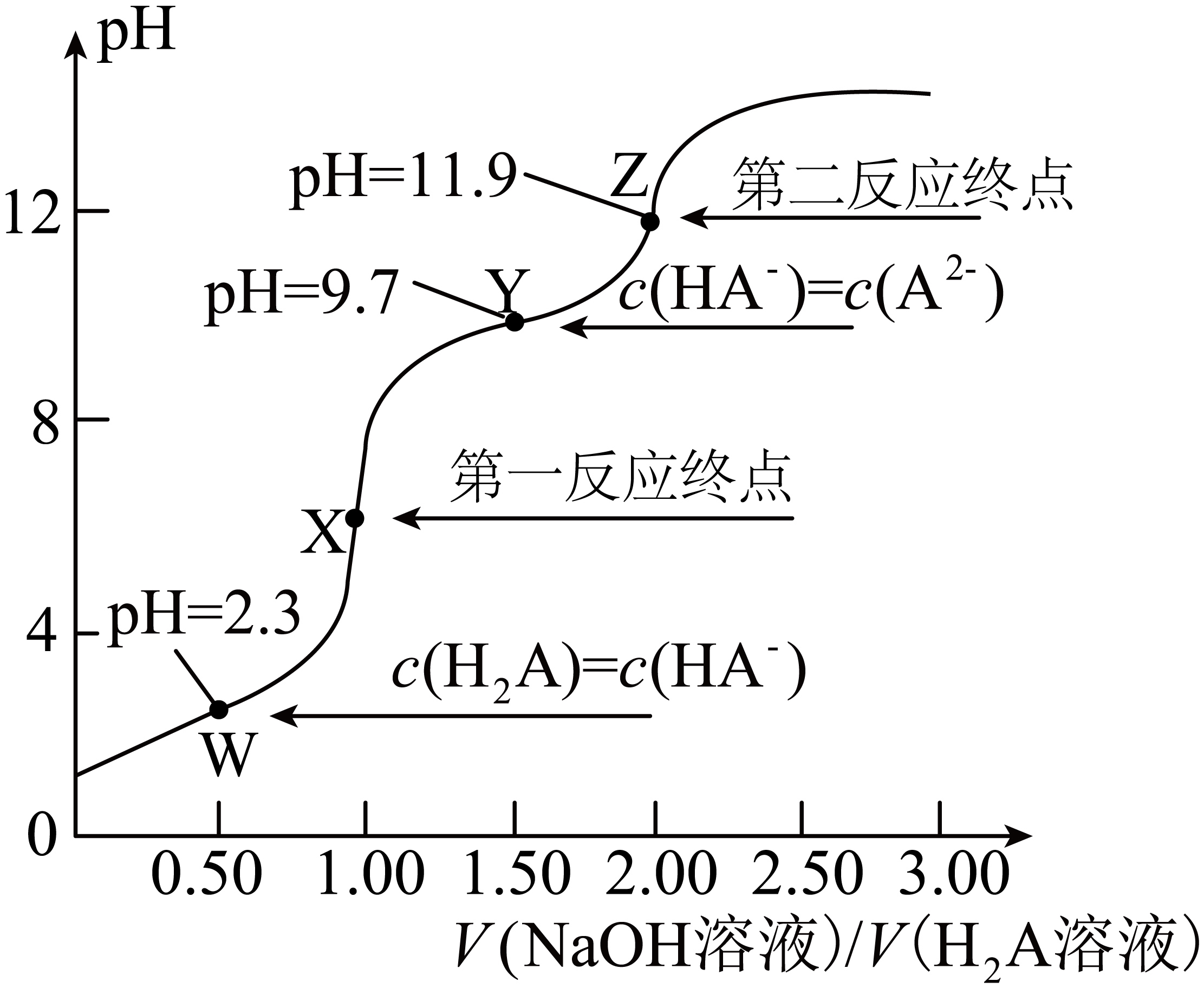
该滴定过程应该选择酚酞溶液作指示剂
","$\\rm W$点到$\\rm X$点发生的主要反应的离子方程式为$\\rm H_{2}A + OH^{−} = HA^{−} + H_{2}O$
","$\\rm Y$点对应的溶液中$\\rm c(Na^{+}) + c(H^{+}) = c(OH^{−}) + 3c(A^{2−})$
","反应$\\rm H_{2}A + A^{2−} ⇌ 2HA^{−}$的平衡常数$\\rm K = 1.0 \\times 10^{-7.4}$
"]向$\rm 20.0\;\rm mL\;\rm 0.10\;\rm mol ⋅ L^{-1}H_{2}A$溶液中滴加$\rm 0.10\;\rm mol ⋅ L^{-1}NaOH$溶液,滴定过程发生反应:$\rm H_{2}A+OH^{-}=HA^{-}+H_{2}O$、$\rm HA^{-}+OH^{-}=A^{2-}+H_{2}O$,结合图像:$\rm X$点溶质为$\rm NaHA$,$\rm Z$点溶质为$\rm Na_{2}A$。
$\rm A$.该滴定过程第一反应终点$\rm X$在$\rm pH=6$左右,应选用甲基橙作指示剂,第二反应终点$\rm Z$在$\rm pH=11.9$,应选酚酞溶液作指示剂,$\rm A$错误;
$\rm B$.$\rm X$点溶质为$\rm NaHA$,$\rm X$点之前主要反应的离子方程式为$\rm H_{2}A + OH^{−} = HA^{−} + H_{2}O$,$\rm B$正确;
$\rm C$.据图示可知,$\rm Y$点处$\rm c(HA^{-})=c(A^{2-})$,根据电荷守恒有:$\rm c(Na^{+}) + c(H^{+}) = c(OH^{−}) + 2c(A^{2−}) + c(HA^{−})$,则$\rm Y$点对应的溶液中$\rm c(Na^{+}) + c(H^{+}) = c(OH^{−}) + 3c(A^{2−})$,$\rm C$正确;
$\rm D$.根据$\rm W$点数据可得,$\rm H_{2}A$的第一步电离平衡常数$\rm K_{1}=10^{-2.3}$,根据$\rm Y$点数据可得,$\rm H_{2}A$的第二步电离平衡常数$\rm K_{2}=10^{-9.7}$,反应$\rm H_{2}A + A^{2−} ⇌ 2HA^{−}$的平衡常数$\rm K = \dfrac{\text{c}^{\text{2}}\left( \text{HA}^{-} \right)}{\text{c}\left( \text{H}_{\text{2}}\text{A} \right)\text{c}\left( \text{A}^{\text{2-}} \right)} = \dfrac{\text{K}_{1}}{\text{K}_{2}}\rm =10^{7.4}$,$\rm D$错误;
故选:$\rm AD$。
| 盐溶液微粒间的三大守恒原理的理解及应用题目答案及解析(完整版)
