高中 | 电解池原理 题目答案及解析
稿件来源:高途
高中 | 电解池原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第三节 电解池
电解池原理
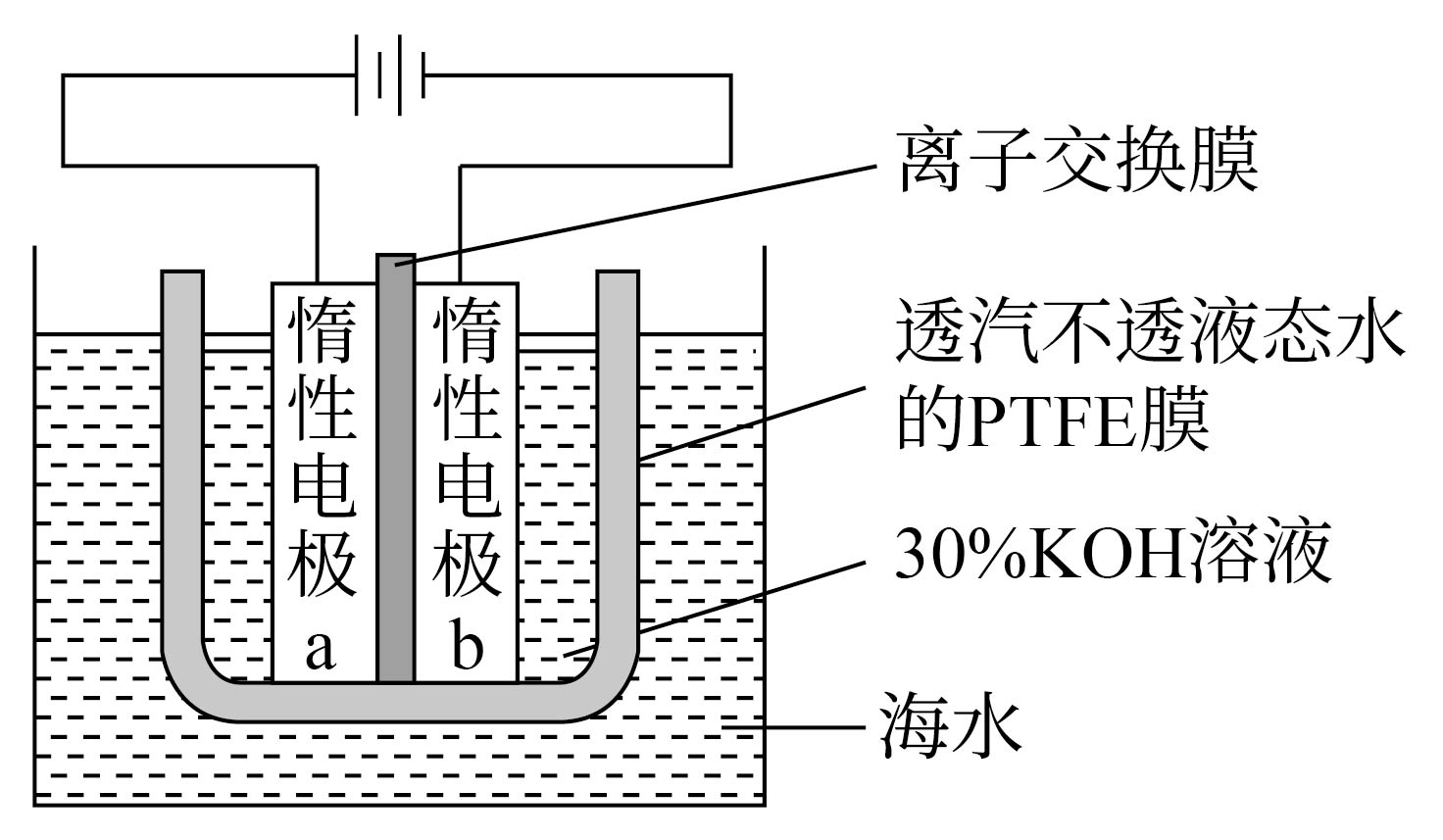
我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置工作时阳极无$\rm \text{C}{{\text{l}}_{2}}$生成且$\rm KOH$溶液的浓度不变,电解生成氢气的速率为$x\text{ mol}\cdot {{\text{h}}^{-1}}$。下列说法错误的是$(\quad\ \ \ \ )$
$\\rm b$电极反应式为:$2\\rm H_{2}O+2e^{-}=H_{2}↑+2OH^{-}$
","离子交换膜为阴离子交换膜
","电解时海水中动能高的水分子可穿过$\\rm PTFE$膜
","海水为电解池补水的速率为$ 2x\\text{ mol}\\cdot {{\\text{h}}^{-1}}$
"]$\rm A$.$\rm b$电极反应式为$\rm b$电极为阴极,发生还原反应,电极反应为$\rm 2{{H}_{2}}O+2{{e}^{-}}={{H}_{2}}\uparrow +2O{{H}^{-}}$,故$\rm A$正确;
$\rm B$.该装置工作时阳极无$\rm Cl_{2}$生成且$\rm KOH$浓度不变,阳极发生的电极反应为$\rm 4O{{H}^{-}}-4{{e}^{-}}={{O}_{2}}\uparrow +2{{H}_{2}}O$,为保持$\rm O{{H}^{-}}$离子浓度不变,则阴极产生的$\rm O{{H}^{-}}$离子要通过离子交换膜进入阳极室,即离子交换膜应为阴离子交换摸,故$\rm B$正确;
$\rm C$.电解时电解槽中不断有水被消耗,海水中的动能高的水可穿过$\rm PTFE$膜,为电解池补水,故$\rm C$正确;
$\rm D$.由电解总反应可知,每生成$\rm 1$ $\rm mol$ $\rm H_{2}$要消耗$\rm 1$ $\rm mol$ $\rm H_{2}O$,生成$\rm H_{2}$的速率为$x\text{ mol}\cdot {{\text{h}}^{-1}}$,则补水的速率也应是$x\text{ mol}\cdot {{\text{h}}^{-1}}$,故$\rm D$错误;
故选:$\rm D$
高中 | 电解池原理题目答案及解析(完整版)
