| 杂化轨道理论 题目答案及解析
稿件来源:高途
| 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
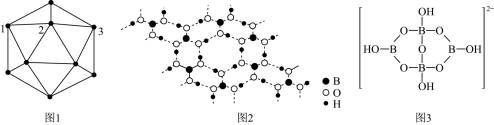
单质硼、硼酸$\rm ({{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}\rm )$、硼砂$\rm (\text{N}{{\text{a}}_{2}}{{\text{B}}_{4}}{{\text{O}}_{7}}\cdot 10{{\text{H}}_{2}}\text{O}\rm )$中阴离子$\rm \left( {{\text{H}}_{4}}{{\text{B}}_{4}}{{\text{O}}_{9}}{{}^{2-}} \right)$的结构或结构单元分别如图$\rm 1$、图$\rm 2$、图$\rm 3$所示。
回答下列问题:
图$\rm 1$为某晶体硼的部分结构单元,其熔点为$\rm 1873\ \text{K}$,属于 晶体,该结构单元由$\rm 20$个等边三角形构成,则构成此结构单元的$\rm B$原子数为 。
晶体硼熔点为$\rm 1873\ \text{K}$,熔点高,属于共价晶体;晶体硼结构单元由$\rm 20$个等边三角形构成,每个$\rm B$原子被$\rm 5$个等边三角形共有,总的$\rm B$原子数为:$\rm \dfrac{1}{5}\times 3\times 20=12$个;
图$\rm 2$为硼酸晶体的平面结构,硼酸晶体中存在的作用力有 $\rm ($填标号$\rm )$
$\rm a$.离子键 $\rm b$.共价键 $\rm c$.配位键 $\rm d$.氢键 $\rm e$.范德华力
在硼酸晶体中,构成微粒是硼酸分子,硼酸分子之间通过分子间作用力(或范德华力)结合,在硼酸分子内,$\rm B-O$、$\rm H-O$键均为共价键,在硼酸分子间易形成分子间氢键,故硼酸晶体中存在的作用力有:共价键、范德华力、氢键,故选:$\rm bde$;
$\rm {{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$与$\rm \text{NaOH}$溶液反应时,反应方程式为$\rm {{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}+\text{NaOH}=\text{NaB}{{\text{O}}_{2}}+2{{\text{H}}_{2}}\text{O}$,则$\rm {{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$是 弱酸$\rm ($填“一元”或“三元”$\rm )$;当$\rm {{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$过量时,反应得到硼砂晶体,其化学方程式为$\rm 4{{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}+2\text{NaOH}+3{{\text{H}}_{2}}\text{O}=\text{N}{{\text{a}}_{2}}{{\text{B}}_{4}}{{\text{O}}_{7}}\cdot 10{{\text{H}}_{2}}\text{O}$,硼砂阴离子$\rm {{\text{H}}_{4}}{{\text{B}}_{4}}\text{O}_{9}^{2-}$的结构如图$\rm 3$所示,其中$\rm \text{B}$原子的杂化方式为 。
氢氧化钠溶液过量时,酸电离产生的$\rm H^{+}$完全反应生成正盐,根据方程式可知,$\rm H_{3}BO_{3}$和$\rm NaOH$以$\rm 1:1$反应,故$\rm H_{3}BO_{3}$为一元弱酸;根据结构可知其中含有两种$\rm B$原子,形成$\rm 3$个$\rm B-O$键的$\rm B$原子采用$\rm sp^{2}$杂化,形成$\rm 4$个$\rm B-O$键的$\rm B$原子采用$\rm sp^{3}$杂化;
$\rm B$、$\rm Al$,$\rm Ga$为同主族元素,$\rm \text{AlC}{{\text{l}}_{3}}$,$\rm \text{GaC}{{\text{l}}_{3}}$在一定条件下均易形成双聚分子,而$\rm \text{BC}{{\text{l}}_{3}}$却很难形成双聚分子,其主要原因是$\rm \text{BC}{{\text{l}}_{3}}$分子内形成了大$\rm \pi $键,该大$\rm \pi $键可表示为 。$\rm ($分子中的大$\rm \pi $键可用符号$ \Pi _{m}^{n}$表示,其中$ m$代表参与形成大$\rm \pi $键的原子数,$n$代表参与形成大$\rm \pi $键的电子数$\rm )$
$\rm BCl_{3}$中$\rm B$原子的价层电子对数为$\rm 3$,$\rm B$原子采用$\rm sp^{2}$杂化,$\rm B$原子提供空的$\rm 2p$轨道,$\rm Cl$原子提供含$\rm 2$个电子的$\rm 3p$轨道,形成四中心六电子的大$\rm \pi$键,表示为$\rm \Pi _{4}^{6}$。
| 杂化轨道理论题目答案及解析(完整版)
