高中 | 电解池原理 题目答案及解析
稿件来源:高途
高中 | 电解池原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第三节 电解池
电解池原理
$\text{NO-}$空气质子交换膜燃料电池实现了制硝酸、发电、环保一体化。某兴趣小组用该电池模拟工业处理废气和废水的过程,装置如图所示,下列说法正确的是$(\qquad)$
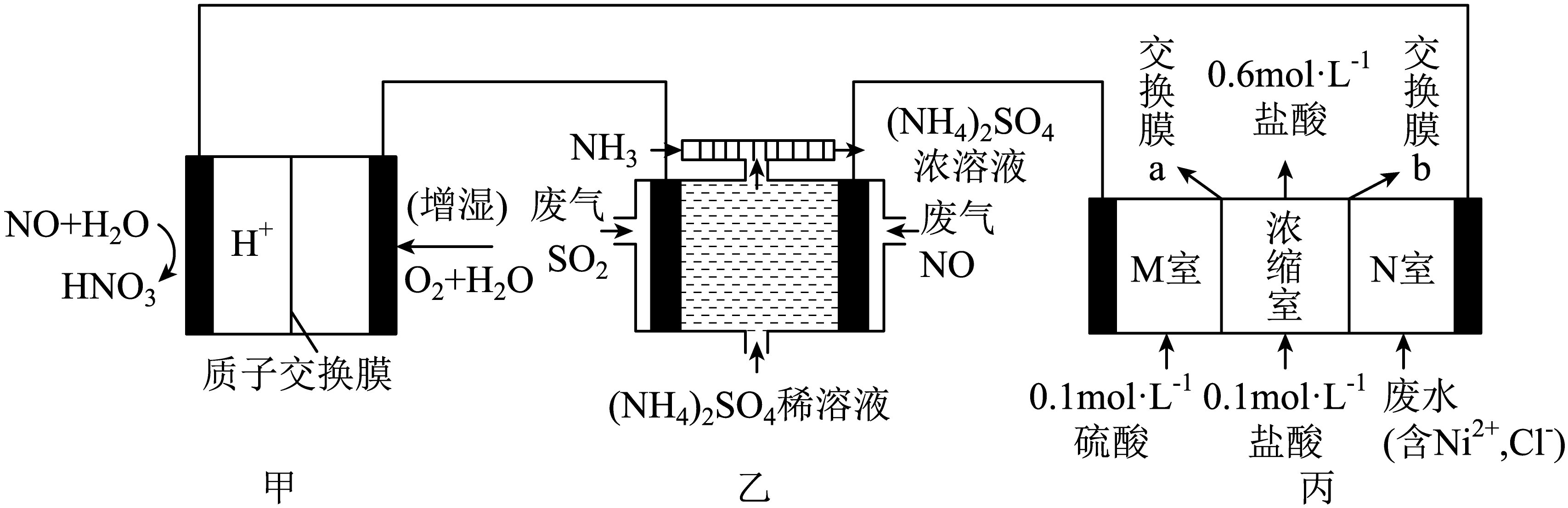
$\\rm a$膜为阴离子交换膜
","乙池中阴极的电极反应式为$\\rm {NO+5}{{ {e}}^{-}} {+5}{{ {H}}_{ {2}}} {O}= {NH}_{ {4}}^{+} {+6O}{{ {H}}^{-}}$
","当浓缩室得到$\\rm {4\\;\\rm L\\; 0} {.6\\;\\rm mol}\\cdot {{ {L}}^{{-1}}}$的盐酸时,$\\rm M$室溶液的质量变化为$\\rm {18\\;\\rm g}\\rm ($溶液体积变化忽略不计$\\rm )$
","标况下,若甲池有$\\rm {11} {.2\\;\\rm L }\\;{{ {O}}_{ {2}}}$参加反应,则乙池中处理废气$\\rm ( {S}{{ {O}}_{ {2}}}$和$\\rm {NO}\\rm )$的总体积为$\\rm {15} {.68\\;\\rm L}$
"]由图可知,甲为原电池,乙和丙为电解池;甲中通入一氧化氮的电极为负极,通入氧气的电极为正极;乙池中通入二氧化硫的电极连为电解池的阳极,水分子作用二氧化硫在阳极上失去电子发生氧化反应生成硫酸根离子和氢离子,通入一氧化氮的电极为阳极,酸性条件下一氧化氮在阴极上得到电子发生还原反应生成铵根离子和水;丙池中,左侧电极为电解池的阳极,水在阳极上失去电子发生氧化反应生成氧气和氢离子,氢离子从$\rm M$室通过阳离子交换膜$\rm a$膜进入浓缩室,右侧电极为阴极,镍离子在阴极得到电子发生还原反应生成镍, $\rm N$室中氯离子通过阴离子交换膜$\rm b$膜进入浓缩室,最终在浓缩室得到较浓的盐酸。
$\rm A$.由分析可知,$\rm a$膜为阳离子交换膜,故$\rm A$错误;
$\rm B$.由分析可知,乙池中通入一氧化氮的电极为阳极,酸性条件下一氧化氮在阴极上得到电子发生还原反应生成铵根离子和水,电极反应式为$\rm {NO+5}{{ {e}}^{-}} {+6}{{ {H}}^{+}}= {NH}_{ {4}}^{+}+{{ {H}}_{ {2}}} {O}$,故$\rm B$错误;
$\rm C$.当浓缩室得到$\rm 4\;\rm L\;\rm 0.6\;\rm mol/L$盐酸时,从$\rm M$室通过阳离子交换膜$\rm a$膜进入浓缩室的氢离子物质的量为$\rm (0.6\;\rm mol/L-0.1\;\rm mol/L)\times 4\;\rm L=2\;\rm mol/L$,则$\rm M$室消耗水的质量为$\rm 2\;\rm mol/L\times \dfrac{1}{2}\rm \times 18\;\rm g/mol=18\;\rm g$,故$\rm C$正确;
$\rm D$.由得失电子数目守恒可知,标况下,若甲池有$\rm 11.2\;\rm L$氧气参加反应时,乙池中处理废气的体积为$\rm \left(\dfrac{ {11} {.2\;\rm L}}{ {22} {.4\;\rm L/mol}} \times 2+\dfrac{ {11} {.2\;\rm L}}{ {22} {.4\;\rm L/mol}} { }\rm \times \dfrac{ {4}}{ {5}} { }\rm\right)\times 22.4\;\rm L/mol=31.36\;\rm L$,故$\rm D$错误。
故选:$\rm C$
高中 | 电解池原理题目答案及解析(完整版)
