高中 | 氯气 题目答案及解析
稿件来源:高途
高中 | 氯气题目答案及解析如下,仅供参考!
必修一
第四章 非金属及其化合物
第二节 富集在海水中的元素——氯
氯气
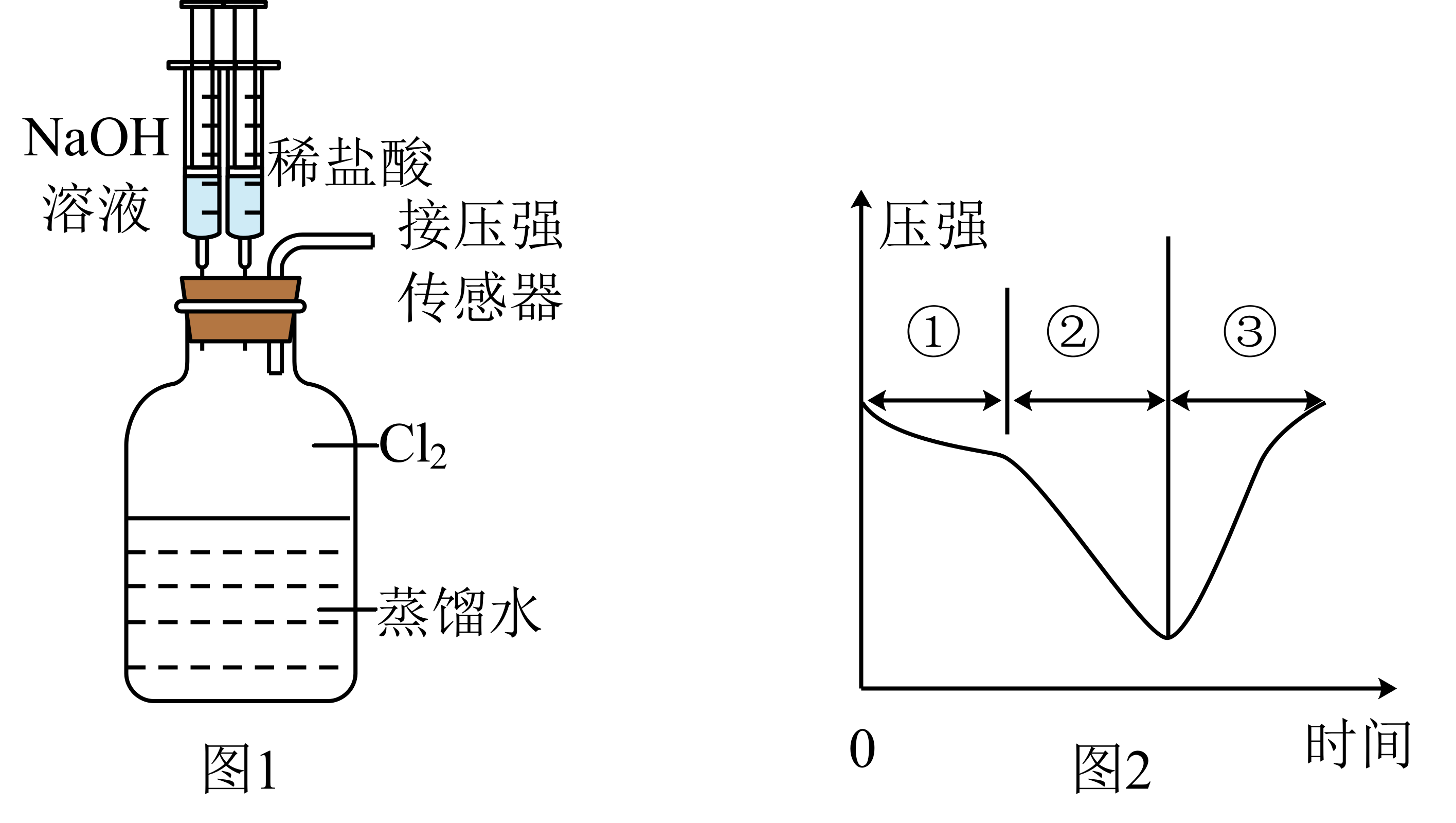
用图$\rm 1$所示装置向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加$\rm NaOH$溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图$\rm 2$所示。下列说法错误的是$(\qquad)$
若将$\\rm Cl_{2}$换成$\\rm CO_{2}$,则压强变化与图$\\rm 2$趋势相似
","阶段②的压强变小,可利用该过程发生的反应制备漂白液
","阶段①说明氯气溶于水,溶于水的氯气全部与水反应
","阶段③发生反应的离子方程式为$\\text{C}{{\\text{l}}^{-}}\\text{+Cl}{{\\text{O}}^{-}}\\text{+2}{{\\text{H}}^{+}}\\text{=C}{{\\text{l}}_{\\text{2}}}\\uparrow +{{\\text{H}}_{\\text{2}}}\\text{O}$
"]向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,此时有部分氯气溶于水,导致气体压强减小,用注射器滴加$\rm NaOH$溶液,$\rm NaOH$与$\rm Cl_{2}$反应,压强继续减小;再利用注射器滴加稀盐酸,此时$\rm Cl^{-}$、$\rm ClO^{-}$与$\rm H^{+}$发生反应生成$\rm Cl_{2}$,导致气体压强增大。
$\rm A$.若将$\rm Cl_{2}$换成$\rm CO_{2}$,起初$\rm CO_{2}$部分溶于水,然后与$\rm NaOH$反应,生成$\rm Na_{2}CO_{3}$或$\rm NaHCO_{3}$或二者的混合物,再加入盐酸,生成$\rm CO_{2}$气体,则压强变化与图$\rm 2$趋势相似,$\rm A$正确;
$\rm B$.阶段②的压强变小,发生反应$\rm Cl_{2}+2NaOH=NaCl+NaClO+H_{2}O$,可利用该过程发生的反应制备漂白液,$\rm B$正确;
$\rm C$.阶段①说明氯气溶于水,但氯气与水的反应为可逆反应,溶于水的氯气不可能全部与水反应,$\rm C$错误;
$\rm D$.由分析可知,阶段③发生反应的离子方程式为$\text{C}{{\text{l}}^{-}}\text{+Cl}{{\text{O}}^{-}}\text{+2}{{\text{H}}^{+}}\text{=C}{{\text{l}}_{\text{2}}}\uparrow +{{\text{H}}_{\text{2}}}\text{O}$,$\rm D$正确;
故选:$\rm C$
高中 | 氯气题目答案及解析(完整版)
