高中 | 摩尔质量 题目答案及解析
稿件来源:高途
高中 | 摩尔质量题目答案及解析如下,仅供参考!
必修一
第一章 从实验学化学
第二节 化学计量在实验中的应用
摩尔质量
实验小组同学需要配制$\rm 500\ mL\ 0.4\ mol\cdot {{L}^{-1}}\ NaCl$溶液。方法如下:
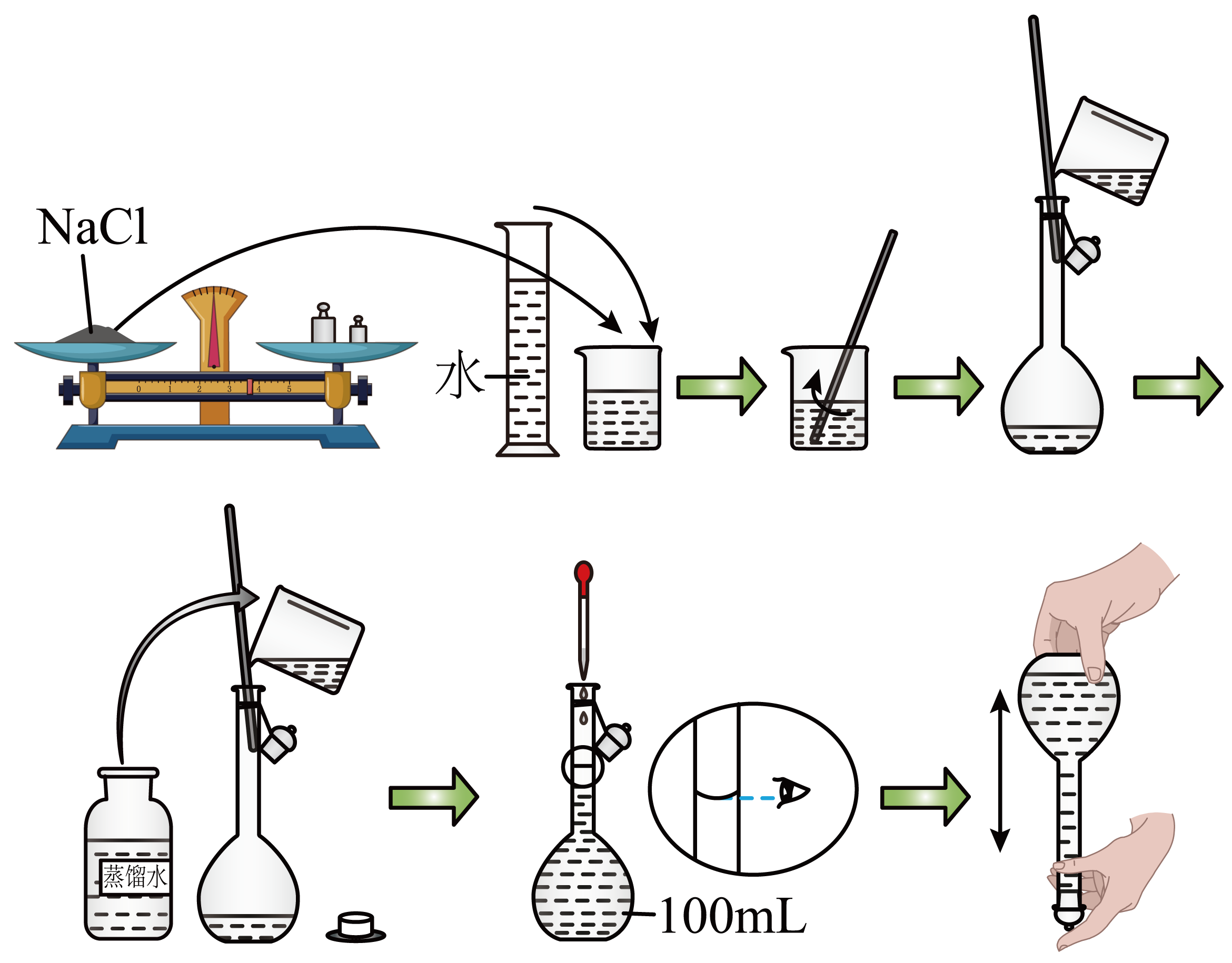
需要称取$\rm NaCl$的质量为 $\rm \ g$。
$\\rm 11.7$
"]]需要称取$\rm NaCl$的质量为$m=c$∙$V$∙$M=0.4\rm \ mol/L\times 0.5\ L\times 58.5\ g/mol=11.7\ g$。
为完成实验,必须用到的玻璃仪器有烧杯、胶头滴管、玻璃棒、量筒和 。
$\\rm 500\\ mL$容量瓶
"]]配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀等,玻璃仪器有烧杯、胶头滴管、玻璃棒、量筒和$\rm 500\ mL$容量瓶,所以缺少的玻璃仪器:$\rm 500\ mL$容量瓶。
在转移溶液时,玻璃棒的作用是 。
引流,防止液体溅出
"]]在转移溶液时,玻璃棒的作用是引流。
配制过程中,下列操作会导致所配溶液物质的量浓度偏小的是 $\rm ($填字母$\rm )$。
$\rm A$.配制溶液所用的容量瓶洗净后没有烘干
$\rm B$.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
$\rm C$.摇匀后,发现溶液的凹液面低于刻度线,又滴加几滴蒸馏水
$\\rm BC$
"]]$\rm A$.配制溶液所用的容量瓶洗净后没有烘干,溶质的物质的量不变,溶液体积也不变,则浓度不变,故$\rm A$不符合题意。
$\rm B$.转移溶液时未洗涤烧杯和玻璃棒,会导致溶质损失,则浓度偏小,故$\rm B$符合题意。
$\rm C$.摇匀后静置,发现液面低于刻度线是正常的,再补加蒸馏水至刻度线,则溶液体积偏多,浓度偏小,故$\rm C$符合题意。
高中 | 摩尔质量题目答案及解析(完整版)
