高中 | 氯气的制法 题目答案及解析
稿件来源:高途
高中 | 氯气的制法题目答案及解析如下,仅供参考!
必修一
第四章 非金属及其化合物
第二节 富集在海水中的元素——氯
氯气的制法
$\rm I$.图中为实验室制取氯气及性质验证的装置图:
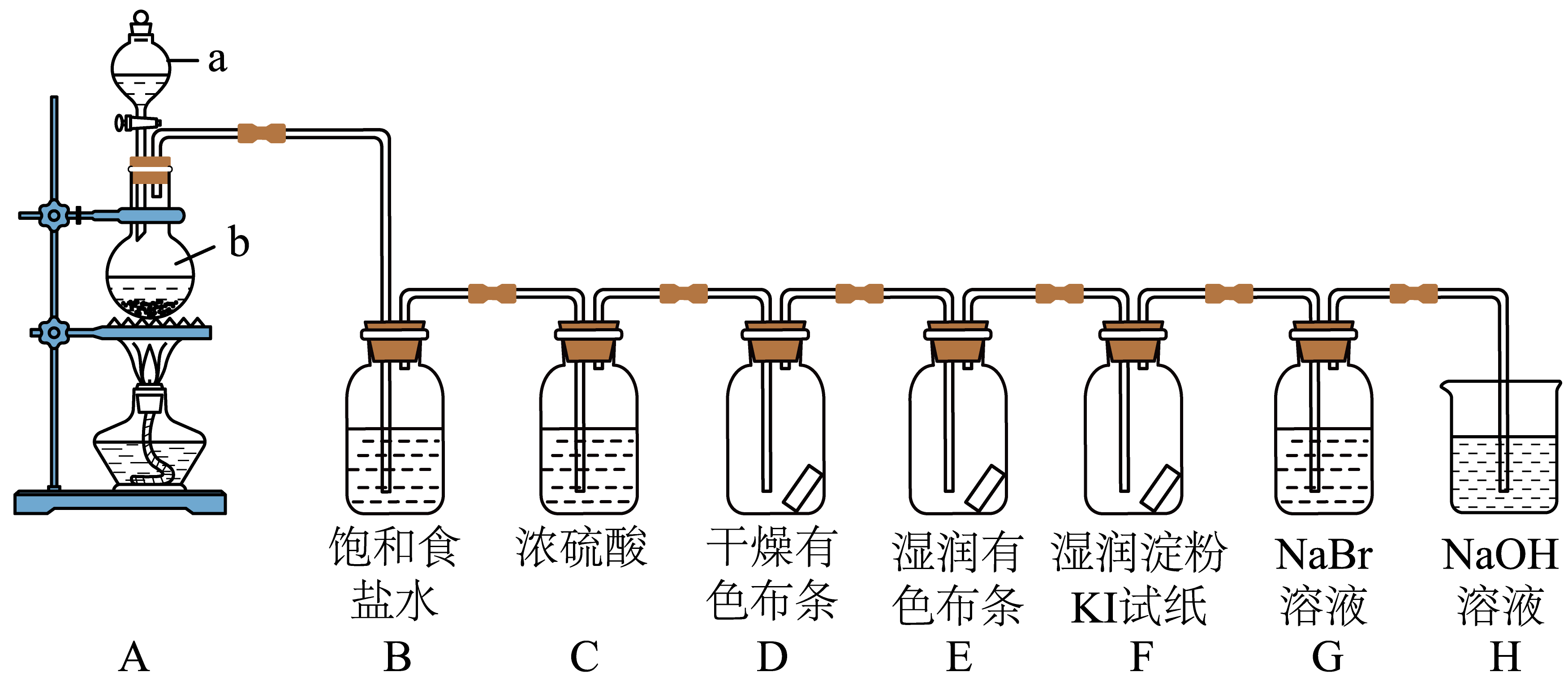
回答下列问题:
仪器$\rm a$的名称 ,写出装置$\rm A$中反应的化学方程式 。
分液漏斗 ; $\\text{Mn}{{\\text{O}}_{2}}+4\\text{HCl(浓)}\\begin{matrix} \\underline{\\underline{_{\\triangle }}} \\\\ {} \\\\\\end{matrix}\\ \\text{MnC}{{\\text{l}}_{\\text{2}}}+\\text{C}{{\\text{l}}_{2}}\\uparrow +2{{\\text{H}}_{2}}\\text{O}$
"]]根据仪器$\rm a$的结构特点可知其为分液漏斗;装置$\rm A$中利用浓盐酸和二氧化锰共热制取$\rm Cl_{2}$,化学方程式为$\rm 4HCl($浓$\rm )$ $+\text{Mn}{{\text{O}}_{2}}\begin{matrix} \underline{\underline{_{\triangle }}} \\ {} \\ \end{matrix}\ \text{MnC}{{\text{l}}_{2}}+\text{C}{{\text{l}}_{2}}\uparrow +2{{\text{H}}_{\text{2}}}\text{O}$;
装置$\rm E$中可观察到的现象是 ,装置$\rm F$中可观察到的现象是 。
有色布条褪色 ; 试纸变蓝
"]]氯气与水反应生成的次氯酸具有漂白性,装置$\rm E$中可观察到的现象是有色布条褪色;氯气具有氧化性,可以将碘离子氧化为碘单质,淀粉遇碘变蓝,所以装置$\rm F$中可观察到的现象是试纸变蓝;
装置$\rm B$的作用为 ,装置$\rm H$的作用为 。
除去$\\text{C}{{\\text{l}}_{2}}$中的$\\rm HCl$气体 ; 吸收多余的$\\text{C}{{\\text{l}}_{2}}$
"]]由于浓盐酸有挥发性,导致生成的氯气中有$\rm HCl$气体,利用装置$\rm B$的饱和食盐水除去$\rm HCl$气体;氯气有毒,会污染环境,$\rm NaOH$溶液可以吸收未反应的氯气,防止污染空气;
$\rm I$$\rm I$.某化学研究性学习小组模拟制备无水$\text{FeC}{{\text{l}}_{3}}$,再用$\text{FeC}{{\text{l}}_{3}}$溶液吸收有毒的${{\text{H}}_{2}}\text{S}$体。
经查阅资料得知:无水$\text{FeC}{{\text{l}}_{3}}$在空气中易潮解,加热易升华,氢硫酸为弱酸。
他们设计了制备无水$\text{FeC}{{\text{l}}_{3}}$的实验方案,装置示意图$\rm ($加热及夹持装置略去$\rm )$及操作步骤如下:
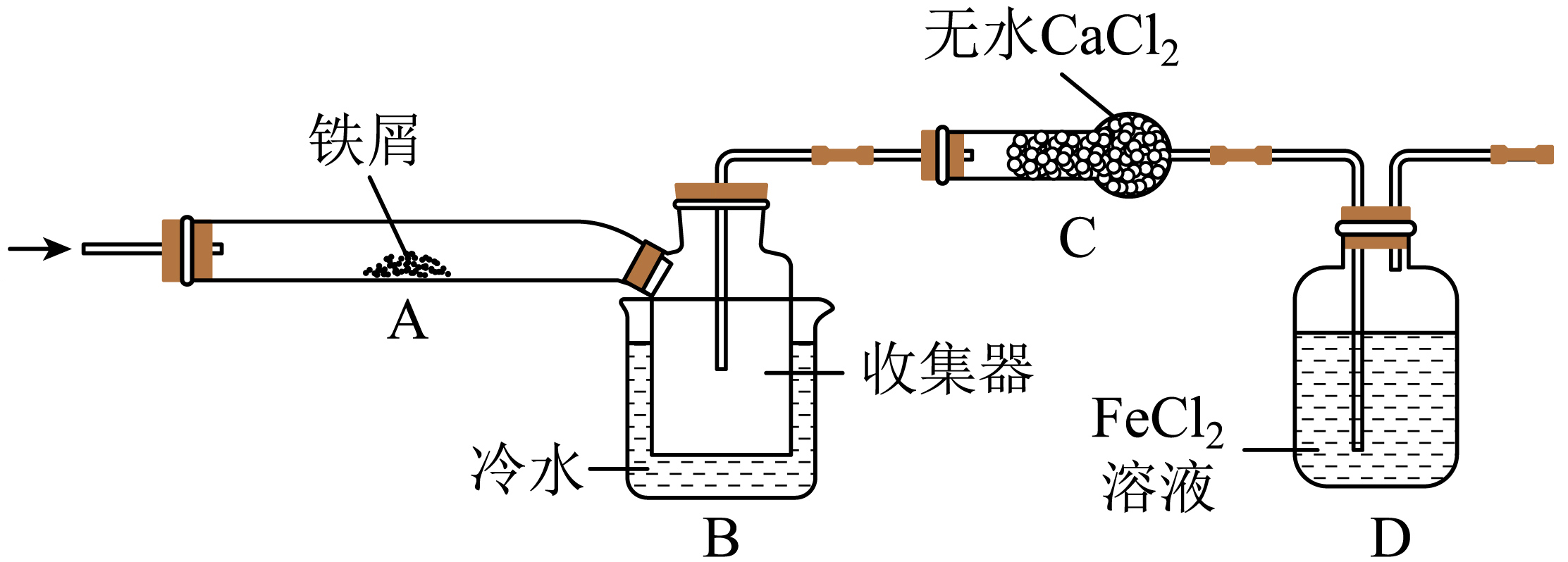
①检验装置的气密性;
②通入干燥的$\text{C}{{\text{l}}_{2}}$,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④∙∙∙∙∙∙
⑤体系冷却后,停止通入$\text{C}{{\text{l}}_{2}}$,并用干燥的${{\text{N}}_{2}}$赶尽$\text{C}{{\text{l}}_{2}}$,将收集器密封。
回答下列问题:
装置$\rm A$中反应的化学方程式为 。
$2\\text{Fe}+3\\text{C}{{\\text{l}}_{2}}\\begin{matrix} \\underline{\\underline{_{\\triangle }}} \\\\ {} \\\\ \\end{matrix}\\ 2\\text{FeC}{{\\text{l}}_{3}}$
"]]氯气具有强氧化性,将变价铁氧化成高价铁,生成氯化铁,所以装置$\rm A$中铁与氯气反应生成氯化铁,反应的方程式为$2\text{Fe}+3\text{C}{{\text{l}}_{2}}\begin{matrix} \underline{\underline{_{\triangle }}} \\ {} \\ \end{matrix}\ 2\text{FeC}{{\text{l}}_{3}}$;
第③步加热后,生成的烟状$\text{FeC}{{\text{l}}_{3}}$大部分进入收集器,少量沉积在反应管$\rm A$右端。要使沉积的$\text{FeC}{{\text{l}}_{3}}$进入收集器,第④步操作应该是 。
在沉积的$\\text{FeC}{{\\text{l}}_{3}}$固体下方加热
"]]第③步加热后,生成的烟状$\rm FeCl_{3}$大部分进入收集器,第④步操作是对准$\rm FeCl_{3}$沉积部位加热发生升华使$\rm FeCl_{3}$进入收集器;
操作步骤中,为防止$\text{FeC}{{\text{l}}_{3}}$潮解所采取的措施有$\rm ($填步骤序号$\rm )$ 。
②⑤
"]]为防止$\rm FeCl_{3}$潮解所采取的措施有②通入干燥的$\rm Cl_{2}$;⑤用干燥的$\rm N_{2}$赶尽$\rm Cl_{2}$;
装置$\rm B$中冷水浴的作用为 。
冷凝氯化铁
"]]装置$\rm B$中冷水浴的作用为冷却$\text{FeC}{{\text{l}}_{3}}$,使$\text{FeC}{{\text{l}}_{3}}$沉积,便于收集产品;
$\text{FeC}{{\text{l}}_{3}}$溶液与${{\text{H}}_{2}}\text{S}$气体反应的离子方程式为 。
$2 \\mathrm{Fe}^{3+}+\\mathrm{H}_{2} \\mathrm{S}=2 \\mathrm{Fe}^{2+}+\\mathrm{S} \\downarrow+2 \\mathrm{H}^{+}$
"]]三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应,离子方程式为$2\text{F}{{\text{e}}^{3+}}+{{\text{H}}_{2}}\text{S}=2\text{F}{{\text{e}}^{2+}}+\text{S}\downarrow \text{+2}{{\text{H}}^{+}}$。
高中 | 氯气的制法题目答案及解析(完整版)
