高中 | 原子晶体 题目答案及解析
稿件来源:高途
高中 | 原子晶体题目答案及解析如下,仅供参考!
选修三
第三章 晶体结构与性质
第二节 分子晶体与原子晶体
原子晶体
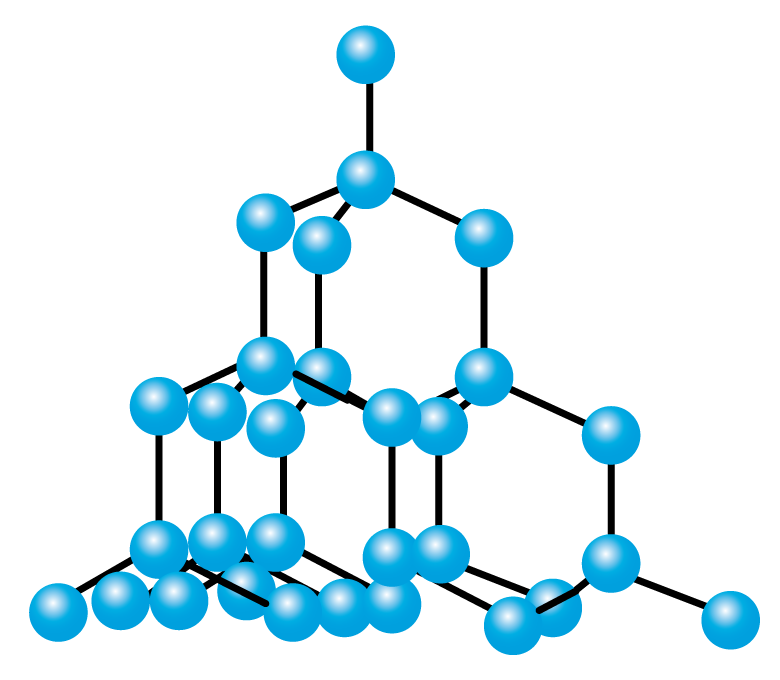
今年,国产$\rm DeepSeek$开源$\rm AI$模型大放异彩。$\rm AI$模型训练需要使用图形处理器$\rm (GPU)$,$\rm GPU$芯片的主要成分是硅,纯硅$\rm ($晶体结构如下图所示$\rm )$的导电性较差,在硅中引入特定的元素$\rm ($如磷、硼等$\rm )$,可以增强其导电性。
下列关于硼的说法中,正确的是$\rm (\qquad)$
硼元素位于元素周期表中的第$\\rm 2$周期第$\\rm 3$族
","硼元素位于元素周期表中的$\\rm s$区
","基态硼原子有$\\rm 2$种不同形状的电子云
","基态硼原子有$\\rm 3$种不同运动状态的电子
"]$\rm A$.硼元素位于元素周期表中第$\rm 2$周期第$\rm IIIA$族,而非第$\rm 3$族,故$\rm A$错误;
$\rm B$.硼为$\rm p$区元素,故$\rm B$错误;
$\rm C$.基态硼原子$\rm (1{{\text{s}}^{2}}2{{\text{s}}^{2}}2{{\text{p}}^{1}}\rm )$有$\rm \text{s}$、$\rm \text{p}$两种形状的电子云,故$\rm C$正确;
$\rm D$.基态硼原子有$\rm 5$个电子,有$\rm 5$种不同运动状态的电子,故$\rm D$错误;
下列关于硅和磷的性质比较中,正确的是$\rm(\qquad) ($不定项$\rm )$
原子半径:$\\text{Si}\\gt \\text{P}$
","第一电离能:$\\text{Si}\\gt \\text{P}$
","熔点:$\\text{Si}\\gt {{\\text{P}}_{4}}\\rm ($白磷$\\rm )$
","酸性:${{\\text{H}}_{2}}\\text{Si}{{\\text{O}}_{3}}\\gt {{\\text{H}}_{3}}\\text{P}{{\\text{O}}_{4}}$
"]$\rm A$.同周期中原子序数越大,原子半径越小,$\rm \text{Si}$ $\rm (14$号$\rm )$原子半径大于$\rm \text{P} (15$号$\rm )$,故$\rm A$正确;
$\rm B$.由于同周期电离能整体越来越大,且$\rm P$的$\rm 3p$处于半充满状态,较稳定,故第一电离能$\rm \text{SiP}$,故$\rm B$错误;
$\rm C$.$\rm \text{Si}$为共价晶体,$\rm {{\text{P}}_{4}}$为分子晶体,一般共价晶体熔沸点比分子晶体熔沸点高,故$\rm \text{Si}\gt {{\text{P}}_{4}}$,故$\rm C$正确;
$\rm D$.$\rm \text{Si}\text{P}$非金属性为$\rm \text{SiP}$,故最高价水化物含氧酸$\rm {{\text{H}}_{2}}\text{Si}{{\text{O}}_{3}}\lt {{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}$,故$\rm D$错误;
当磷原子取代了纯硅中少量硅原子后,能形成导电性较好的$\rm n$型半导体。请从结构的角度解释导电性增强的原因。
磷原子最外层有$\\rm 5$个电子,$\\rm 4$个与硅原子成键后还有一个电子没有成键,该电子在一定条件下可以定向移动而导电
"]]当磷原子取代了纯硅中少量硅原子后,能形成导电性较好的$\rm n$型半导体原因在于磷原子最外层有$\rm 5$个电子,$\rm 4$个与硅原子成键后还有一个电子没有成键,该电子在一定条件下可以定向移动而导电。
高中 | 原子晶体题目答案及解析(完整版)
