高中 | 离子键 题目答案及解析
稿件来源:高途
高中 | 离子键题目答案及解析如下,仅供参考!
必修二
第一章 物质结构 元素周期律
第三节 化学键
离子键
某离子液体结构中,$\rm Q$、$\rm R$、$\rm T$、$\rm X$、$\rm Y$和$\rm Z$是原子序数依次增大的短周期主族元素,基态$\rm T$原子和$\rm Y$原子最外层均有两个单电子,$\rm Q$、$\rm R$、$\rm X$和$\rm Z$质子数均为奇数且和为$\rm 22$,下列说法正确的是$(\qquad)$
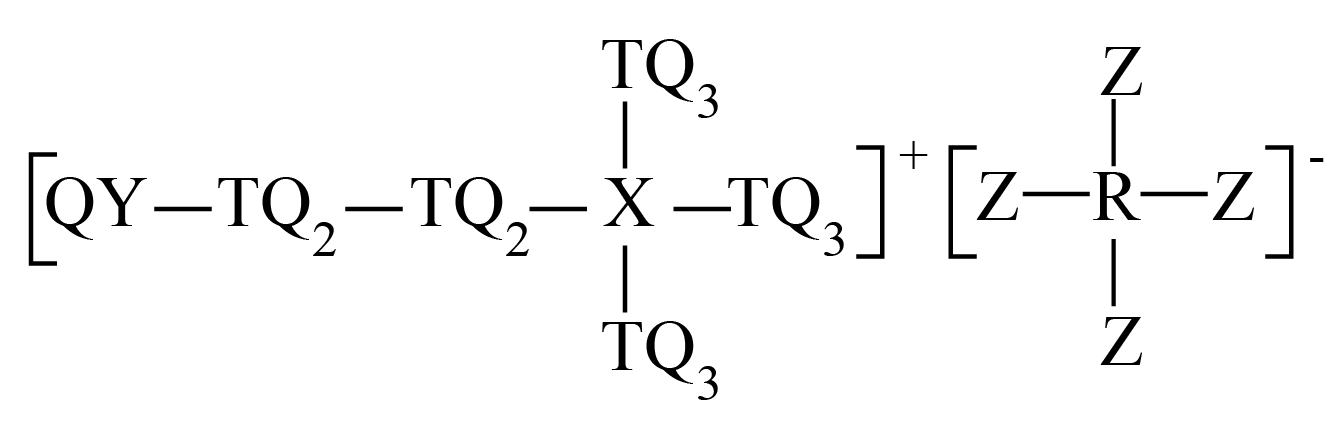
氢化物的沸点:$\\rm {T\\lt X\\lt Y}$
","$\\rm Q$与$\\rm X$形成的一种物质可做燃料
","该物质中所有原子最外层均达到$\\rm 8$电子稳定结构
","该物质的熔点高于$\\text{NaZ}$,难挥发,可做溶剂
"]$\rm Q$、$\rm R$、$\rm T$、$\rm X$、$\rm Y$和$\rm Z$是原子序数依次增大的短周期主族元素,阳离子结构中$\rm Q$只形成一个价键,则$\rm Q$为$\rm IA$族或$\rm VIIA$族元素,阴离子结构中$\rm Z$只形成一个价键,则$\rm Z$为$\rm VIIA$族元素,$\rm Q$、$\rm R$、$\rm X$和$\rm Z$质子数均为奇数且和为$\rm 22$,$\rm Q$的原子序数最小,则$\rm Q$为$\rm H$元素,$\rm Z$为$\rm F$元素;基态$\rm T$原子和$\rm Y$原子最外层均有两个单电子,原子序数小于$\rm F$,则$\rm T$和$\rm Y$的价电子排布式分别为$\rm 2s^{2}2p^{2}$、$\rm 2s^{2}2p^{4}$,即$\rm T$和$\rm Y$分别为$\rm C$、$\rm O$元素;$\rm X$原子序数介于$\rm C$、$\rm O$元素之间,则$\rm X$为$\rm N$元素;$\rm R$的原子序数为$\rm 22-1-7-9=5$,所以$\rm R$为$\rm B$元素,综上所述,$\rm Q$、$\rm R$、$\rm T$、$\rm X$、$\rm Y$和$\rm Z$分别为$\rm H$、$\rm B$、$\rm C$、$\rm N$、$\rm O$、$\rm F$。
$\rm A$.$\rm T$、$\rm X$、$\rm Y$分别为:$\rm C$、$\rm N$、$\rm O$,这些元素能形成的氢化物种类比较多,无法进行比较,$\rm A$错误;
$\rm B$.$\rm Q$与$\rm X$形成的化合物$\rm N_{2}H_{4}$,可以作为燃料,$\rm B$正确;
$\rm C$.$\rm H$原子最外层为$\rm 2$电子稳定结构,$\rm C$错误;
$\rm D$.该物质的阴离子和$\rm F^{-}$一样带一个单位的负电荷,阳离子和$\rm Na^{+}$一样带一个单位的正电荷,但$\rm NaF$的阴、阳离子半径更小,即$\rm NaF$的离子键更强,所以$\rm NaF$的熔点更高,$\rm D$错误。
故选:$\rm B$
高中 | 离子键题目答案及解析(完整版)
