高中 | 分子间作用力 题目答案及解析
稿件来源:高途
高中 | 分子间作用力题目答案及解析如下,仅供参考!
必修二
第一章 物质结构 元素周期律
第三节 化学键
分子间作用力
磷酸铁$\left( \text{FeP}{{\text{O}}_{4}} \right)$常用于制造磷酸铁锂电池、催化剂等材料,可通过如下反应制备:$\text{6FeS}{{\text{O}}_{4}}+6{{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}+\text{NaCl}{{\text{O}}_{3}}+12\text{NaOH}=6\text{FeP}{{\text{O}}_{4}}\cdot 2{{\text{H}}_{2}}\text{O}+\text{NaCl}+6\text{N}{{\text{a}}_{2}}\text{S}{{\text{O}}_{4}}+3{{\text{H}}_{2}}\text{O}$。${{N}_{\text{A}}}$为阿伏加德罗常数的值。下列说法错误的是$(\qquad)$
$1\\text{ L }0.1\\;\\rm \\text{mol}\\cdot {{\\text{L}}^{-1}}\\text{ FeS}{{\\text{O}}_{4}}$溶液中含有的$\\text{F}{{\\text{e}}^{2+}}$数目小于$0.1{{N}_{\\text{A}}}$
","$49\\text{ g }{{\\text{H}}_{3}}\\text{P}{{\\text{O}}_{4}}$中$\\sigma $键的数目为$3.5{{N}_{\\text{A}}}$
","$0.5\\;\\rm \\text{mol }{{\\text{H}}_{2}}\\text{O}\\rm (l)$中含有的氢键数目为${{N}_{\\text{A}}}$
","反应中每转移$1\\;\\rm \\text{mol}$电子生成$\\text{FeP}{{\\text{O}}_{4}}\\cdot 2{{\\text{H}}_{2}}\\text{O}$的数目为${{N}_{\\text{A}}}$
"]$\rm A$.$\rm Fe^{2+}$易水解,$1\text{ L }0.1\;\rm \text{mol}\cdot {{\text{L}}^{-1}}\text{ FeS}{{\text{O}}_{4}}$溶液中含有的$\text{F}{{\text{e}}^{2+}}$数目小于$0.1{{N}_{\text{A}}}$,故$\rm A$错误;
$\rm B$.磷酸的结构式为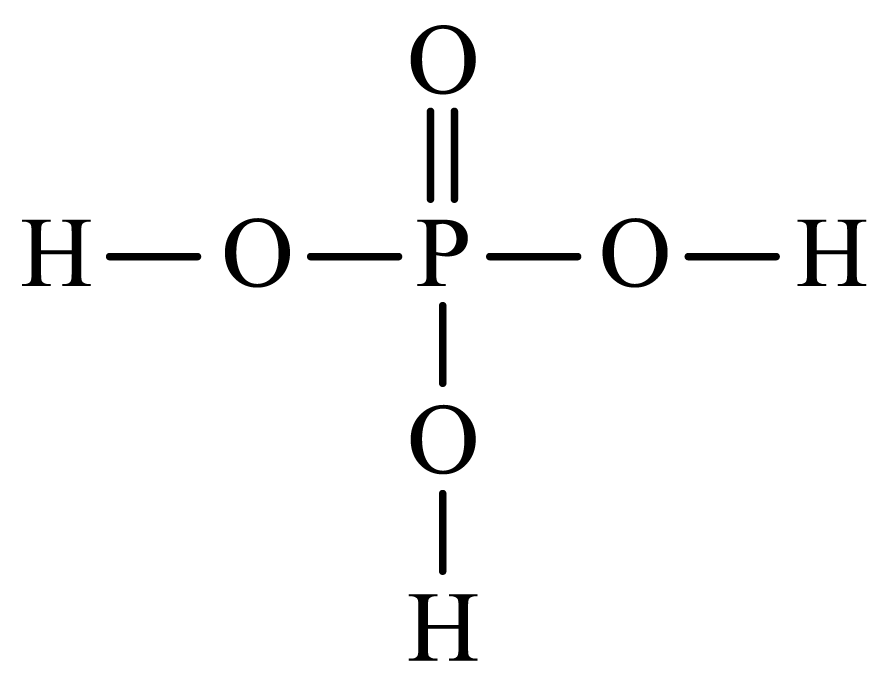 ,$\rm 1$个分子中含有$\rm 7$个$\sigma $键,$49\text{ g }{{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}$的物质的量为$\rm 0.5\;\rm mol$,其中$\sigma $键的数目为$3.5{{N}_{\text{A}}}$,故$\rm B$正确;
,$\rm 1$个分子中含有$\rm 7$个$\sigma $键,$49\text{ g }{{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}$的物质的量为$\rm 0.5\;\rm mol$,其中$\sigma $键的数目为$3.5{{N}_{\text{A}}}$,故$\rm B$正确;
$\rm C$.冰晶体中,每个水分子最多与周围$\rm 4$个水分子形成$\rm 4$个氢键,液态水中的氢键数目小于冰中的氢键数目,$0.5\;\rm \text{mol }{{\text{H}}_{2}}\text{O}\rm (l)$中含有的氢键数目小于${{N}_{\text{A}}}$,故$\rm C$错误;
$\rm D$.反应中,$\rm Fe$元素化合价由$\rm +2$升高为$\rm +3$,每转移$1\;\rm \text{mol}$电子生成$\text{FeP}{{\text{O}}_{4}}\cdot 2{{\text{H}}_{2}}\text{O}$的数目为${{N}_{\text{A}}}$,故$\rm D$正确。
故选:$\rm C$
高中 | 分子间作用力题目答案及解析(完整版)
