高中 | 原电池工作原理 题目答案及解析
稿件来源:高途
高中 | 原电池工作原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第一节 原电池
原电池工作原理
某$\text{LiFeP}{{\text{O}}_{4}}$电池的切面结构示意图如图所示,放电时的反应为$\text{L}{{\text{i}}_{x}}{{\text{C}}_{6}}+\text{L}{{\text{i}}_{1-x}}\text{FeP}{{\text{O}}_{4}}=6\text{C}+\text{LiFeP}{{\text{O}}_{4}}$。下列说法错误的是$(\quad\ \ \ \ )$
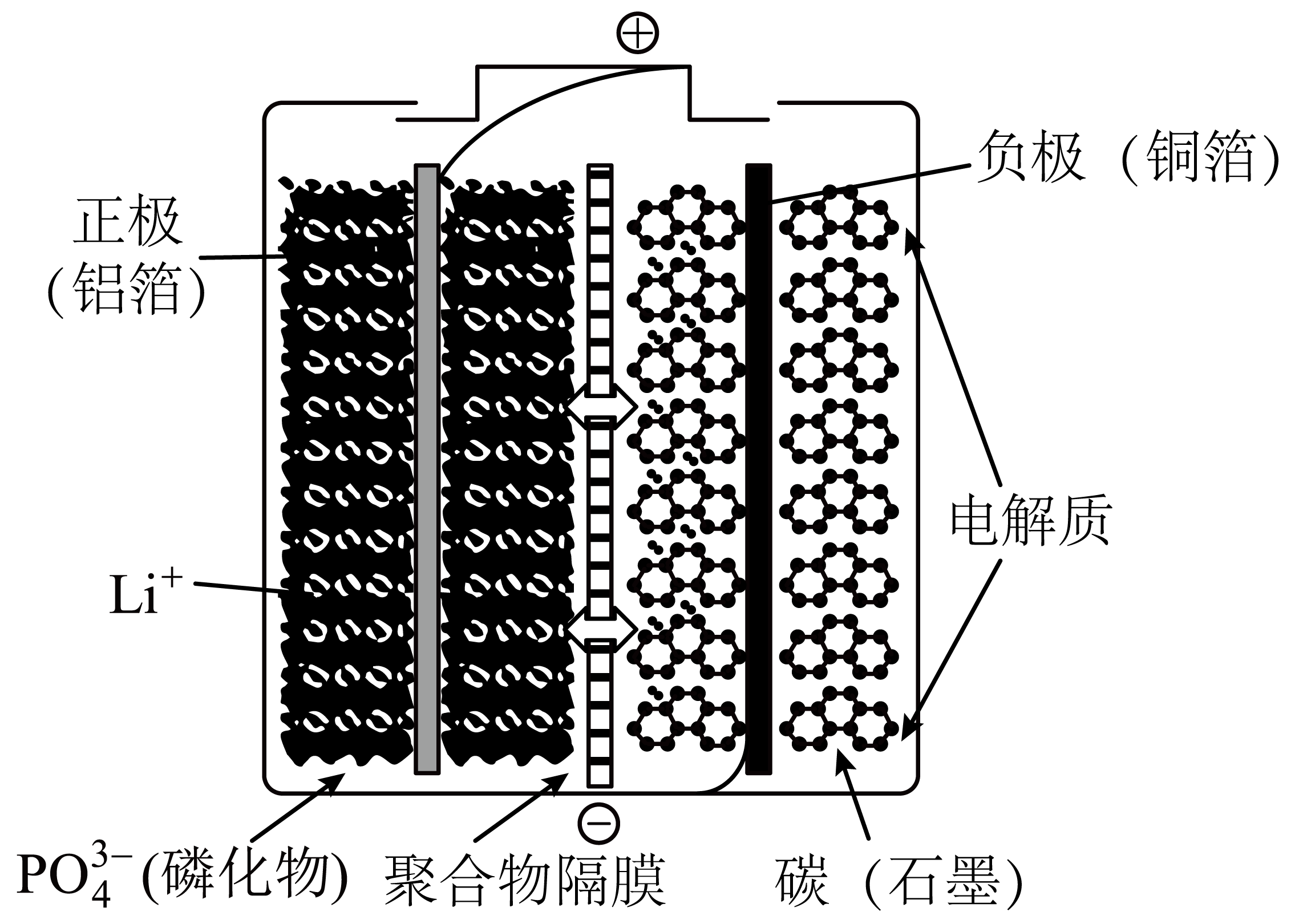
该电池工作时,$\\text{L}{{\\text{i}}^{+}}$向正极移动
","聚合物隔膜为阳离子交换膜
","放电时,正极的电极反应为$\\text{L}{{\\text{i}}_{\\text{1-}x}}\\text{FeP}{{\\text{O}}_{\\text{4}}}+x{{\\text{e}}^{-}}+x\\text{L}{{\\text{i}}^{+}}=\\text{LiFeP}{{\\text{O}}_{\\text{4}}}$
","若初始两电极质量相等,放电转移$2{{N}_{\\text{A}}}$个电子,则两电极的质量差为$14\\,\\text{g}$
"]根据电池反应:$\text{L}{{\text{i}}_{x}}{{\text{C}}_{6}}+\text{L}{{\text{i}}_{1-x}}\text{FeP}{{\text{O}}_{4}}=6\text{C}+\text{LiFeP}{{\text{O}}_{4}}$可知正极反应为:$\text{L}{{\text{i}}_{1-x}}\text{FeP}{{\text{O}}_{4}}+x\text{L}{{\text{i}}^{+}}+x{{\text{e}}^{-}}=\text{LiFeP}{{\text{O}}_{4}}$,负极反应为:$\text{L}{{\text{i}}_{x}}{{\text{C}}_{6}}-x{{\text{e}}^{-}}=6\text{C}+x\text{L}{{\text{i}}^{+}}$。
$\rm A$.放电时,阳离子向正极移动,则该电池工作时,$\text{L}{{\text{i}}^{+}}$向正极移动,$\rm A$正确;
$\rm B$.根据分析可知$\text{L}{{\text{i}}^{+}}$通过隔膜向正极移动,则隔膜为阳离子交换膜,$\rm B$正确;
$\rm C$.根据分析可知放电时正极反应为:$\text{L}{{\text{i}}_{\text{1-}x}}\text{FeP}{{\text{O}}_{\text{4}}}+x{{\text{e}}^{-}}+x\text{L}{{\text{i}}^{+}}=\text{LiFeP}{{\text{O}}_{\text{4}}}$,$\rm C$正确;
$\rm D$.放电转移$2{{N}_{\text{A}}}$个电子,负极减少了$2\,\text{mol}\,\text{Li}$,正极增加了$2\,\text{mol}\,\text{Li}$,则两电极的质量差为$28\,\text{g}$,$\rm D$错误;
故选:$\rm D$
高中 | 原电池工作原理题目答案及解析(完整版)
