高中 | 化学平衡常数 题目答案及解析
稿件来源:高途
高中 | 化学平衡常数题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
化学平衡常数
甲醇水蒸气重整制氢是生产氢气的重要途径,其主要反应为:
Ⅰ.$\text{C}{{\text{H}}_{3}}\text{OH}\left( \text{g} \right)+{{\text{H}}_{2}}\text{O}\left( \text{g} \right)\rightleftharpoons \text{C}{{\text{O}}_{2}}\left( \text{g} \right)+3{{\text{H}}_{2}}\left( \text{g} \right)\qquad \Delta {{H}_{1}}=+49.4\;\rm \text{kJ}\cdot \text{mo}{{\text{l}}^{-1}}$
Ⅱ.$\text{C}{{\text{H}}_{3}}\text{OH}\left( \text{g} \right)\rightleftharpoons \text{CO}\left( \text{g} \right)+2{{\text{H}}_{2}}\left( \text{g} \right)\qquad \Delta {{H}_{2}}=+90.6\;\rm \text{kJ}\cdot \text{mo}{{\text{l}}^{-1}}$
$1.01\times {{10}^{5}}\ \text{Pa}$$、$$n_{起始}\left( \text{H}_{2}\text{O}\right):n_{起始}\left( \text{C}\text{H}_{3}\text{OH}\right)=1.2:1$时,混合气体以一定流速通过反应管,在催化剂作用下反应一段时间后测得$\text{C}{{\text{H}}_{3}}\text{OH}$转化率、CO选择性[$ \dfrac{{{n}_{生成}}\left( \text{CO} \right)}{{{n}_{反应}}\left( \text{C}{{\text{H}}_{3}}\text{OH} \right)}\times 100$%]随温度的变化如图所示。下列说法正确的是$(\qquad)$
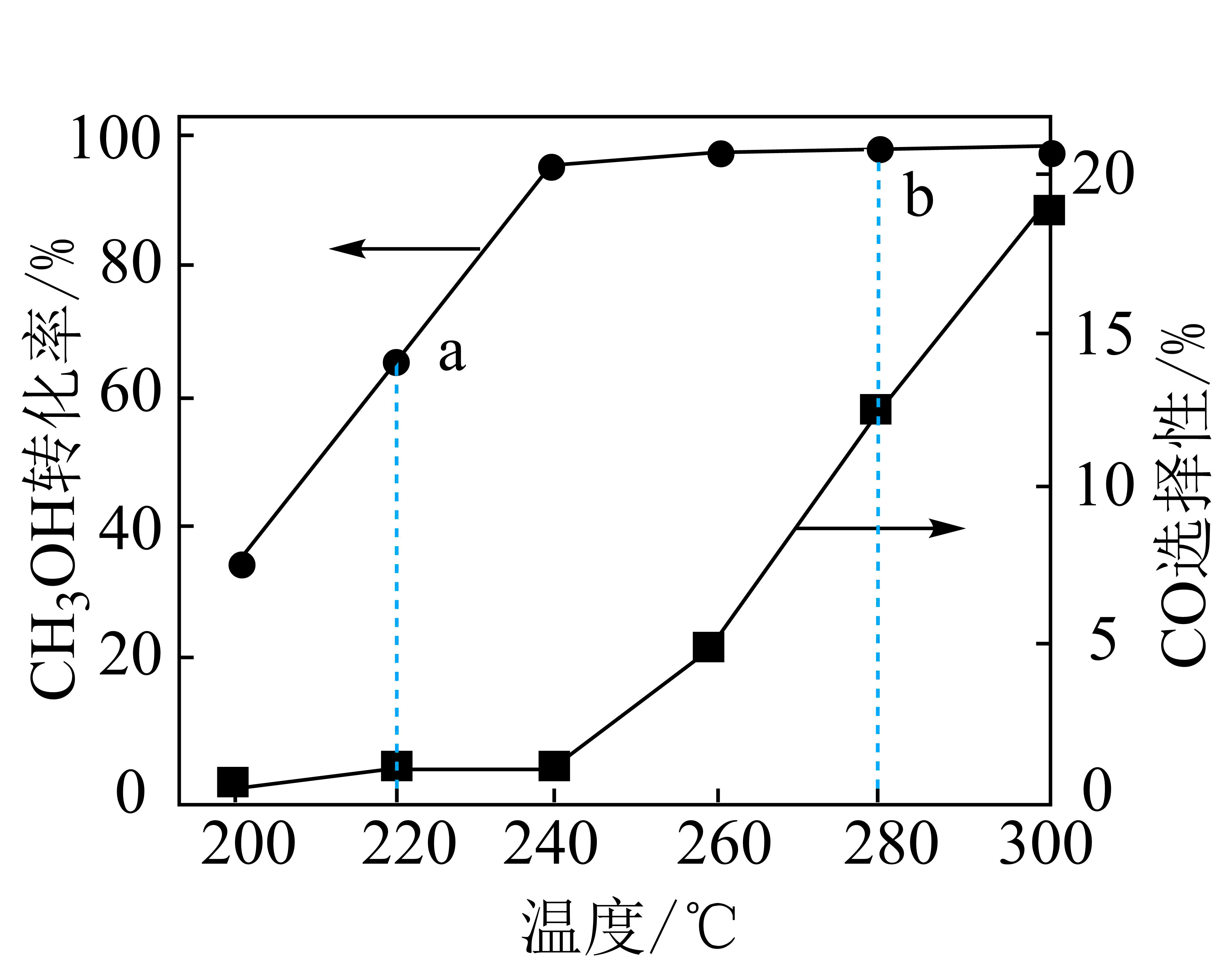
反应Ⅱ的平衡常数:$K_{220\\;\\rm^\\circ\\rm C}\\gt K_{280\\;\\rm^\\circ\\rm C}$
","$\\text{C}{{\\text{O}}_{2}}$的物质的量:$\\rm a$点$\\rm \\lt b$点
","其他条件不变,混合气体流速越大,$\\text{C}{{\\text{H}}_{3}}\\text{OH}$的转化率越大
","温度高于$\\rm 240\\;\\rm ^\\circ\\rm C$,$\\rm CO$选择性迅速上升的原因是反应Ⅱ速率大于反应Ⅰ
"]$\rm A$.反应Ⅱ为吸热反应,温度升高,反应Ⅱ的$K$值增大,其平衡常数:$\textit{K}_{\text{220}\;\rm ^\circ\rm C}\gt \textit{K}_{\text{280}\;\rm ^\circ\rm C}$,$\rm A$错误;
$\rm B$.$1.01\times {{10}^{5}}\;\rm \text{Pa}$、$n_{起始}\left( \text{H}_{2}\text{O}\right):n_{起始}\left( \text{C}\text{H}_{3}\text{OH}\right)=1.2:1$时,设起始甲醇物质的量为$\rm 1\;\rm mol$,$\rm a$点$\text{C}{{\text{H}}_{3}}\text{OH}$转化率较低$\rm ($约为$\rm 65\%)$、$\rm CO$选择性很低$\rm ($约为$\rm 2\%)$,则$n\rm(CO)=1\;\rm mol\times 65\%\times 2\%=0.013\;\rm mol$,$n\rm (CO_{2})=0.65\;\rm mol-0.013\;\rm mol=0.637\;\rm mol$,$\rm b$点$\text{C}{{\text{H}}_{3}}\text{OH}$转化率较高$\rm ($约为$\rm 95\%)$、$\rm CO$选择性相对较高$\rm ($约为$\rm 12\%)$,则$n\rm (CO)=1\;\rm mol\times 95\%\times 12\%=0.114\;\rm mol$,$n\rm (CO_{2})=0.95\;\rm mol-0.114\;\rm mol=0.836\;\rm mol$,故$\text{C}{{\text{O}}_{2}}$的物质的量:$\rm a$点$\rm \lt b$点,$\rm B$正确;
$\rm C$.其他条件不变,混合气体流速越大,$\text{C}{{\text{H}}_{3}}\text{OH}$不能完全反应,故转化率不一定越大,$\rm C$错误;
$\rm D$.温度高于$\rm 240\;\rm ^\circ\rm C$,甲醇的转化率基本不变、$\rm CO$选择性迅速上升,说明反应Ⅱ速率随温度增大的程度大于反应Ⅰ,但是无法得出反应Ⅱ速率大于反应Ⅰ,$\rm D$错误;
故选:$\rm B$
高中 | 化学平衡常数题目答案及解析(完整版)
