高中 | 配合物理论 题目答案及解析
稿件来源:高途
高中 | 配合物理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
配合物理论
在元素周期表中,某些主族元素与右下方的主族元素的某些性质是相似的。如:$\text{Be}{{\left( \text{OH} \right)}_{2}}$和$\text{Al}{{\left( \text{OH} \right)}_{3}}$均为两性氢氧化物,$\text{Be}{{\left( \text{OH} \right)}_{2}}$溶于强碱形成${{\left[ \text{Be}{{\left( \text{OH} \right)}_{4}} \right]}^{2-}}$;$\rm BeO$和$\text{A}{{\text{l}}_{2}}{{\text{O}}_{3}}$都具有难溶于水、高熔点等性质。$\text{BeC}{{\text{l}}_{2}}$和$\text{AlC}{{\text{l}}_{3}}$在气态时通常以二聚体的形式存在。$\rm B$和$\rm Si$均能溶于$\rm NaOH$溶液生成盐和${{\text{H}}_{2}}$。工业上用焦炭和$\text{Si}{{\text{O}}_{2}}$在高温下反应制粗硅。硼酸$\rm ({{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}\rm )$和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列说法正确的是$(\qquad)$
$\\text{AlC}{{\\text{l}}_{3}}$二聚体中含有配位键
","${{\\left[ \\text{Be}{{\\left( \\text{OH} \\right)}_{4}} \\right]}^{2-}}$的空间结构为平面正方形
","$\\text{Si}{{\\text{O}}_{2}}$中的$\\text{O}-\\text{Si}-\\text{O}$键角为$\\rm 180^\\circ$
","${{\\text{H}}_{3}}\\text{B}{{\\text{O}}_{3}}$晶体在常温下能导电
"]$\rm A$.$\text{AlC}{{\text{l}}_{3}}$二聚体结构为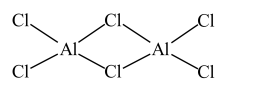 ,$\rm Al$最外层电子数为$\rm 3$,存在配位键,$\rm A$正确;
,$\rm Al$最外层电子数为$\rm 3$,存在配位键,$\rm A$正确;
$\rm B$.${{\left[ \text{Be}{{\left( \text{OH} \right)}_{4}} \right]}^{2-}}$的中心原子为$\rm Be$,$\rm Be$原子和四个$\rm OH^{-}$形成$\rm 4$个共价键,无孤电子对,为$\rm sp^{3}$杂化,空间结构为正四面体形,$\rm B$错误;
$\rm C$.$\rm Si$和$\rm O$构成了硅氧四面体,其结构如图: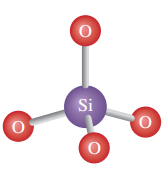 每个$\rm Si$结合$\rm 4$个$\rm O$,$\rm Si$ 在中心,$\rm O$在四面体的$\rm 4$个顶角,$\text{O}-\text{Si}-\text{O}$键角不是$\rm 180^\circ$,$\rm C$错误;
每个$\rm Si$结合$\rm 4$个$\rm O$,$\rm Si$ 在中心,$\rm O$在四面体的$\rm 4$个顶角,$\text{O}-\text{Si}-\text{O}$键角不是$\rm 180^\circ$,$\rm C$错误;
$\rm D$.${{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$晶体有类似于石墨的片层状结构,但$\rm B$最外层电子数为$\rm 3$,形成了$\rm 3$个共价键,为$\rm sp^{2}$杂化,与石墨具有自由电子的结构不同,无法导电,$\rm D$错误;
故选:$\rm A$
高中 | 配合物理论题目答案及解析(完整版)
