高中 | 盖斯定律 题目答案及解析
稿件来源:高途
高中 | 盖斯定律题目答案及解析如下,仅供参考!
选修四
第一章 化学反应与能量
第三节 化学反应热的计算
盖斯定律
向丙烷脱氢制丙烯的反应体系中加入$\text{C}{{\text{O}}_{2}}$,可以提高丙烷的利用率。在相同温度下,分别将投料比相同的$\mathrm{CO}_2-\mathrm{C}_3 \mathrm{H}_8$、$\rm N_{2}-\mathrm{C}_{3}\mathrm{H}_{8}$混合气体以相同流速持续通过同种催化剂表面,${{\text{C}}_{3}}{{\text{H}}_{8}}$转化率和${{\text{C}}_{3}}{{\text{H}}_{6}}$选择性随通入气体时间的变化如图:
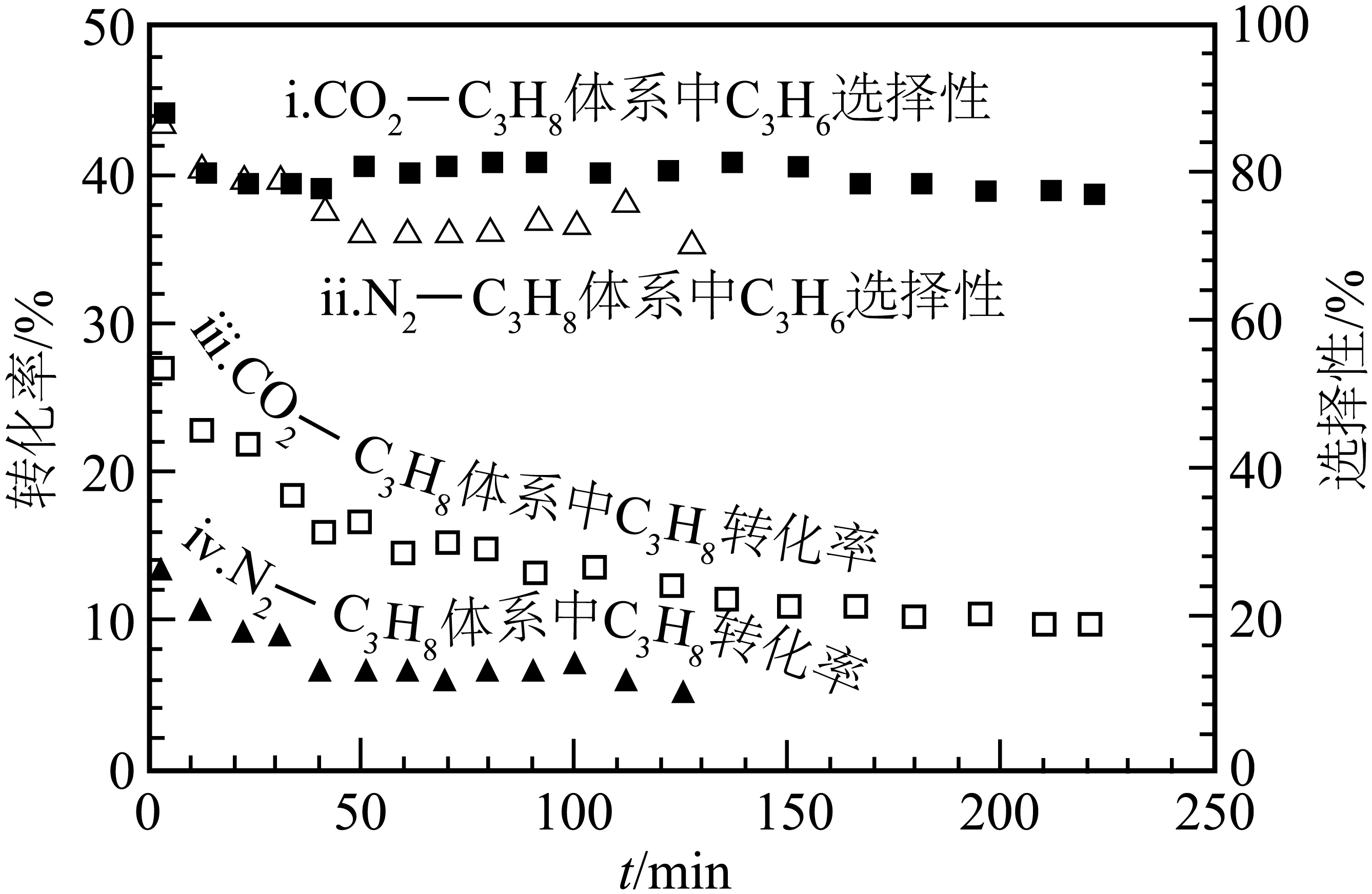
已知:I.反应①${{\text{C}}_{3}}{{\text{H}}_{8}}(\text{g})\rightleftharpoons {{\text{C}}_{3}}{{\text{H}}_{6}}(\text{g})+{{\text{H}}_{2}}(\text{g})\qquad\Delta{{H}_{1}}=+124\;\rm \text{kJ}\cdot \text{mo}{{\text{l}}^{-1}}$
反应②${{\text{H}}_{2}}(\text{g})+\text{C}{{\text{O}}_{2}}(\text{g})\rightleftharpoons {{\text{H}}_{2}}\text{O}(\text{g})+\text{CO}(\text{g})\qquad\Delta{{H}_{2}}=+41.2\;\rm \text{kJ}\cdot \text{mo}{{\text{l}}^{-1}}$
Ⅱ.反应体系中存在${{\text{C}}_{3}}{{\text{H}}_{8}}$的裂解和生成积炭等副反应。
Ⅲ.${{\text{C}}_{3}}{{\text{H}}_{6}}$的选择性$=\dfrac{n\left(生成 \text{C}_{3}\text{H}_{6}所用的\text{C}_{3}\text{H}_{8}\right)}{n\left( 反应消耗的\text{C}_{3}\text{H}_{8}\right)}\times100\%$
下列说法正确的是$(\qquad)$
${{\\text{C}}_{3}}{{\\text{H}}_{8}}(\\text{g})+\\text{C}{{\\text{O}}_{2}}(\\text{g})\\rightleftharpoons {{\\text{C}}_{3}}{{\\text{H}}_{6}}(\\text{g})+{{\\text{H}}_{2}}\\text{O}(\\text{g})+\\text{CO}(\\text{g})\\qquad \\Delta H=+82.8\\;\\rm \\text{kJ}\\cdot \\text{mo}{{\\text{l}}^{-1}}$
","$\\rm 30\\;\\rm min$内,两体系中${{\\text{C}}_{3}}{{\\text{H}}_{6}}$选择性相同,生成${{\\text{C}}_{3}}{{\\text{H}}_{6}}$的速率也相同
","$\\rm iii$中的${{\\text{C}}_{3}}{{\\text{H}}_{8}}$转化率高于$\\rm iv$中的,是因为反应②使反应①的平衡正向移动
","$\\rm iii$、$\\rm iv$对比,$\\rm 150\\;\\rm min$后$\\rm iv$中${{\\text{C}}_{3}}{{\\text{H}}_{8}}$转化率为$\\rm 0$,可能是因为积炭使催化剂失效
"]$\rm A$.由盖斯定律可知,反应①$\rm +$②可得反应${{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}\text{(g)+C}{{\text{O}}_{\text{2}}}\text{(g)}\rightleftharpoons {{\text{C}}_{\text{3}}}{{\text{H}}_{\text{6}}}\text{(g)+}{{\text{H}}_{\text{2}}}\text{O(g)+CO(g)}$,则反应$ \Delta H=(+124\;\rm kJ/mol)+$ $\rm (+41.2\;\rm kJ/mol)=$ $\rm +162.5\;\rm kJ/mol$,故$\rm A$错误;
$\rm B$.由图可知,$\rm 30\;\rm min$内,两体系中丙烯的选择性相同,但二氧化碳的转化率不同,所以生成丙烯的物质的量不同,反应的反应速率不同,故$\rm B$错误;
$\rm C$.由图可知,$\rm iii$中的丙烷转化率高于$\rm iv$中的丙烷转化率是因为$\rm C{{O}_{\text{2}}}$可以消除积炭而使催化剂保持较高的活性,反应速率快,故$\rm C$错误;
$\rm D$.二氧化碳能与碳共热反应生成一氧化碳,$\rm iii$、$\rm iv$对比,$\rm 150\;\rm min$后$\rm iv$中丙烷转化率为$\rm 0$可能是丙烷分解生成的碳附着在催化剂表面导致催化剂失效,使得反应无法进行,故$\rm D$正确;
故选:$\rm D$
高中 | 盖斯定律题目答案及解析(完整版)
