高中 | 电解原理的应用 题目答案及解析
稿件来源:高途
高中 | 电解原理的应用题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第三节 电解池
电解原理的应用
普通电解精炼铜的方法所制备的铜中仍含杂质,利用如图中的双膜(阴离子交换膜和过滤膜)电解装置可制备高纯度的$\rm Cu$.下列有关叙述正确的是$(\quad\ \ \ \ )$
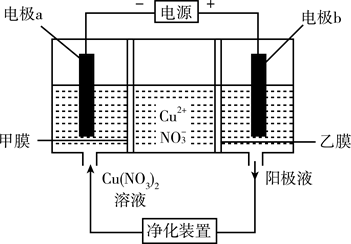
["
电极 $\\rm a$ 为粗铜
","甲膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区
","乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区
","当电路中通过 $\\rm 1\\text{ }mol$ 电子时,可生成 $\\rm 32\\text{ }g$ 精铜
"][["D"]]
A.电极$\rm a$为阴极,为纯铜,故A错误;
B.甲膜为阴离子交换膜,可阻止杂质阳离子进入阴极区,故B错误;
C.电极$\rm b$为阳极,为粗铜,电极反应:$\rm Cu-2{{e}^{-}}=C{{u}^{2+}}$,乙膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区,故C错误;
D.阳极电极反应:$\rm Cu-2{{e}^{-}}=C{{u}^{2+}}$,阴极电极反应:$\rm C{{u}^{2+}}+2{{e}^{-}}=Cu$,电路中通过$\rm 1\text{ }mol$电子,生成铜物质的量为 $\rm 0.5\text{ }mol$,生成铜质量为 $\rm 0.5\text{ }mol\times64\text{ }g/mol=32\text{ }g$,故D正确。
故选:D
高中 | 电解原理的应用题目答案及解析(完整版)
去刷题
今日推荐 ![]()
![]()
![]()
