高中 | 氮的固定和自然界中氮的循环 题目答案及解析
稿件来源:高途
高中 | 氮的固定和自然界中氮的循环题目答案及解析如下,仅供参考!
必修一
第四章 非金属及其化合物
第四节 氨 硝酸 硫酸
氮的固定和自然界中氮的循环
Ⅰ.我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
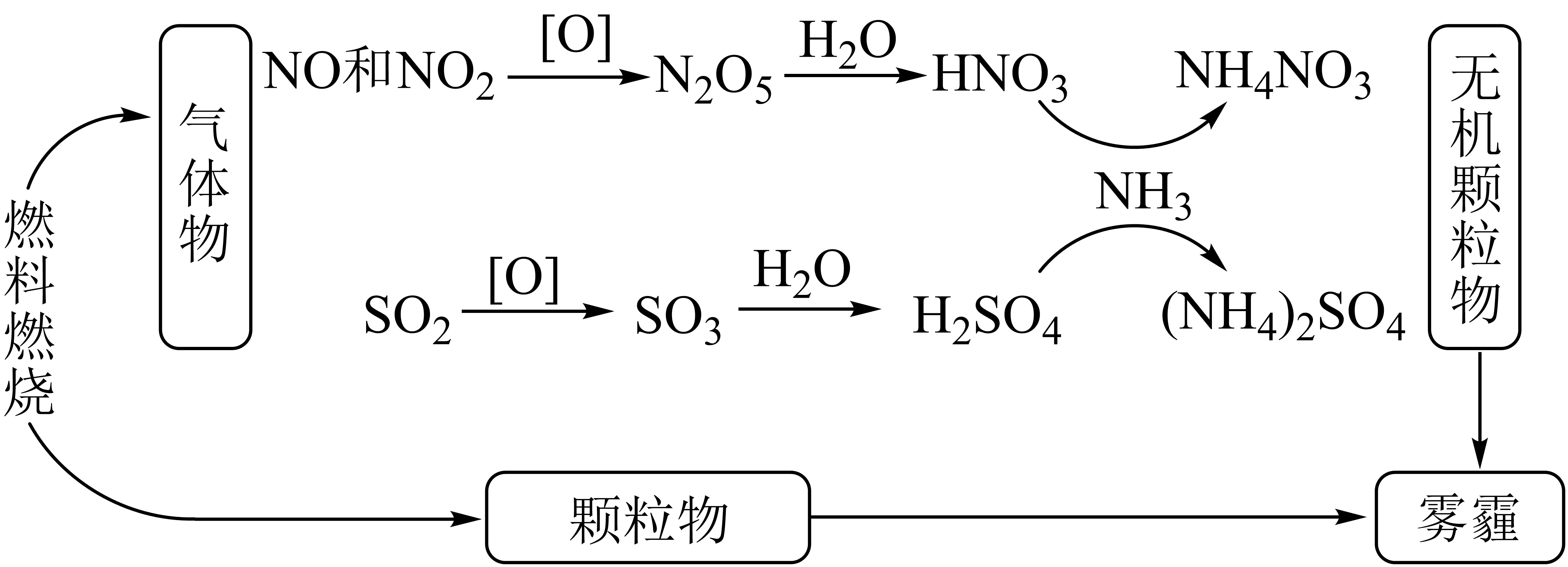
回答下列问题:
从物质分类的角度看,图中的物质属于酸性氧化物的有 种。
$\\rm 3$
"]]酸性氧化物是能与碱反应只生成盐和水的氧化物,图中:$\rm N_{2}O_{5}$、$\rm SO_{2}$、$\rm SO_{3}$属于酸性氧化物,共计$\rm 3$种。
工业上利用氨气制备一氧化氮,化学方程式为$ {m\rm N}{{\text{H}}_{3}}+ {n}{{\text{O}}_{2}}\to {p\rm NO}+\square $,配平后$\rm □$中应填 。
$\\rm H_{2}O$
"]]根据原子守恒可知,工业上利用氨气制备一氧化氮,化学方程式为$ {m\rm N}{{\text{H}}_{3}}+ {n}{{\text{O}}_{2}}\to {p\rm NO}+\square $,配平后$\rm □$中应填$\rm H_{2}O$。
下列关于雾霾叙述正确的是$(\quad\ \ \ \ )$。
雾和霾的分散质相同
","雾霾中含有硝酸铵和硫酸铵
","大气中的氨气在反应过程中被氧化
","雾霾的形成与过度施用氮肥、燃料燃烧有关
"]$\rm A$.雾的分散质是小液滴,霾的分散质含有固体小颗粒,故$\rm A$错误:
$\rm B$.由图示信息可知雾霾中含有硝酸铵和硫酸铵,故$\rm B$正确;
$\rm C$.$\rm NH_{3}$是形成无机颗粒物的反应物,做碱性气体,其$\rm N$和$\rm H$元素化合价未发生变化,所以没有被氧化,故$\rm C$错误;
$\rm D$.过度施用氮肥或燃料燃烧会增加空气中氮氧化物的排放,促使雾霾的形成,故$\rm D$正确。
Ⅱ.化肥工业产生的氨氮废水$\rm ($主要含$\text{NH}_{4}^{+}\rm )$,可造成水体富营养化。某研究团队设计处理氨氮废水流程如下:

过程①加热条件下生成氨气。请写出该过程的离子方程式 。
$\\rm NH_{4}^{+}+O{{H}^{-}}\\begin{array}{*{20}{c}}{\\underline{\\underline {\\triangle}} }\\\\{}\\end{array}N{{H}_{3}}\\uparrow +{{\\text{H}}_{2}}\\text{O}$
"]]铵根离子与氢氧根离子在加热条件下会生成氨气和水,其离子方程式为:$\rm NH_{4}^{+}+O{{H}^{-}}\begin{array}{*{20}{c}}{\underline{\underline {\triangle}} }\\{}\end{array}N{{H}_{3}}\uparrow +{{\text{H}}_{2}}\text{O}$。
过程②中控制溶液为酸性,在微生物作用下实现$\rm \text{NH}_{4}^{+}\to \text{NO}_{3}^{-}$,请写出该过程的离子方程式 。
$\\rm NH_{4}^{+}+2{{\\text{O}}_{2}}\\overset{}{\\mathop{=}}\\,NO_{3}^{-}+2{{\\text{H}}^{+}}+{{\\text{H}}_{2}}\\text{O}$
"]]在酸性条件下铵根离子被氧气氧化成硝酸根离子的反应离子方程式为$\rm NH_{4}^{+}+2{{\text{O}}_{2}}\overset{}{\mathop{=}}\,NO_{3}^{-}+2{{\text{H}}^{+}}+{{\text{H}}_{2}}\text{O}$。
过程③:一定条件下向废水中加入$\text{C}{{\text{H}}_{3}}\text{OH}$,实现$\text{HN}{{\text{O}}_{3}}\to {{\text{N}}_{2}}$,称为反硝化过程。其中$\text{C}{{\text{H}}_{\text{3}}}\text{OH}$的作用为 。
起还原性
"]]$\text{HN}{{\text{O}}_{3}}\to {{\text{N}}_{2}}$转化中$\rm N$的化合价降低,所以实现此转化需要加入还原剂,则加入甲醇的作用为:起还原性。
②中${{\text{O}}_{2}}$可用$\rm NaClO$替代,此时含氮化合物可被氧化为${{\text{N}}_{2}}$,将一定量的氨氮废水与不同量的$\rm NaClO$混合,测得溶液中氨氮去除率、总氮$\rm ($溶液中所有可溶性的含氮化合物中氮元素的总量$\rm )$去除率与$\rm NaClO$投入量$\rm ($用$x$表示$\rm )$的关系如图所示。

当$x\text{(NaClO}\gt {{x}_{1}})$时,水体中总氮去除率下降,可能的原因是 。
有部分氨氮被氧化为$\\text{NO}_{3}^{-}$等可溶性离子留在废水中
"]]当$x\text{(NaClO}\gt {{x}_{1}})$时,水体中总氮去除率下降,可能的原因是有部分氨氮被氧化为$\text{NO}_{3}^{-}$等可溶性离子留在废水中。
高中 | 氮的固定和自然界中氮的循环题目答案及解析(完整版)
