高中 | 氧化性、还原性强弱的比较 题目答案及解析
稿件来源:高途
高中 | 氧化性、还原性强弱的比较题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化性、还原性强弱的比较
某小组同学探究浓硫酸的性质,向试管①、②中加入等量的$\rm 98\%$的浓硫酸,实验如下。
| 实验$\rm 1$ | 实验$\rm 2$ | 实验$\rm 3$ | |
| 装置 |  | 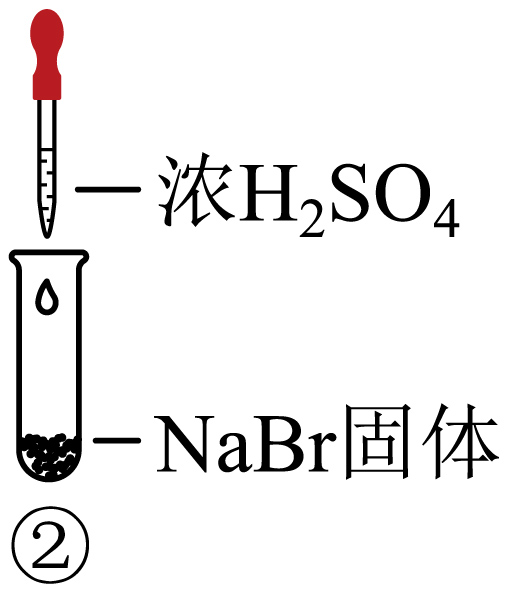 |  |
| 现象 | 溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟 | 溶液变黄;把湿润的品红试纸靠近试管口,试纸褪色 | 溶液变深紫色$\rm ($经检验溶液含单质碘$\rm )$ |
下列对实验的分析不合理的是$(\qquad)$
实验$\\rm 1$中,白烟是$\\rm NH_{4}Cl$
","根据实验$\\rm 1$和实验$\\rm 2$判断还原性:$\\rm Br^{-}\\gt Cl^{-}$
","根据实验$\\rm 3$判断还原性:$\\rm I^{-}\\gt Br^{-}$
","上述实验体现了浓$\\rm H_{2}SO_{4}$的强氧化性、难挥发性等性质
"]实验$\rm 1$,浓硫酸与氯化钠固体反应生成氯化氢气体;实验$\rm 2$,溶液变黄,说明有溴单质生成;②中溶液含有浓硫酸和溴单质,加入碘化钠生成碘单质,可能是浓硫酸把碘离子氧化为碘单质;实验$\rm 1$体现浓硫酸的难挥发性、实验$\rm 2$体现浓硫酸的氧化性。
$\rm A$.实验$\rm 1$,试管口挥发出的氯化氢气体与浓氨水挥发出的氨气反应生成白烟氯化铵,故$\rm A$合理;
$\rm B$.实验$\rm 1$溶液颜色无明显变化说明浓硫酸不能氧化氯离子,实验$\rm 2$溶液变黄说明浓硫酸能氧化溴离子,所以判断还原性:$\rm Br^{-}\gt Cl^{-}$,故$\rm B$合理;
$\rm C$.②中溶液含有浓硫酸和溴单质,加入碘化钠生成碘单质,可能是浓硫酸把碘离子氧化为碘单质,不能得出还原性$\rm I^{-}\gt Br^{-}$的结论,故$\rm C$不合理;
$\rm D$.实验$\rm 1$体现浓硫酸的难挥发性、实验$\rm 2$体现浓硫酸的氧化性,故$\rm D$合理。
故选:$\rm C$
高中 | 氧化性、还原性强弱的比较题目答案及解析(完整版)
