高中 | 氯气 题目答案及解析
稿件来源:高途
高中 | 氯气题目答案及解析如下,仅供参考!
必修一
第四章 非金属及其化合物
第二节 富集在海水中的元素——氯
氯气
冰晶石$\text{N}{{\text{a}}_{3}}\left[ \text{Al}{{\text{F}}_{6}} \right]$是一种白色晶体,微溶于水,是电解铝工业的助熔剂、也是玻璃工业和搪瓷工业的原料。实验室制备冰晶石的装置如图所示。
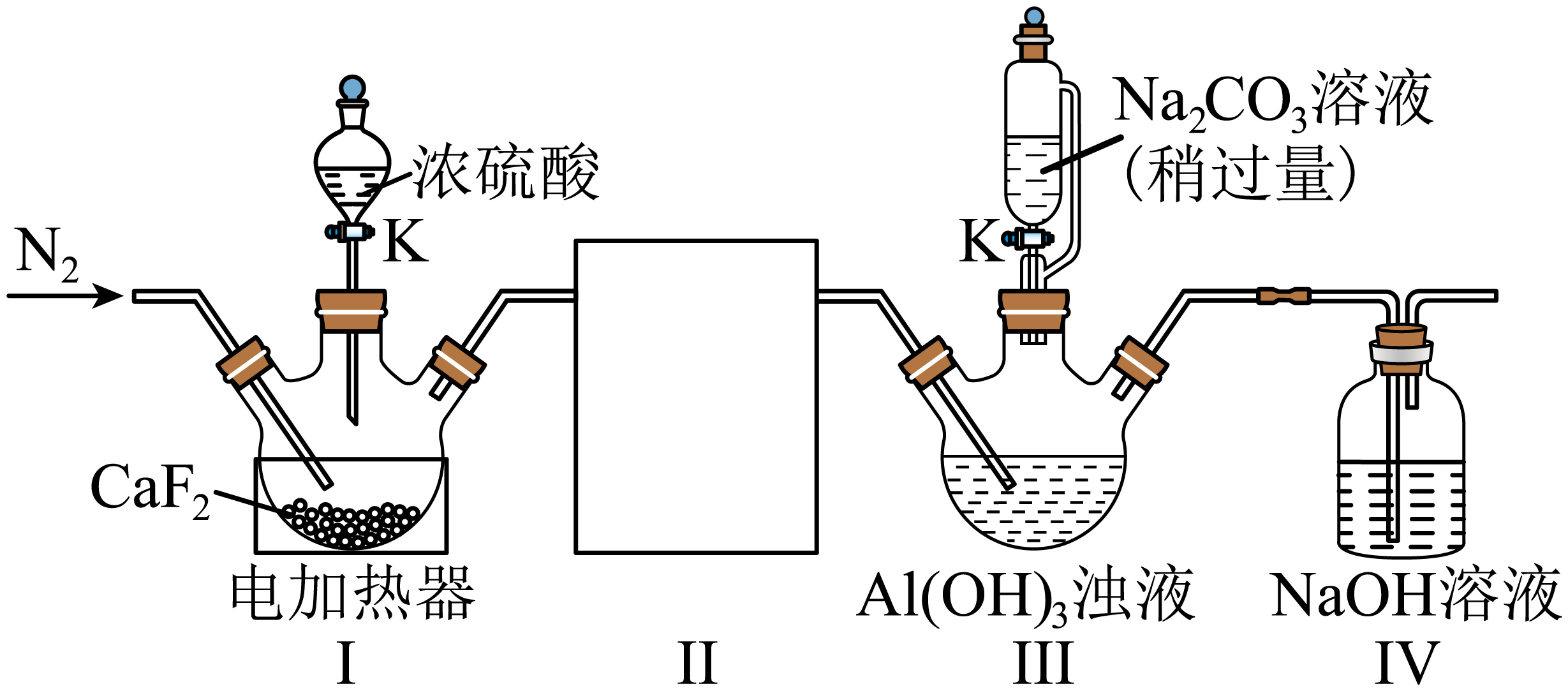
请回答下列问题:
该实验中所使用的仪器材质为 $\rm ($填“普通玻璃”“石英玻璃”或“耐热塑料”$\rm )$。
耐热塑料
"]]该反应需要加热,同时生成$\rm HF$,$\rm HF$会腐蚀玻璃,所以不可用普通玻璃和石英玻璃,应选耐热塑料;
向装置Ⅰ的三颈瓶中加入$7.8\text{ g Ca}{{\text{F}}_{2}}$,再滴入浓硫酸,打开加热装䍜,即可生成$\rm HF$,反应的化学方程式为 。待装置Ⅰ中反应完毕后,需通入一段时间的${{\text{N}}_{2}}$,其目的为 。
${{\\text{H}}_{\\text{2}}}\\text{S}{{\\text{O}}_{\\text{4}}}\\text{(浓}\\text{)+Ca}{{\\text{F}}_{\\text{2}}}\\begin{matrix} \\underline{\\underline{{\\triangle }}} \\\\ {} \\\\\\end{matrix}\\text{CaS}{{\\text{O}}_{\\text{4}}}\\text{+2HF}\\uparrow $ ; 将残留于装置内的$\\rm HF$吹入反应装置中,充分吸收;
"]]$\rm CaF_{2}$和浓硫酸反应生成$\rm HF$和$\rm CaSO_{4}$,反应的化学方程式为${{\text{H}}_{\text{2}}}\text{S}{{\text{O}}_{\text{4}}}\text{(浓}\text{)+Ca}{{\text{F}}_{\text{2}}}\begin{matrix} \underline{\underline{{\triangle }}} \\ {} \\\end{matrix}\text{CaS}{{\text{O}}_{\text{4}}}\text{+2HF}\uparrow $ 。由实验分析可知反应生成$\rm HF$,为了提高$\rm HF$的利用率,需要将残留于制备装置Ⅰ和安全装置内的$\rm HF$赶到制备装置Ⅱ内,充分反应。
装置Ⅲ是生成$\text{N}{{\text{a}}_{3}}\left[ \text{Al}{{\text{F}}_{6}} \right]$的装置,通入$\rm HF$和滴入$\text{N}{{\text{a}}_{2}}\text{C}{{\text{O}}_{3}}$溶液除生成目标产物外,还会生成一种酸式盐 $\rm ($写化学式$\rm )$,$\text{N}{{\text{a}}_{2}}\text{C}{{\text{O}}_{3}}$溶液稍过量的目的是 。
$\\text{NaHC}{{\\text{O}}_{\\text{3}}}$ ; 使$\\rm HF$充分反应
"]]根据实验分析,装置Ⅲ中制备冰晶石,$\text{2N}{{\text{a}}_{\text{2}}}\text{C}{{\text{O}}_{\text{3}}}\text{+Al(OH}{{\text{)}}_{\text{3}}}\text{+6HF}=\text{N}{{\text{a}}_{\text{3}}}\text{Al}{{\text{F}}_{\text{6}}}\text{+NaHC}{{\text{O}}_{\text{3}}}\text{+4}{{\text{H}}_{\text{2}}}\text{O+C}{{\text{O}}_{\text{2}}}\uparrow $;由此可知,除生成外,还生成一种酸式盐为$\text{NaHC}{{\text{O}}_{\text{3}}}$,$\text{N}{{\text{a}}_{\text{2}}}\text{C}{{\text{O}}_{\text{3}}}$溶液稍过量的目的是$\text{N}{{\text{a}}_{\text{2}}}\text{C}{{\text{O}}_{\text{3}}}$溶液显碱性,加入过量$\text{N}{{\text{a}}_{\text{2}}}\text{C}{{\text{O}}_{\text{3}}}$有利于吸收$\rm HF$,提高的利用率。
装置Ⅱ可选取的装置是 $\rm ($填序号$\rm )$。
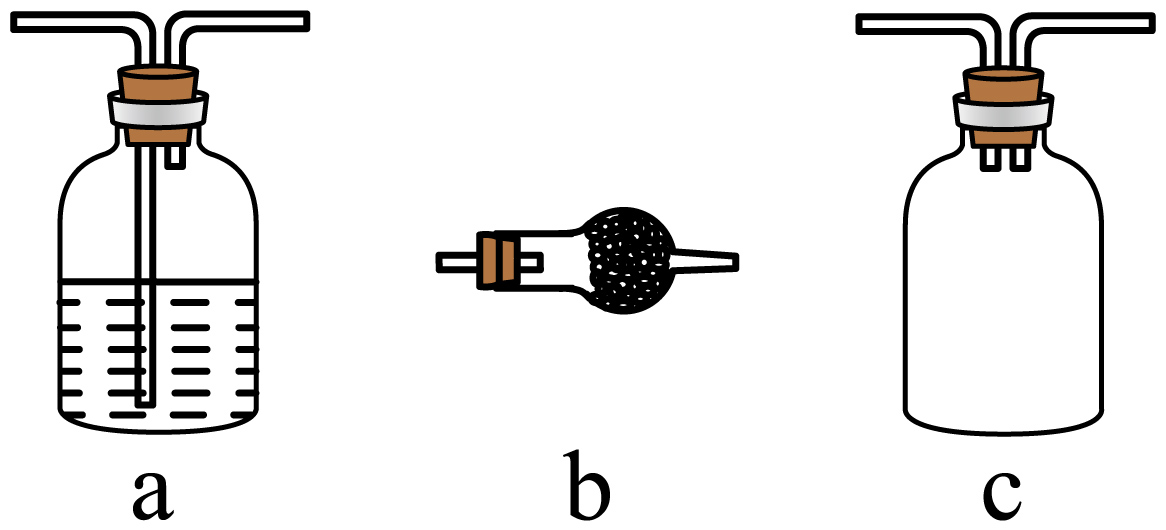
$\\rm c$
"]]装置Ⅱ为防倒吸装置,$\rm a$为洗气装置,$\rm b$为干燥装置,$\rm c$为安全瓶,故选:$\rm c$。
实验结束后,将装置Ⅲ中的沉淀过滤、洗涤、干燥,称量得$\rm 4.9$ $\rm g$产品。该制备实验所得目标产物的产率是 。
$\\rm 70\\%$
"]]设$\rm 7.8$ $\rm g$ $\rm CaF_{2}$参加反应,理论上可制得$\text{N}{{\text{a}}_{\text{3}}}\text{Al}{{\text{F}}_{\text{6}}}$的质量为$x$,由实验分析得关系式:$\begin{matrix} 3\text{Ca}{{\text{F}}_{\text{2}}} & \sim & 6\text{HF} & \sim & \text{N}{{\text{a}}_{\text{3}}}\text{Al}{{\text{F}}_{\text{6}}} \\ 78\times 3 & {} & {} & {} & 210 \\ 7.8\text{ g} & {} & {} & {} & x \\ \end{matrix}$
解得$x=7.0\text{ g}$,故产率$\rm =\dfrac{\text{4}\text{.9 g}}{\text{7}\text{.0 g}}\times 100\%=70\%$。
装置Ⅳ的目的是吸收尾气,该装置中吸收有毒气体的离子方程式为 。
$\\text{HF+O}{{\\text{H}}^{-}}={{\\text{F}}^{-}}+{{\\text{H}}_{\\text{2}}}\\text{O}$
"]]根据分析,装置Ⅳ为尾气处理装置,用$\rm NaOH$溶液可吸收有毒的$\rm HF$气体,生成氟化钠和水,反应的离子方程式为:$\text{HF+O}{{\text{H}}^{-}}={{\text{F}}^{-}}+{{\text{H}}_{\text{2}}}\text{O}$。
高中 | 氯气题目答案及解析(完整版)
