高中 | 铁盐 亚铁盐 题目答案及解析
稿件来源:高途
高中 | 铁盐 亚铁盐题目答案及解析如下,仅供参考!
必修一
第三章 金属及其化合物
第二节 几种重要的金属化合物
铁盐 亚铁盐
工业上利用硫铁矿烧渣$\rm ($主要成分为$\text{F}{{\text{e}}_{3}}{{\text{O}}_{4}}、\text{F}{{\text{e}}_{2}}{{\text{O}}_{3}}、\text{FeO}、\text{Si}{{\text{O}}_{2}}\rm )$为原料制备高档颜料$\rm ——$铁红$\left( \text{F}{{\text{e}}_{2}}{{\text{O}}_{3}} \right)$,具体生产流程如下:
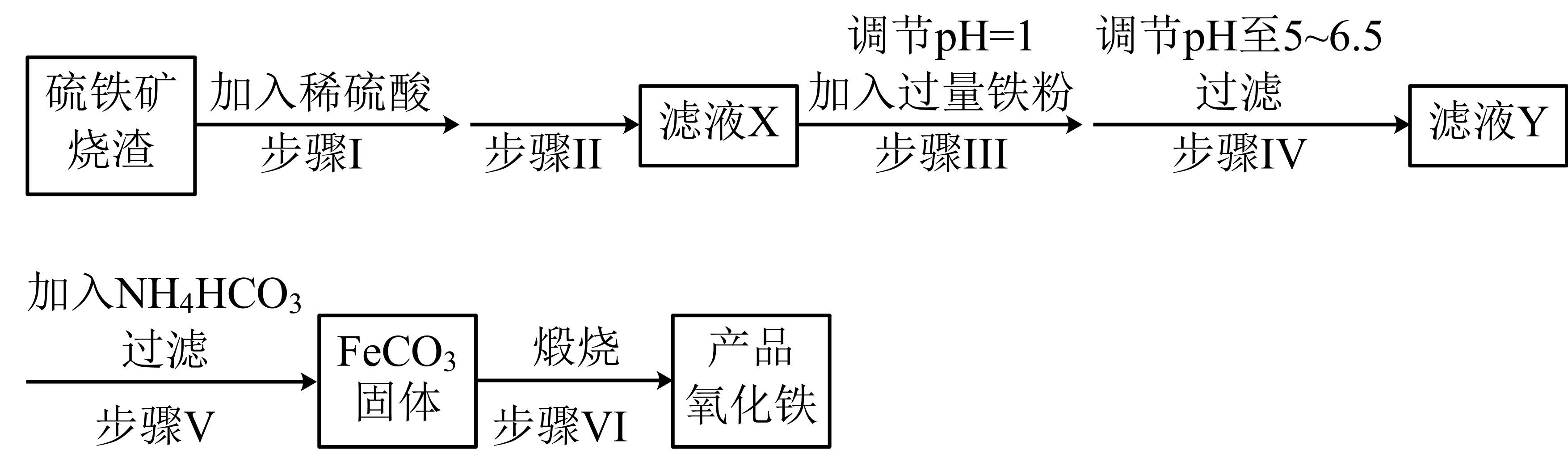
回答下列问题:
为提高酸浸的效率,可采取的措施有 $\rm ($任写一种$\rm )$。
升高温度$\\rm ($或搅拌、粉碎烧渣、适当增大硫酸的浓度$\\rm )$
"]]为提高酸浸的效率,可采取的措施有升高温度$\rm ($或搅拌、粉碎烧渣、适当增大硫酸的浓度$\rm )$;
实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有 、玻璃棒和烧杯等,该步骤是为了除去 $\rm ($填相关物质的化学式$\rm )$。
$\\rm ($普通$\\rm )$漏斗; $\\text{Si}{{\\text{O}}_{\\text{2}}}$
"]]根据分析可知,步骤Ⅱ为过滤,过滤操作所用的玻璃仪器有漏斗、玻璃棒和烧杯等,硫铁矿烧渣(主要成分为$\rm Fe_{3}O_{4}$、$\rm Fe_{2}O_{3}$、$\rm FeO$、$\rm SiO_{2}$),酸溶过程中$\rm Fe_{3}O_{4}$、$\rm Fe_{2}O_{3}$、$\rm FeO$都可以溶解,二氧化硅是酸性氧化物,不和硫酸反应,所以不溶物为$\rm SiO_{2}$,故步骤Ⅱ为过滤,是为了除去不溶的$\rm SiO_{2}$;
检验步骤Ⅲ已经进行完全,可用的试剂是 。
$\\text{KSCN}$溶液$\\rm [$或$\\mathrm{K}_{4} \\mathrm{Fe}(\\mathrm{CN})_{6}$溶液$\\rm ]$
"]]步骤Ⅲ是将铁离子还原成亚铁离子,检验步骤Ⅲ已经进行完全,即溶液中没有铁离子,可以用$\rm KSCN$溶液$\rm [$或$\mathrm{K}_{4} \mathrm{Fe}(\mathrm{CN})_{6}$溶液$\rm ]$;
步骤$\rm V$的反应温度一般需控制在$35$$\ {}^\circ \text{C}$以下,其目的是 ;该步骤中反应生成$\text{FeC}{{\text{O}}_{\text{3}}}$的同时有气泡产生,该反应的离子方程式为 。
防止$\\text{N}{{\\text{H}}_{4}}\\text{HC}{{\\text{O}}_{3}}$分解 ;$2\\text{HCO}_{3}^{-}+\\text{F}{{\\text{e}}^{2+}}=\\text{FeC}{{\\text{O}}_{3}}\\downarrow +\\text{C}{{\\text{O}}_{2}}\\uparrow +{{\\text{H}}_{2}}\\text{O}$
"]]步骤Ⅴ是加入碳酸氢铵产生碳酸亚铁溶液,温度过高碳酸氢铵容易分解,所以温度一般需控制在$\rm 35\;\rm ^\circ\rm C$以下,步骤中反应生成$\text{FeC}{{\text{O}}_{\text{3}}}$的同时有气泡产生,该反应的离子方程式为$2\text{HCO}_{3}^{-}+\text{F}{{\text{e}}^{2+}}=\text{FeC}{{\text{O}}_{3}}\downarrow +\text{C}{{\text{O}}_{2}}\uparrow +{{\text{H}}_{2}}\text{O}$。
高中 | 铁盐 亚铁盐题目答案及解析(完整版)
