高中 | 铝的氧化物 题目答案及解析
稿件来源:高途
高中 | 铝的氧化物题目答案及解析如下,仅供参考!
必修一
第三章 金属及其化合物
第二节 几种重要的金属化合物
铝的氧化物
为研究浓硝酸与$\rm Cu$的反应,进行如图所示实验。下列说法不正确的是$\rm (\qquad)$
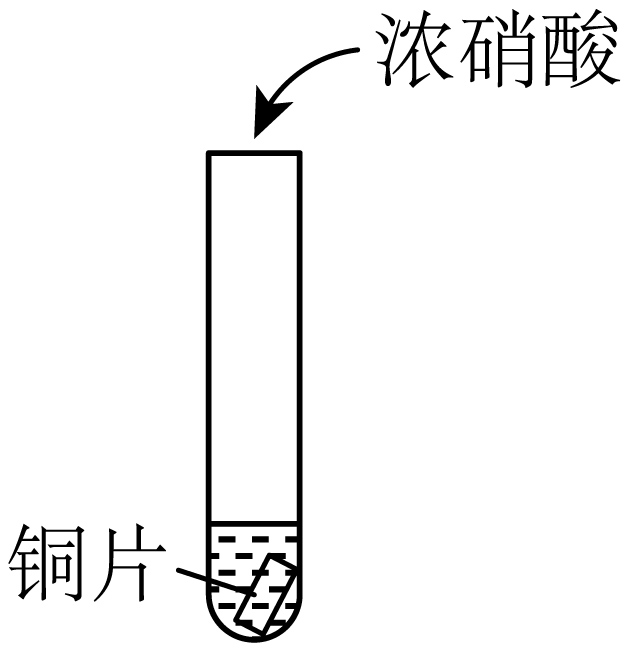
滴入浓硝酸后,无需加热即可反应
","反应开始后,试管中产生红棕色气体,说明浓硝酸具有氧化性
","反应消耗$\\rm 0.05\\ mol$ $\\rm Cu$时,转移电子数约为$\\rm 6.02\\times {{10}^{22}}$
","若将铜片换成铝片,无明显现象,说明还原性:$\\rm Al\\lt Cu$
"]$\rm A$.浓硝酸具有强氧化性,与铜片接触后,无需加热即可发生反应,方程式为:$\rm Cu+4HNO_{3}($浓$\rm )=Cu(NO_{3})_{2}+2NO_{2}↑+2H_{2}O$,$\rm A$ 正确;
$\rm B$.反应开始后,试管中产生红棕色气体$\rm NO_{2}$,$\rm HNO_{3}$中氮元素化合价降低,得到电子,说明浓硝酸具有氧化性,$\rm B$ 正确;
$\rm C$.铜与浓硝酸反应的化学方程式为$\rm Cu+4HNO_{3}($浓$\rm )=Cu(NO_{3})_{2}+2NO_{2}↑+2H_{2}O$,铜元素化合价从$\rm 0$价升高到 $\rm +$ $\rm 2$价,消耗$\rm 1\ mol$铜转移$\rm 2\ mol$电子,当反应消耗$\rm 0.05\ mol\ Cu$时,转移电子数为$\rm 0.05\ mol\times 2\times 6.02\times 10^{23}\ mol^{-1}$ $\rm =$ $\rm 6.02\times 10^{22}$,$\rm C$正确;
$\rm D$.若将铜片换成铝片,无明显现象,是因为常温下铝在浓硝酸中发生钝化,在铝表面生成一层致密的氧化物薄膜,阻止反应进一步进行,而不是因为还原性$\rm Al\lt Cu$,实际上铝的还原性比铜强,$\rm D$ 错误;
故选:D
高中 | 铝的氧化物题目答案及解析(完整版)
