| 杂化轨道理论 题目答案及解析
稿件来源:高途
| 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
在我国青海、西藏等地有许多干涸盐湖盛产含钠盐的$\text{Q}$。$\text{Q}$是一种易溶于水的白色固体,其水溶液用硫酸酸化可得到${{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}\rm [$其分子结构可描述为$\text{B}{{\left( \text{OH} \right)}_{3}}\rm ]$。纯净的${{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$为无色小片状透明晶体。将${{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$与甲醇、浓硫酸混合点燃,可以产生独特的绿色火焰。已知此反应的原理为:在浓硫酸的催化下${{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$与甲醇反应生成硼酸三甲酯$\text{B}{{\left( \text{OC}{{\text{H}}_{3}} \right)}_{3}}$;$\text{B}{{\left( \text{OC}{{\text{H}}_{3}} \right)}_{3}}$发生燃烧,生成的水和$\text{C}{{\text{O}}_{2}}$逸出体系,而生成的${{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$留在反应体系中。结合上述材料和所学知识,判断下列说法正确的是$(\quad\ \ \ \ )$
已知$\\text{Al}{{\\left( \\text{OH} \\right)}_{3}}$溶于浓$\\text{NaOH}$可得到$\\text{Al}\\left( \\text{OH} \\right)_{4}^{-}$和少量$\\text{Al}\\left( \\text{OH} \\right)_{6}^{3-}$,则$\\text{Q}$中很可能含有$\\text{NaB}{{\\left( \\text{OH} \\right)}_{4}}$和少量$\\text{N}{{\\text{a}}_{3}}\\ \\text{B}{{\\left( \\text{OH} \\right)}_{6}}$
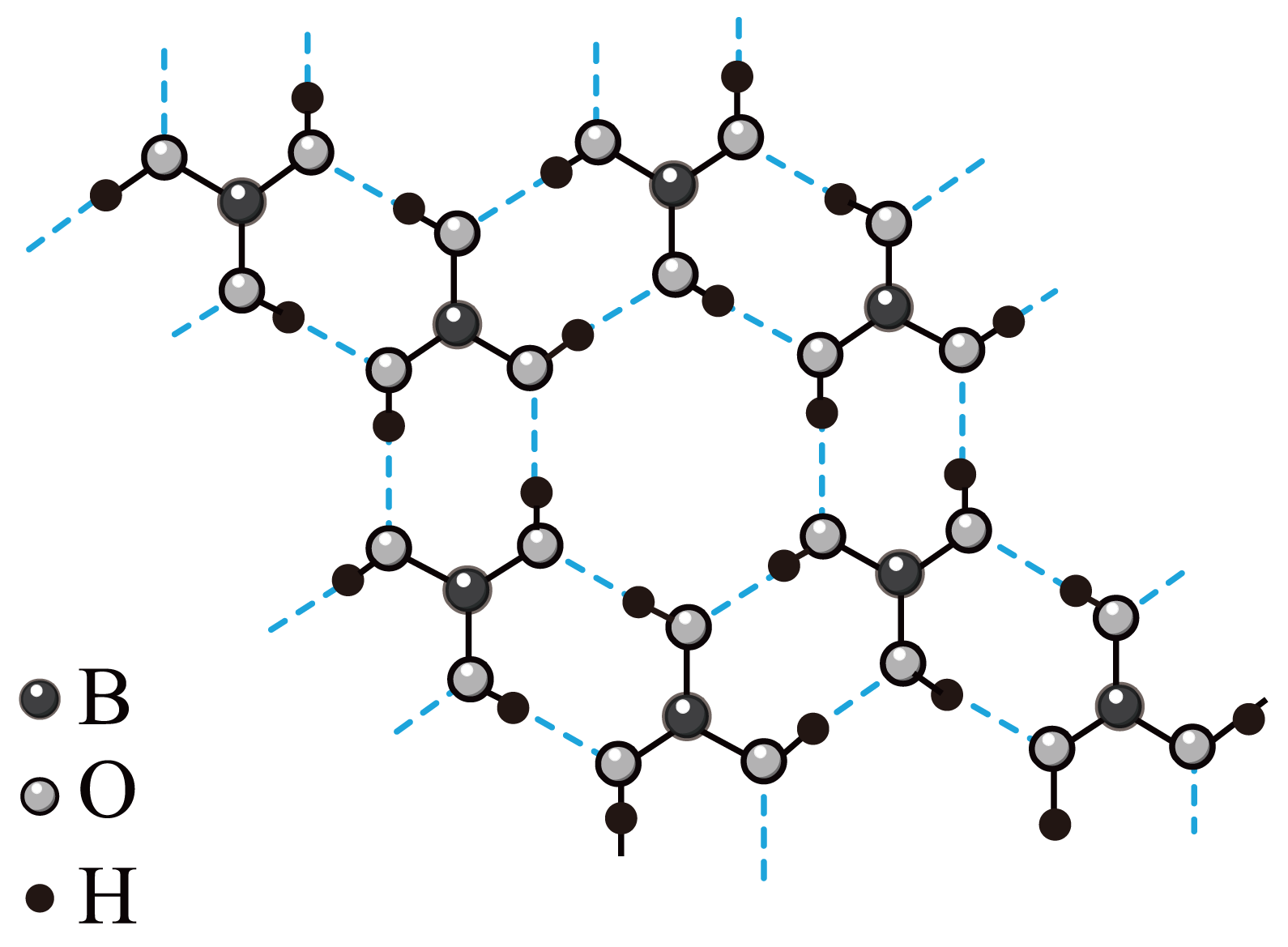
","已知$\\text{B}{{\\left( \\text{OH} \\right)}_{3}}$的最常见晶体中有类似石墨的层状结构,且每层按如图所示的方式通过氢键形成无限网状结构,则其晶体类型为混合晶体
","已知原亚硝酸三甲酯$\\text{N}{{\\left( \\text{OC}{{\\text{H}}_{3}} \\right)}_{3}}$中的$\\text{N}$原子采取$\\text{s}{{\\text{p}}^{3}}$杂化,则硼酸三甲酯中$\\text{B}$亦采取$\\text{s}{{\\text{p}}^{3}}$杂化
","题中所描述的燃烧反应进行一段时间后,火焰逐渐熄灭,如要使反应继续进行,需要添加甲醇并重新点燃
"]$\rm A$.题目通过类比$\rm Al(OH)_{3}$与浓$\rm NaOH$反应生成${{[\text{Al}{{\left( \text{OH} \right)}_{\text{4}}}]}^{-}}$,推测$\rm Q$中可能含有$\rm NaB(OH)_{4}$和少量$\rm Na_{3}B(OH)_{6}$。然而,实际硼酸钠盐的结构复杂,水解后酸化生成$\rm H_{3}BO_{3}$,其结构式可以写成$\rm Na_{2}[B_{4}O_{5}(OH)_{4}]·8H_{2}O$,其中含有$\rm [B_{4}O_{5}(OH)_{4}]^{2-}$的结构,水解原理为:$\rm [B_{4}O_{5}(OH)_{4}]^{2-}+$ $\rm 3H_{2}O+$ $\rm 2H^{+}=4H_{3}BO_{3}$,$\rm A$错误;
$\rm B$.硼酸$\rm ({{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}\rm )$虽具有层状氢键结构,但其晶体类型仍为分子晶体$\rm ($层内氢键,层间分子间作用力$\rm )$,而非石墨的混合晶体$\rm ($层内共价键,层间分子间作用力$\rm )$,$\rm B$错误;
$\rm C$.硼酸三甲酯$\text{B}{{\left( \text{OC}{{\text{H}}_{3}} \right)}_{3}}$中,$\rm B$原子无孤对电子,形成平面三角形结构,为$\text{s}{{\text{p}}^{\text{2}}}$杂化,而原亚硝酸三甲酯$\text{N}{{\left( \text{OC}{{\text{H}}_{3}} \right)}_{3}}$中$\rm N$原子因孤对电子采取$\text{s}{{\text{p}}^{3}}$杂化。两者杂化方式不同,$\rm C$错误;
$\rm D$.燃烧生成的${{\text{H}}_{3}}\text{B}{{\text{O}}_{3}}$可继续与甲醇反应生成硼酸三甲酯,若火焰熄灭,补充甲醇后需重新点燃以启动反应,$\rm D$正确;
故选:$\rm D$
| 杂化轨道理论题目答案及解析(完整版)
