高中 | 铝的氧化物 题目答案及解析
稿件来源:高途
高中 | 铝的氧化物题目答案及解析如下,仅供参考!
必修一
第三章 金属及其化合物
第二节 几种重要的金属化合物
铝的氧化物
部分含硫元素或氮元素物质的类别与相应化合价关系如图所示。
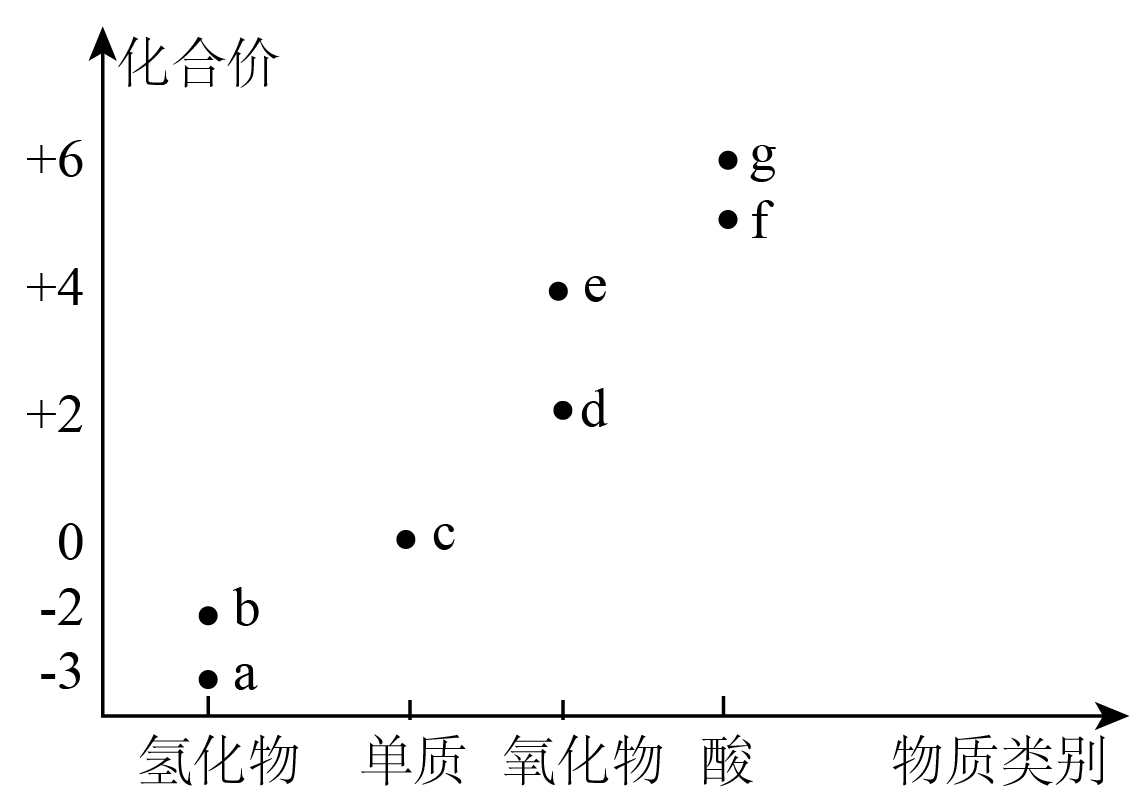
下列描述不合理的是$\rm (\qquad)$
在自然界中存在$\\rm c$,说明该元素非金属性较弱
","一定条件下,$\\rm b$与$\\rm e$可发生反应转化为$\\rm c$
","$\\rm f$、$\\rm g$为常见的强酸,常温下其浓溶液可用铁制容器储运
","$\\rm a$、$\\rm b$分子中中心原子的$\\rm VSEPR$模型相同
"]由图可知,若为氮元素物质的类别,则$\rm a$为$\rm NH_{3}$、$\rm b$为$\rm N_{2}H_{4}$、$\rm c$为$\rm N_{2}$,$\rm d$为$\rm NO$,$\rm e$为$\rm NO_{2}(N_{2}O_{4})$,$\rm f$为$\rm HNO_{3}$;若为硫元素物质的类别,则$\rm b$为$\rm H_{2}S$、$\rm c$为$\rm S$,$\rm e$为$\rm SO_{2}$,$\rm g$为$\rm H_{2}SO_{4}$,据此分析;
$\rm A$.在自然界中存在$\rm S$($\rm N_{2}$),$\rm S$在一定条件下能够氧化金属生成金属硫化物,无法说明该元素非金属性较弱,$\rm A$错误;
$\rm B$.一定条件下$\rm {{\text{N}}_{\text{2}}}{{\text{H}}_{\text{4}}}$与$\rm \text{N}{{\text{O}}_{\text{2}}}$反应$\rm {{\text{N}}_{\text{2}}}$,方程式为$\rm \text{2}\text{N}_{\text{2}}\text{H}_{\text{4}}\text{+2N}\text{O}_{\text{2}}\text{=3}\text{N}_{\text{2}}\text{+4H}_{\text{2}}O$,一定条件下$\rm {{\text{H}}_{\text{2}}}\text{S}$与$\rm \text{S}{{\text{O}}_{\text{2}}}$反应$\rm S$,方程式为$\rm \text{2}{{\text{H}}_{\text{2}}}\text{S+S}{{\text{O}}_{\text{2}}}\text{=3S}\downarrow \text{+2}{{\text{H}}_{\text{2}}}\text{O}$,$\rm B$正确;
$\rm C$.根据分析可知,$\rm HNO_{3}$、$\rm H_{2}SO_{4}$为常见的强酸,常温下其浓溶液可使铁钝化,故可用铁制容器储运,$\rm C$正确;
$\rm D$.$\rm a$为$\rm NH_{3}$中心原子的价层电子对数$\rm 3+\dfrac{5-1\times 3}{2}=4$, $\rm b$为$\rm N_{2}H_{4}$、$\rm H_{2}S$,$\rm N_{2}H_{4}$中心原子的价层电子对数$\rm 3+\dfrac{5-2\times 1\times 1\times 1}{2}=4$,$\rm H_{2}S$中心原子的价层电子对数$\rm 2+\dfrac{6-2\times 1}{2}=4$,$\rm VSEPR$模型均是四面体形,$\rm D$正确。
故选:$\rm A$
高中 | 铝的氧化物题目答案及解析(完整版)
