高中 | 离子方程式 题目答案及解析
稿件来源:高途
高中 | 离子方程式题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第二节 离子反应
离子方程式
我国的蛇纹石资源十分丰富,它的主要成分是$\rm \text{M}{{\text{g}}_{\text{3}}}\text{S}{{\text{i}}_{\text{2}}}{{\text{O}}_{\text{5}}}{{\text{(OH)}}_{\text{4}}}$,伴生有少量$\rm \text{Ni}$、$\rm \text{Fe}$、$\rm \text{Al}$等元素。利用蛇纹石转化与绿矾分解的耦合回收$\rm \text{NiO}$并矿化固定二氧化碳的实验流程如图所示。
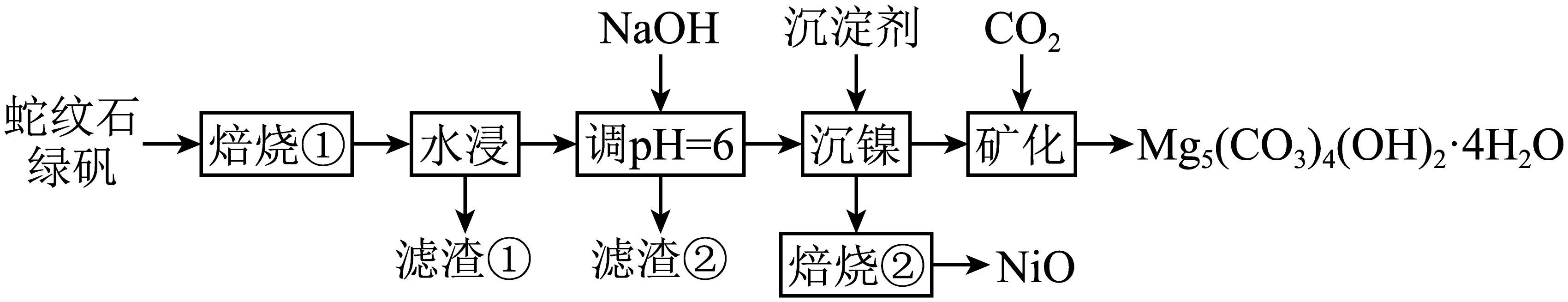
已知:
| $\rm \text{Al(OH}{{\text{)}}_{\text{3}}}$ | $\rm \text{Fe(OH}{{\text{)}}_{\text{3}}}$ | $\rm \text{Mg(OH}{{\text{)}}_{\text{2}}}$ | $\rm \text{Ni(OH}{{\text{)}}_{\text{2}}}$ | |
| $\rm {{\textit{K}}_{\text{sp}}}$ | $\rm \text{1}\text{.3}\times \text{1}{{\text{0}}^{\text{-33}}}$ | $\rm \text{2}\text{.8}\times \text{1}{{\text{0}}^{\text{-39}}}$ | $\rm \text{5}\text{.6}\times \text{1}{{\text{0}}^{\text{-12}}}$ | $\rm \text{5}\text{.5}\times \text{1}{{\text{0}}^{\text{-16}}}$ |
回答下列问题:
绿矾$\rm (\text{FeS}{{\text{O}}_{\text{4}}}\cdot \text{7}{{\text{H}}_{\text{2}}}\text{O}\rm )$在高温下分解,得到红棕色固体和气体产物,反应的化学方程式为 。
$\\rm \\text{2FeS}{{\\text{O}}_{\\text{4}}}\\cdot \\text{7}{{\\text{H}}_{\\text{2}}}\\text{O}\\begin{matrix} \\underline{\\underline{高温}} \\\\ {} \\\\ \\end{matrix}\\text{F}{{\\text{e}}_{\\text{2}}}{{\\text{O}}_{\\text{3}}}\\text{+S}{{\\text{O}}_{\\text{2}}}\\uparrow \\text{+S}{{\\text{O}}_{\\text{3}}}\\uparrow \\text{+14}{{\\text{H}}_{\\text{2}}}\\text{O}\\uparrow $
"]]绿矾$\rm (\text{FeS}{{\text{O}}_{\text{4}}}\cdot \text{7}{{\text{H}}_{\text{2}}}\text{O}\rm )$在高温下分解,得到红棕色固体$\rm \text{F}{{\text{e}}_{2}}{{\text{O}}_{3}}$和气体产物三氧化硫、二氧化硫,反应的化学方程式为$\rm \text{2FeS}{{\text{O}}_{\text{4}}}\cdot \text{7}{{\text{H}}_{\text{2}}}\text{O}\begin{matrix} \underline{\underline{高温}} \\ {} \\ \end{matrix}\text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{\text{3}}}\text{+S}{{\text{O}}_{\text{2}}}\uparrow \text{+S}{{\text{O}}_{\text{3}}}\uparrow \text{+14}{{\text{H}}_{\text{2}}}\text{O}\uparrow $
经“焙烧①”“水浸”,过滤分离后,滤液中金属离子的浓度$\rm (\text{mol}\cdot {{\text{L}}^{\text{-1}}}\rm )$分别为:$\rm \text{N}{{\text{i}}^{\text{2+}}}\text{0}\text{.005}$、$\rm \text{F}{{\text{e}}^{\text{3+}}}\text{0}\text{.150}$、$\rm \text{M}{{\text{g}}^{\text{2+}}}\text{0}\text{.430}$、$\rm \text{A}{{\text{l}}^{\text{3+}}}\text{0}\text{.010}$。滤渣①的主要成分是 、 。
$\\rm \\text{F}{{\\text{e}}_{2}}{{\\text{O}}_{3}};\\text{Si}{{\\text{O}}_{\\text{2}}}$
"]]$\rm \text{M}{{\text{g}}_{\text{3}}}\text{S}{{\text{i}}_{\text{2}}}{{\text{O}}_{\text{5}}}{{\text{(OH)}}_{\text{4}}}$经“焙烧①”,生成氧化镁、二氧化硅、水;$\rm \text{FeS}{{\text{O}}_{\text{4}}}\cdot \text{7}{{\text{H}}_{\text{2}}}\text{O}$分解生成$\rm \text{F}{{\text{e}}_{2}}{{\text{O}}_{3}}$、二氧化硫、三氧化硫, “水浸”,过滤分离后,滤渣①的主要成分是为$\rm \text{F}{{\text{e}}_{2}}{{\text{O}}_{3}}$、$\rm \text{Si}{{\text{O}}_{\text{2}}}$
加入$\rm \text{NaOH}$ “调$\rm \text{pH=6}$”,过滤后,滤渣②是 、 ,滤液中$\rm \text{A}{{\text{l}}^{\text{3+}}}$的浓度为 $\rm \;\rm \text{mol}\cdot {{\text{L}}^{\text{-1}}}$。
$\\rm \\text{Fe(OH}{{\\text{)}}_{\\text{3}}};\\text{Al(OH}{{\\text{)}}_{\\text{3}}};\\text{1}\\text{.3}\\times \\text{1}{{\\text{0}}^{\\text{-9}}}$
"]]加入$\rm \text{NaOH}$ “调$\rm \text{pH=6}$”,$\rm \textit{c}({{\text{H}}^{+}})={{10}^{-6}}\text{mol/L}$,$\rm \textit{c}(\text{O}{{\text{H}}^{-}})={{10}^{-8}}\text{mol/L}$,$\rm \textit{c}(\text{F}{{\text{e}}^{\text{3+}}})=\dfrac{{\textit{K}_{\text{sp}}}[\text{Fe(OH}{{\text{)}}_{\text{3}}}]}{{\textit{c}^{3}}(\text{O}{{\text{H}}^{-}})}=\dfrac{2.8\times {{10}^{-39}}}{{{(1\times {{10}^{-8}})}^{3}}}=2.8\times {{10}^{-15}}\text{mol/L}\lt 1\times {{10}^{-5}}\text{mol/L}$,$\rm \textit{c}(\text{A}{{\text{l}}^{\text{3+}}})=\dfrac{{\textit{K}_{\text{sp}}}[\text{Al(OH}{{\text{)}}_{\text{3}}}]}{{\textit{c}^{3}}(\text{O}{{\text{H}}^{-}})}=\dfrac{1.3\times {{10}^{-33}}}{{{(1\times {{10}^{-8}})}^{3}}}=1.3\times {{10}^{-9}}\text{mol/L}\lt 1\times {{10}^{-5}}\text{mol/L}$,溶液中没有铁离子、氯离子,两者均以氢氧化物沉淀下来,过滤后,滤渣②是为$\rm \text{Fe(OH}{{\text{)}}_{\text{3}}}$、$\rm \text{Al(OH}{{\text{)}}_{\text{3}}}$;滤液中$\rm \text{A}{{\text{l}}^{\text{3+}}}$的浓度为$\rm \textit{c}(\text{A}{{\text{l}}^{\text{3+}}})=\dfrac{{\textit{K}_{\text{sp}}}[\text{Al(OH}{{\text{)}}_{\text{3}}}]}{{\textit{c}^{3}}(\text{O}{{\text{H}}^{-}})}=\dfrac{1.3\times {{10}^{-33}}}{{{(1\times {{10}^{-8}})}^{3}}}=1.3\times {{10}^{-9}}\text{mol/L}$
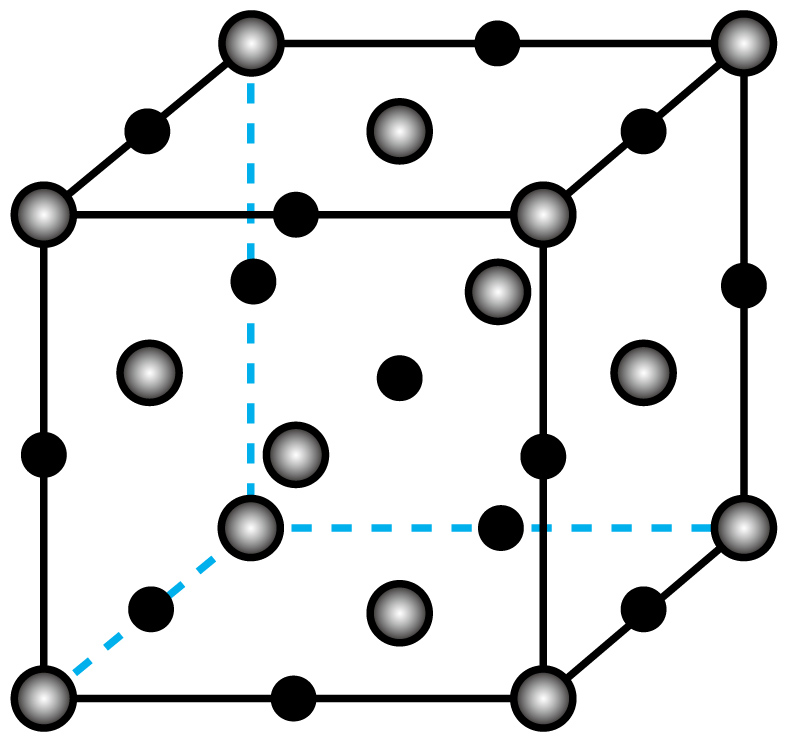
“焙烧②”后得到$\rm \text{NiO}$。$\rm \text{NiO}$晶胞如图所示,晶胞中含有$\rm \text{N}{{\text{i}}^{\text{2+}}}$的个数为 。
$\\rm 4$
"]]因为离子半径$\rm \text{N}{{\text{i}}^{\text{2+}}}\gt {{\text{O}}^{\text{2-}}}$,$\rm \text{NiO}$晶胞图中$\rm \text{N}{{\text{i}}^{\text{2+}}}$位于$\rm 8$个顶点,$\rm 6$个面心,$\rm 1$个晶胞中$\rm \text{N}{{\text{i}}^{\text{2+}}}$的个数为$\rm 8\times \dfrac{1}{8}+6\times \dfrac{1}{2}=4$
调节“沉镍”后的溶液为碱性,“矿化”反应的离子方程式为 。
$\\rm \\text{5M}{{\\text{g}}^{\\text{2+}}}\\text{+10O}{{\\text{H}}^{-}}\\text{+4C}{{\\text{O}}_{\\text{2}}}\\text{=M}{{\\text{g}}_{\\text{5}}}{{\\left( \\text{C}{{\\text{O}}_{\\text{3}}} \\right)}_{\\text{4}}}{{\\text{(OH)}}_{\\text{2}}}\\cdot \\text{4}{{\\text{H}}_{\\text{2}}}\\text{O}\\downarrow $
"]]调节“沉镍”后的溶液为碱性,通入二氧化碳“矿化”发生反应$\rm \text{5M}{{\text{g}}^{\text{2+}}}\text{+10O}{{\text{H}}^{-}}\text{+4C}{{\text{O}}_{\text{2}}}\text{=M}{{\text{g}}_{\text{5}}}{{\left( \text{C}{{\text{O}}_{\text{3}}} \right)}_{\text{4}}}{{\text{(OH)}}_{\text{2}}}\cdot \text{4}{{\text{H}}_{\text{2}}}\text{O}\downarrow $
$\rm \text{1.0\;\rm kg}$蛇纹石“矿化”固定$\rm \text{C}{{\text{O}}_{\text{2}}}$,得到$\rm 0.466\;kg\ {{\text{Mg}}_{\text{5}}}{{\left( \text{C}{{\text{O}}_{\text{3}}} \right)}_{\text{4}}}{{\text{(OH)}}_{\text{2}}}\cdot \text{4}{{\text{H}}_{\text{2}}}\text{O}$,相当于固定$\rm \text{C}{{\text{O}}_{\text{2}}}$ $\rm \;\rm L($标准状况$\rm )$。
$\\rm 89.6$
"]]$\rm\text{0.466\;\rm kg M}{{\text{g}}_{\text{5}}}{{\left( \text{C}{{\text{O}}_{\text{3}}} \right)}_{\text{4}}}{{\text{(OH)}}_{\text{2}}}\cdot \text{4}{{\text{H}}_{\text{2}}}\text{O}$物质的量为$\rm \dfrac{\text{0}\text{.466}\times \text{1}{{\text{0}}^{\text{3}}}\;\text{g}}{\text{466\;\rm g/mol}}=1\;\rm \text{mol}$,根据$\rm C$原子守恒$\rm \text{M}{{\text{g}}_{\text{5}}}{{\left( \text{C}{{\text{O}}_{\text{3}}} \right)}_{\text{4}}}{{\text{(OH)}}_{\text{2}}}\cdot \text{4}{{\text{H}}_{\text{2}}}\text{O}\sim \text{4C}\sim \text{4C}{{\text{O}}_{2}}$,固定$\rm \text{C}{{\text{O}}_{\text{2}}}$为$\rm 4\;\rm \text{mol}$,标准状况下的体积为$\rm 4\;\rm \text{mol}\times 22.4\;L/mol=89.6\;\rm L$
高中 | 离子方程式题目答案及解析(完整版)
