高中 | 盐类水解在生活中的应用 题目答案及解析
稿件来源:高途
高中 | 盐类水解在生活中的应用题目答案及解析如下,仅供参考!
选修四
第三章 水溶液中的离子平衡
第三节 盐类的水解
盐类水解在生活中的应用
短周期主族元素形成的二元化合物甲能发生如图所示反应,图示中参与反应的$\rm H_{2}O$未标出,下列说法不正确的是$(\qquad)$
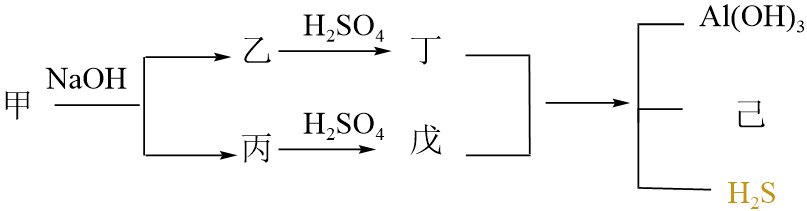
化合物甲溶于水会发生水解反应,生成刺激性气味气体
","反应中$\\rm H_{2}SO_{4}$都不宜过量
","丁物质的水溶液长时间加热蒸干再灼烧,最后产物还是自身
","丙物质和$\\rm H_{2}S$都可以在工业上用作沉淀剂,促使$\\rm Cu^{2+}$、$\\rm Fe^{2+}$、$\\rm Ba^{2+}$、$\\rm Ag^{+}$等生成相应沉淀
"]根据流程图,丁和戊反应生成氢氧化铝和$\rm H_{2}S$,则甲中含有$\rm Al$、$\rm S$元素,甲是$\rm Al_{2}S_{3}$,$\rm Al_{2}S_{3}$和氢氧化钠溶液反应生成$\text{Na}\left[ \text{Al}{{\left( \text{OH} \right)}_{\text{4}}} \right]$、$\text{N}{{\text{a}}_{\text{2}}}\text{S}$ ,乙是$\text{Na}\left[ \text{Al}{{\left( \text{OH} \right)}_{\text{4}}} \right]$、丙为$\rm Na_{2}S$,$\text{Na}\left[ \text{Al}{{\left( \text{OH} \right)}_{\text{4}}} \right]$与足量硫酸反应生成$\rm Al_{2}(SO_{4})_{3}$,丁是$\rm Al_{2}(SO_{4})_{3}$;$\text{N}{{\text{a}}_{\text{2}}}\text{S}$和适量硫酸反应生成$\rm NaHS$,戊是$\rm NaHS$;$\rm Al_{2}(SO_{4})_{3}$、$\rm NaHS$发生双水解反应生成氢氧化铝、$\rm H_{2}S$、硫酸钠。
$\rm A$.$\rm Al_{2}S_{3}$溶于水会发生水解反应生成氢氧化铝沉淀和$\rm H_{2}S$气体,故$\rm A$正确;
$\rm B$.$\text{Na}\left[ \text{Al}{{\left( \text{OH} \right)}_{\text{4}}} \right]$与过量硫酸反应后丁中含有硫酸,与$\rm NaHS$反应不能生成氢氧化铝沉淀;$\rm Na_2S$与过量硫酸反应生成硫酸钠和$\rm H_{2}S$气体,所以硫酸都不宜过量,故$\rm B$正确;
$\rm C$.硫酸难挥发,$\rm Al_{2}(SO_{4})_{3}$的水溶液长时间加热蒸干再灼烧,最后产物还是$\rm Al_{2}(SO_{4})_{3}$,故$\rm C$正确;
$\rm D$.$\text{N}{{\text{a}}_{\text{2}}}\text{S}$和$\rm H_{2}S$都可以在工业上用作沉淀剂,促使$\rm Cu^{2+}$、$\rm Fe^{2+}$、$\rm Ag^{+}$等生成相应硫化物沉淀,$\rm BaS$可溶于水,不能使$\rm Ba^{2+}$沉淀,故$\rm D$错误。
故选:$\rm D$
高中 | 盐类水解在生活中的应用题目答案及解析(完整版)
