高中 | 盐类水解在生活中的应用 题目答案及解析
稿件来源:高途
高中 | 盐类水解在生活中的应用题目答案及解析如下,仅供参考!
选修四
第三章 水溶液中的离子平衡
第三节 盐类的水解
盐类水解在生活中的应用
利用下列装置$\rm ($夹持装置略$\rm )$进行实验,能达到实验目的的是$\rm (\qquad)$
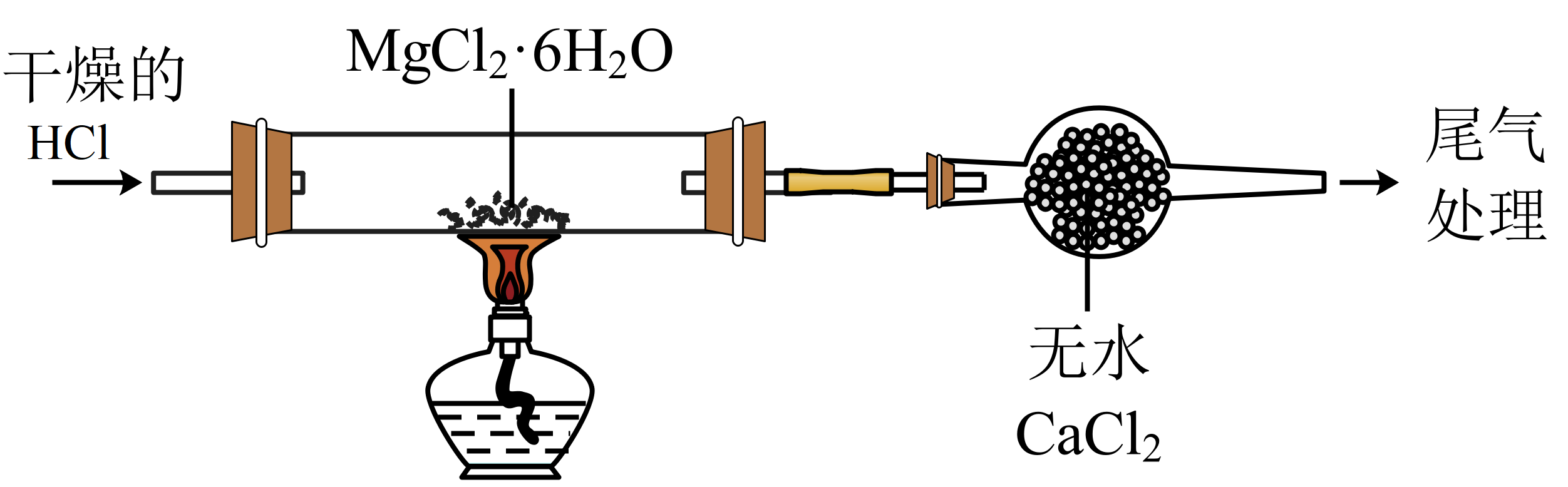
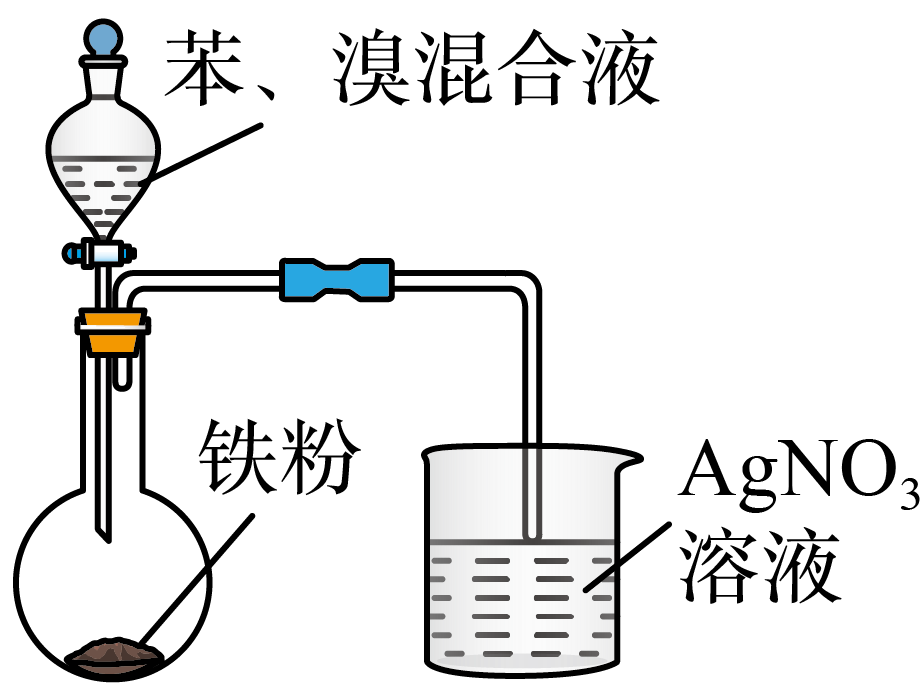
| $\rm A$.制备无水$\rm MgC{{l}_{2}}$ | $\rm B$.制备溴苯并验证有$\rm HBr$产生 |
 |  |
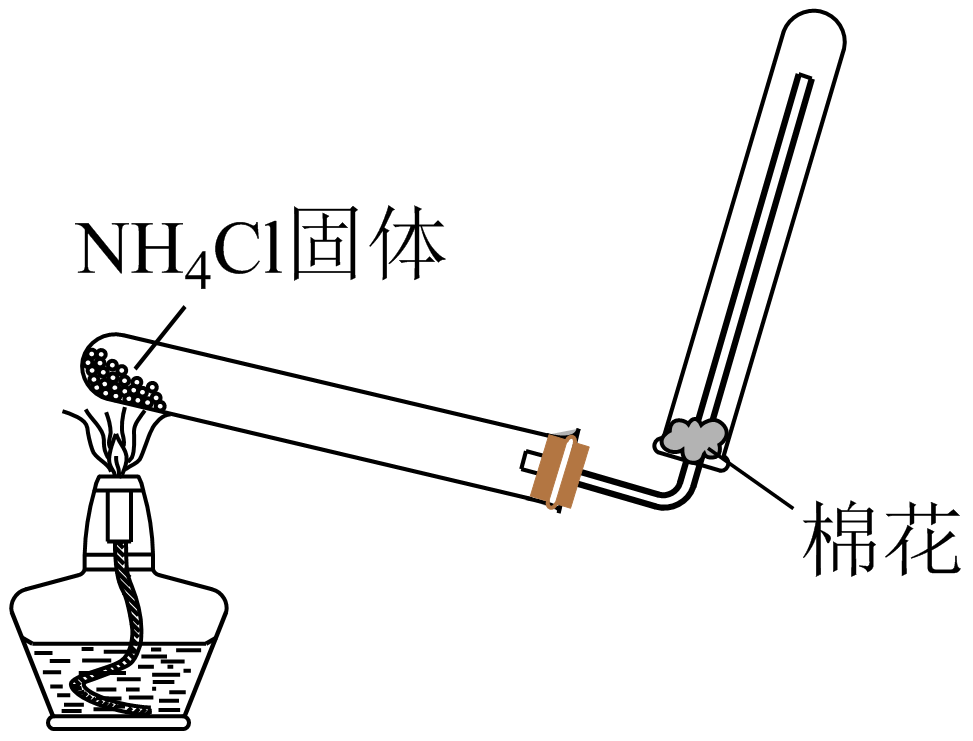
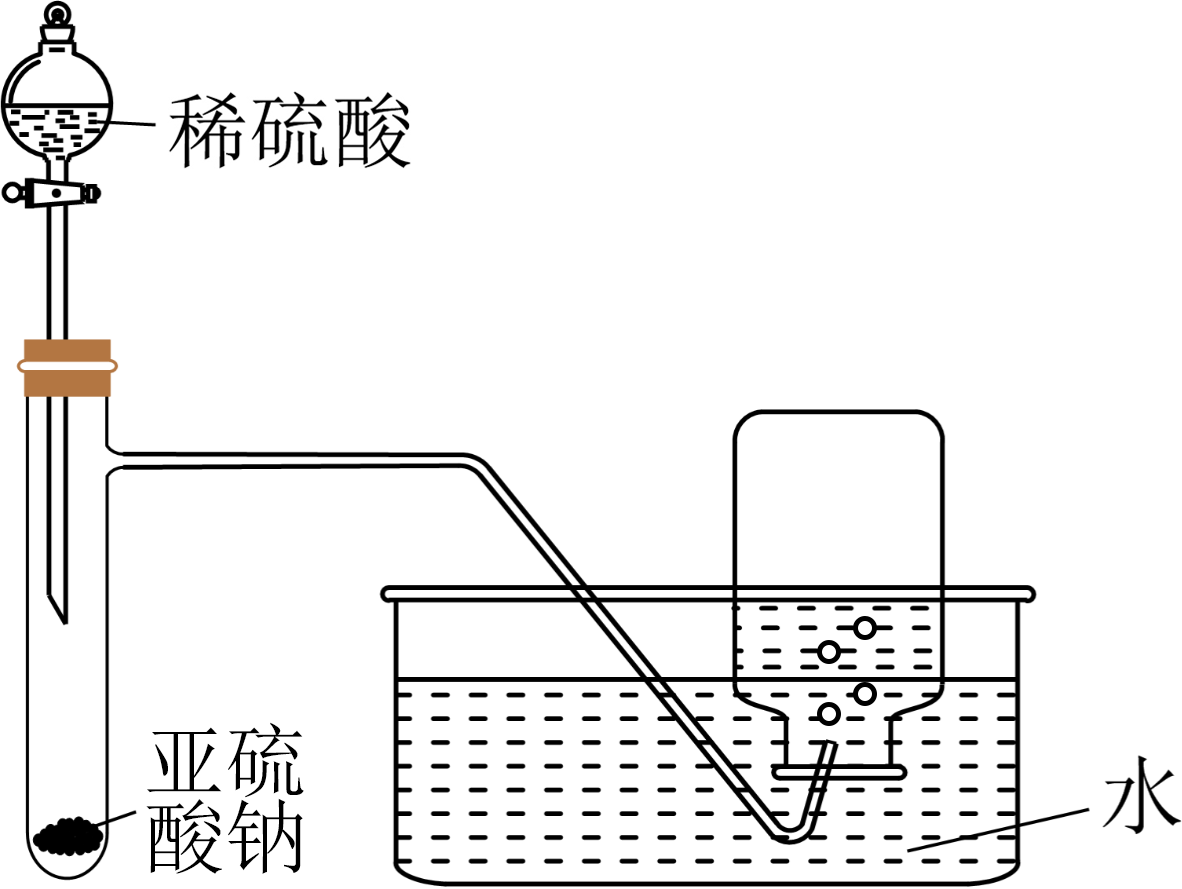
| $\rm C$.制备并收集氨气 | $\rm D$.制备并收集$\rm SO_{2}$ |
 |  |
$\\rm A$
","$\\rm B$
","$\\rm C$
","$\\rm D$
"]$\rm A$.制备无水$\rm MgC{{l}_{2}}$时,由于$\rm MgC{{l}_{2}}\cdot 6{{H}_{2}}O$加热时易水解生成$\rm Mg(OH)Cl$或$\rm MgO$,通入干燥$\rm HCl$可抑制$\rm M{{g}^{2+}}$水解$\rm (HCl$气氛中平衡$\rm MgC{{l}_{2}}+2{{H}_{2}}O\rightleftharpoons Mg{{(OH)}_{2}}+2HCl$逆向移动$\rm )$,装置中通入干燥$\rm HCl$并加热,能得到无水$\rm MgC{{l}_{2}}$,$\rm A$正确。
$\rm B$.制备溴苯并验证$\rm HBr$时,苯与液溴在催化剂作用下剧烈反应,由于$\rm B{{r}_{2}}$易挥发,生成的$\rm HBr$中含有挥发的$\rm B{{r}_{2}}$蒸汽,装置中未除杂$\rm B{{r}_{2}}$,$\rm B{{r}_{2}}$进入$\rm AgN{{O}_{3}}$溶液会与水反应生成$\rm HBr$,也能与$\rm AgN{{O}_{3}}$反应生成$\rm AgBr$沉淀,无法区分沉淀是否来自反应生成的$\rm HBr$,$\rm B$错误。
$\rm C$.制备并收集氨气时,$\rm N{{H}_{4}}Cl$固体加热分解生成$\rm N{{H}_{3}}$和$\rm HCl$,二者在试管口遇冷又化合为$\rm N{{H}_{4}}Cl$,无法制得$\rm N{{H}_{3}}$,应使用$\rm N{{H}_{4}}Cl$与$\rm Ca{{(OH)}_{2}}$混合加热制备,$\rm C$错误。
$\rm D$.制备并收集$\rm S{{O}_{2}}$时,稀硫酸与亚硫酸钠反应生成的$\rm S{{O}_{2}}$易溶于水$\rm (1:40)$,难以逸出;且$\rm S{{O}_{2}}$易溶于水,不能用排水法收集,应使用浓硫酸制备并采用向上排空气法收集,$\rm D$错误。
故选:$\rm A$
高中 | 盐类水解在生活中的应用题目答案及解析(完整版)
