高中 | 杂化轨道理论 题目答案及解析
稿件来源:高途
高中 | 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
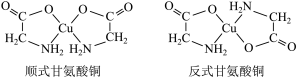
甘氨酸铜是一种优质的有机铜源,其化学结构稳定,对环境污染也比无机铜低。甘氨酸铜有顺式和反式两种同分异构体,结构如下图。下列说法正确的是$\rm (\quad\ \ \ \ )$
["
铜原子的杂化类型为$\\rm \\text{s}{{\\text{p}}^{3}}$杂化
","$\\rm O→Cu$的配位键键能小于$\\rm N→Cu$的配位键键能
","顺式甘氨酸铜溶解度小于反式甘氨酸铜
","甘氨酸铜晶体中相邻微粒通过范德华力相连,堆积成超分子
"][["B"]]
$\rm A$.甘氨酸铜有顺式和反式两种同分异构体,则甘氨酸铜中$\rm Cu$、与铜形成$\rm \sigma$键的$\rm 2$个$\rm O$、$\rm 2$个$\rm N$处于同一平面,则铜原子的杂化类型为$\rm dsp^{2}$杂化,故$\rm A$错误;
$\rm B$.由于$\rm O$的电负性大于$\rm N$,所以$\rm N$原子更易形成配位键,$\rm O→Cu$的配位键键能小于$\rm N→Cu$的配位键键能,故$\rm B$正确;
$\rm C$.由结构简式可知,顺式甘氨酸铜是极性分子,反式甘氨酸铜是非极性分子,根据“相似相溶”原理可知顺式甘氨酸铜在水中的溶解度更大,故$\rm C$错误;
$\rm D$.从结构可看出,顺式甘氨酸铜相邻微粒间还有氢键相连,故$\rm D$错误;
故选:$\rm B$
高中 | 杂化轨道理论题目答案及解析(完整版)
去刷题
相关题库:
钙钛矿太阳能电池是一种具有广阔应用前景的新型光伏技术。科研人员通过甲基吡咯烷酮 和二苯基亚砜 协同作用,成功制备了大面积高质量钙钛矿薄膜。
已知氨和硼烷可以发生加合反应生成氨硼烷,它和乙烷具有相似的结构。下列有关这种分子的说法正确的是
如图所示的铼配合物离子能电催化还原。短周期元素的原子序数依次增大。标准状况下,和是等密度的无色气体,是黄绿色气体。下列说法错误的是
是一种重要的有机溶剂,其工业制备原理为:,下列说法正确的是
乙二胺四乙酸铁钠可用于感光材料冲洗药品及漂白剂,化学式为;工业上可用与、溶液发生反应进行制备,合成路线如下:
硼的化合物有重要应用。
今日推荐 ![]()
![]()
![]()
