高中 | 萃取与分液 题目答案及解析
稿件来源:高途
高中 | 萃取与分液题目答案及解析如下,仅供参考!
必修一
第一章 从实验学化学
第一节 化学实验基本方法
萃取与分液
己二酸$\rm ($![]() ,其相对分子质量为$\rm 146)$是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。
,其相对分子质量为$\rm 146)$是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。
$\rm I$.催化剂钨磷酸晶体$\rm ({{H}_{3}}P{{W}_{12}}{{O}_{40}})$的制备实验流程如图:
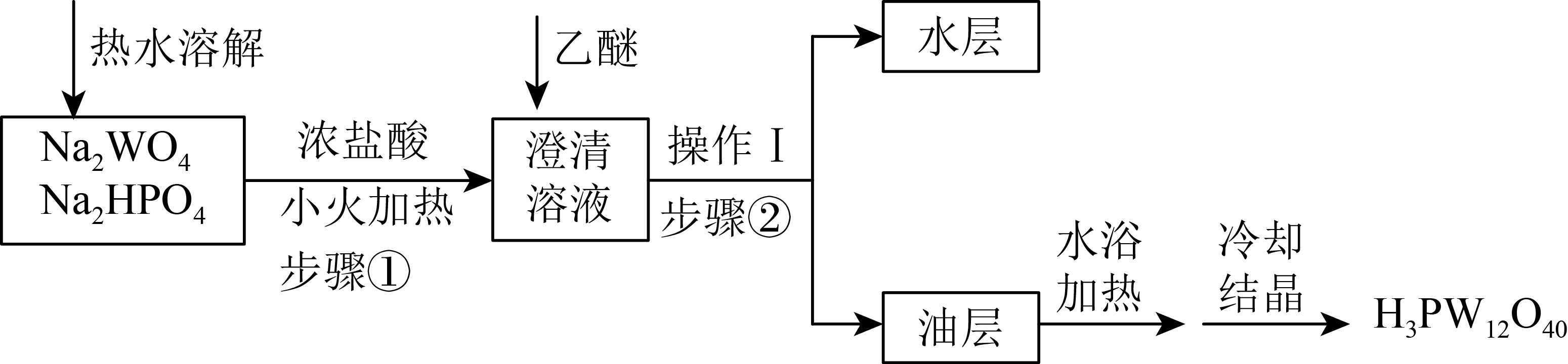
操作$\rm I$所需的玻璃仪器除烧杯外还有 。
分液漏斗
"]]由题意,加入乙醚后进行分液操作,分出水层和油层,因此乙醚作用为萃取钨磷酸;操作$\rm I$为分液操作,所需的玻璃仪器除烧杯外还需要分液漏斗。
水层中的物质有大量$\rm NaCl$和少量$\rm HCl$,步骤①中发生反应的化学方程式为 。
$\\rm 12N{{a}_{2}}W{{O}_{4}}+N{{a}_{2}}HP{{O}_{4}}+26HCl\\begin{matrix} \\underline{\\underline{\\triangle}} \\\\ {} \\\\ \\end{matrix}{{H}_{3}}P{{W}_{12}}{{O}_{40}}+26NaCl+12{{H}_{2}}O$
"]]从流程图中及产物可知,参加反应的物质有$\rm Na_{2}WO_{4}$、$\rm Na_{2}HPO_{4}$、$\rm HCl$,产物中有$\rm H_{3}PW_{12}O_{40}$可得化学方程式为$\rm 12N{{a}_{2}}W{{O}_{4}}+N{{a}_{2}}HP{{O}_{4}}+26HCl\begin{matrix} \underline{\underline{\triangle}} \\ {} \\ \end{matrix}{{H}_{3}}P{{W}_{12}}{{O}_{40}}+26NaCl+12{{H}_{2}}O$。
Ⅱ.己二酸的合成
向三颈烧瓶中加入$\rm 0{}10\ g$钨磷酸催化剂和$\rm 30\ mL\ 30 \%$双氧水,在室温下搅拌$\rm 5\ min$,然后加入$\rm 5{}0\ mL$试剂$\rm X$,得到溶液$\rm A$。
环己烯、环己醇、环己酮均可被双氧水氧化成己二酸。仅从所需双氧水理论用量的角度看,试剂$\rm X$的最佳选择是 $($填序号$\rm )$。
$\rm A$.环己烯$\rm ($![]() $\rm )$
$\rm )$
$\rm B$.环己醇$\rm ($![]() $)$
$)$
$\rm C$.环己酮$\rm ($![]() $\rm )$
$\rm )$
$\\rm C$
"]]由于存在如下关系式:$\rm 1\ mol$环己烯$\rm \sim 4\ mol$双氧水$\rm \sim 1\ mol$己二酸,$\rm 1\ mol$环己醇$\rm \sim 4\ mol$双氧水$\rm \sim 1\ mol$己二酸,$\rm 1\ mol$环己酮$\rm \sim 3\ mol$双氧水$\rm \sim 1\ mol$己二酸,因此,生产等物质的量的己二酸时环己酮消耗的双氧水最少,因此最佳选择为$\rm C$。
如图是己二酸的浓度与温度关系曲线图。介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸溶液处于 。实验室常根据图中直线$\rm EHI$从溶液$\rm A$获取己二酸晶体,对应的实验操作为: 过滤、洗涤、干燥。
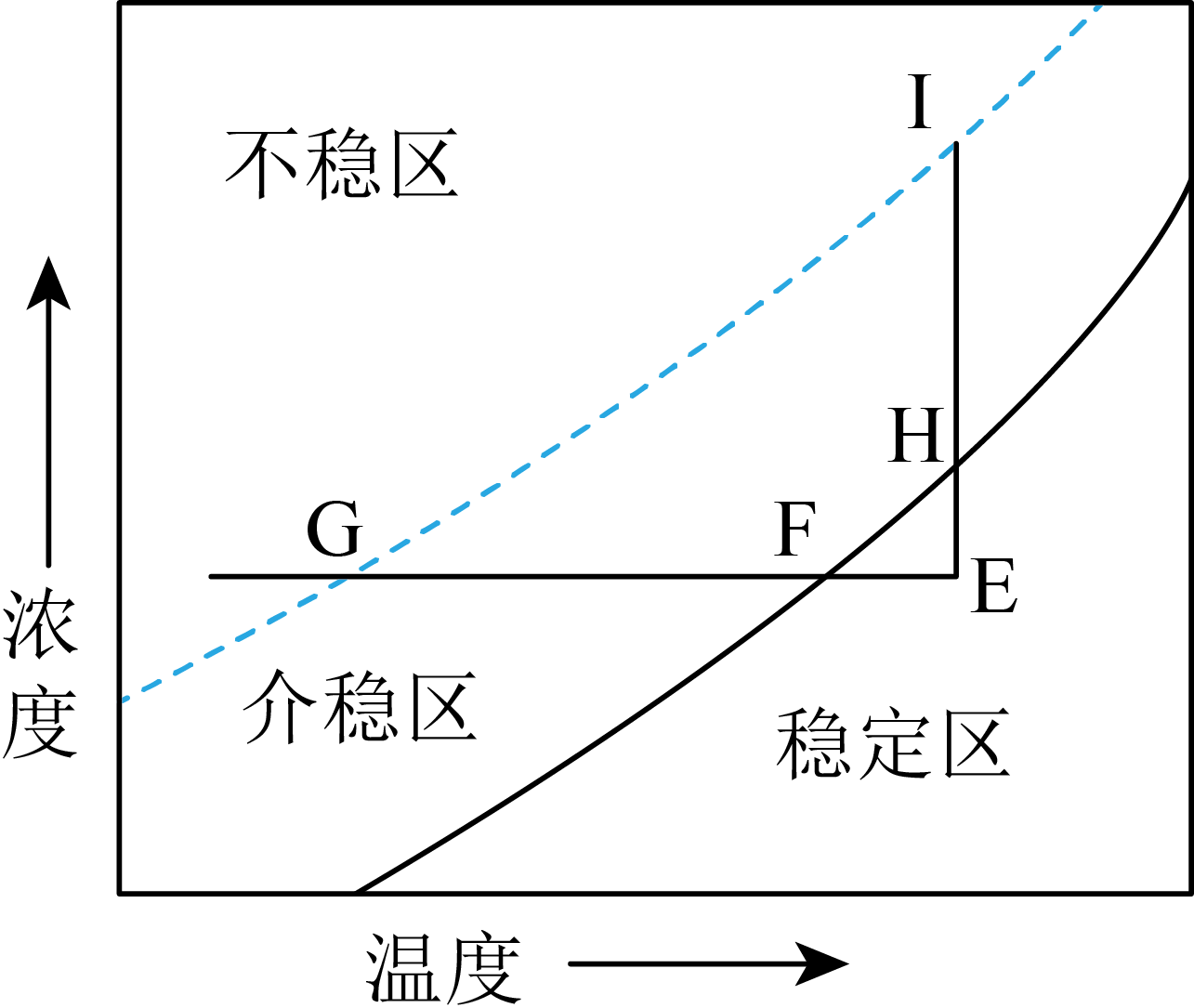
不饱和状态;恒温蒸发结晶
"]]介稳区表示己二酸溶液处于饱和状态,稳定区应表示己二酸溶液处于不饱和状态,己二酸溶液稳定存在,不会有晶体析出;实验室常根据直线$\rm EHI$从溶液$\rm A$获取己二酸晶体,对应的实验操作为恒温蒸发结晶,过滤。
$\rm II$$\rm I$.己二酸的纯度测定
将$\rm 0{}5000\ g$己二酸样品配制成$\rm 100\ mL$溶液,每次取$\rm 20{}00\ mL$试样溶液于锥形瓶中,滴入几滴酚酞试液,用$\rm 0{}1000\ mol/L\ NaOH$溶液滴定至终点,平均消耗$\rm NaOH$溶液$\rm 10{}00\ mL($己二酸被完全中和$\rm )$。
①下列说法错误的是 $\rm ($填字母$\rm )$。
$\rm A$.用$\rm 100\ mL$容量瓶配制成溶液后,最好用$\rm 25\ mL$规格的量筒量取待测液于锥形瓶中
$\rm B$.滴定时,未用待测液润洗锥形瓶,则测定结果偏低
$\rm C$.接近滴定终点时,应控制活塞,改为滴加半滴标准液,直至溶液由无色变为浅红色,且半分钟内不变色
$\rm D$.若滴定前滴定管尖嘴部分无气泡,滴定后产生气泡,则测定结果偏高
②己二酸的纯度为 $\rm \%$。
$\\rm ABD$;$\\rm 73$
"]]①$\rm A$.用酸式滴定管取$\rm 20{}00\ mL$试样己二酸溶液于锥形瓶中,故$\rm A$错误。
$\rm B$.滴定时,锥形瓶不需要润洗,未用待测液润洗锥形瓶,不影响实验结果,故$\rm B$错误。
$\rm C$.接近滴定终点时,应控制活塞,改为滴加半滴标准液,直至溶液由无色变为浅红色,且半分钟内不变色,滴定终点达到,故$\rm C$正确。
$\rm D$.若滴定前滴定管尖嘴部分无气泡,滴定后产生气泡,使得标准液体积读数偏小,则测定溶液浓度偏低,故$\rm D$错误。
②根据关系式:$\rm 己二酸\sim 2NaOH$,则己二酸纯度为$\rm \dfrac{0.1000\ mol/L\times 10.00\times 1{{0}^{-3}}\ L\times \dfrac{1}{2}\times \dfrac{100\ mL}{20.00\ mL}\times 146\ g/mol}{0.5000\ g}\times 100\%=73\%$。
若要得到纯度更高的己二酸,可通过 的方法提纯。
重结晶
"]]要得到纯度更高的己二酸,可通过重结晶的方法提纯。
高中 | 萃取与分液题目答案及解析(完整版)
