高中 | 氧化还原反应的计算 题目答案及解析
稿件来源:高途
高中 | 氧化还原反应的计算题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应的计算
漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为$\text{Ca}{{\left( \text{Cl}{{\text{O}}_{2}} \right)}_{2}}$,相应的生产流程如图。
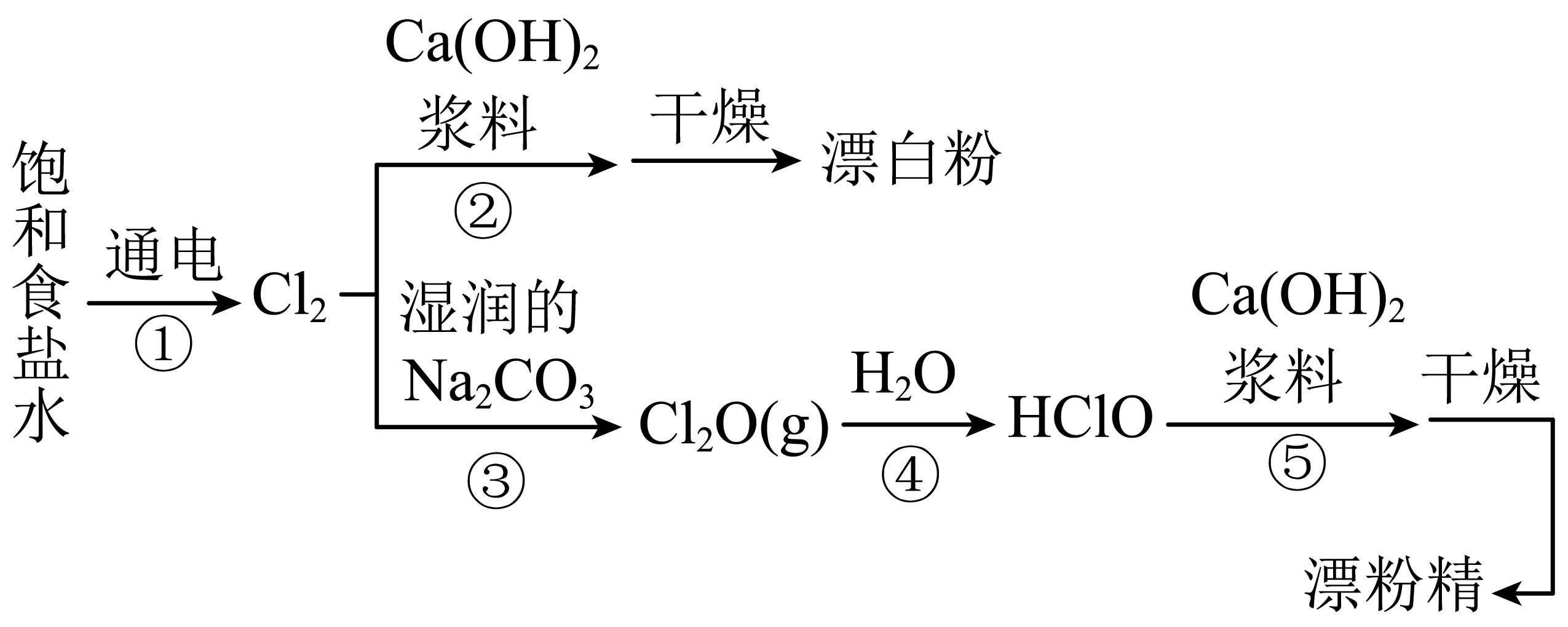
下列说法不正确的是$(\qquad)$
②中反应的离子方程式为$\\text{C}{{\\text{l}}_{2}}+\\text{Ca}{{\\left( \\text{OH} \\right)}_{2}}=\\text{C}{{\\text{a}}^{2+}}+\\text{Cl}{{\\text{O}}^{-}}+\\text{C}{{\\text{l}}^{-}}+{{\\text{H}}_{2}}\\text{O}$
","在清洁卫生间时,可将洁厕灵$\\rm ($主要成分为盐酸$\\rm )$与漂白粉溶液混合使用以增强去污效果
","在上述②制备过程中消耗$\\rm 1\\;\\rm mol\\;\\rm Cl_{2}$,转移电子$\\rm 1\\;\\rm mol$
","漂白粉与漂粉精的区别是漂粉精中次氯酸钙的质量百分数更大
"]反应①是电解饱和食盐水生成氢氧化钠、氢气、氯气;反应②是氯气和石灰乳反应生成氯化钙、次氯酸钙、水;反应③是氯气和碳酸钠反应生成一氧化二氯、氯化钠、二氧化碳;反应④是一氧化二氯和水反应生成次氯酸;反应⑤是氢氧化钙和次氯酸反应生成次氯酸钙和水。
$\rm A$.反应②是氯气和石灰乳反应生成氯化钙、次氯酸钙、水,反应为$\text{C}{{\text{l}}_{\text{2}}}\text{+Ca}{{\left( \text{OH} \right)}_{\text{2}}}\text{=C}{{\text{a}}^{\text{2+}}}\text{+C}{{\text{l}}^{-}}\text{+Cl}{{\text{O}}^{-}}+{{\text{H}}_{\text{2}}}\text{O}$,$\rm A$正确;
$\rm B$.在清洁卫生间时,洁厕灵$\rm ($主要成分为盐酸$\rm )$与漂白粉溶液中次氯酸根离子反应生成有毒的氯气,$\rm B$错误;
$\rm C$.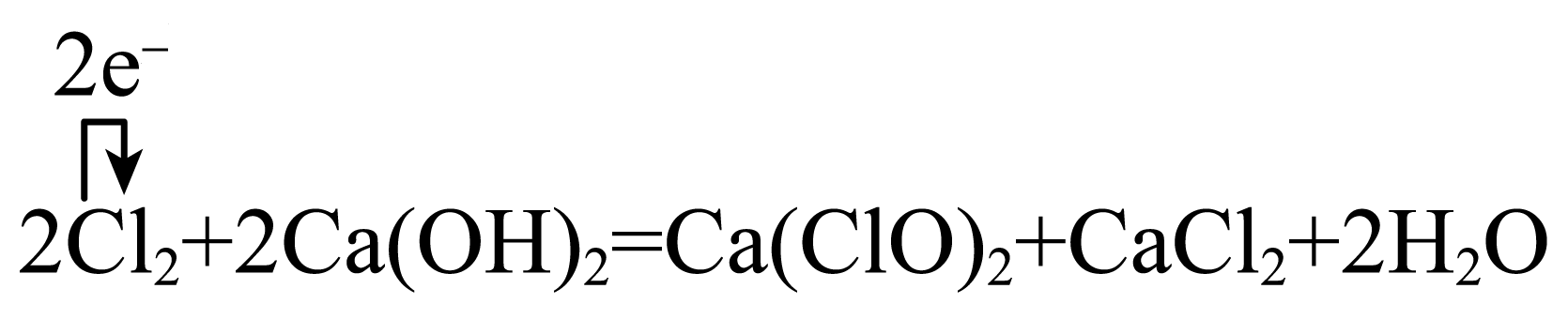 ,则②制备过程中消耗$\rm 1\;\rm mol\;\rm Cl_{2}$,转移电子$\rm 1\;\rm mol$,$\rm C$正确;
,则②制备过程中消耗$\rm 1\;\rm mol\;\rm Cl_{2}$,转移电子$\rm 1\;\rm mol$,$\rm C$正确;
$\rm D$.由流程可知,漂白粉中含有氯化钙和次氯酸钙,漂白精中含次氯酸钙不含氯化钙,故漂白粉与漂粉精的区别是漂粉精中次氯酸钙的质量百分数更大,$\rm D$正确;
故选:$\rm B$
高中 | 氧化还原反应的计算题目答案及解析(完整版)
