高中 | 化学键 题目答案及解析
稿件来源:高途
高中 | 化学键题目答案及解析如下,仅供参考!
必修二
第一章 物质结构 元素周期律
第三节 化学键
化学键
$\text{C}{{\text{O}}_{2}}$与$\text{NO}_{3}^{-}$通过电催化反应生成$\text{CO}{{\left( \text{N}{{\text{H}}_{2}} \right)}_{2}}$,可能的反应机理如图所示$\rm ($图中吸附在催化剂表面的物种用“*”标注$\rm )$。下列说法正确的是$(\quad\ \ \ \ )$
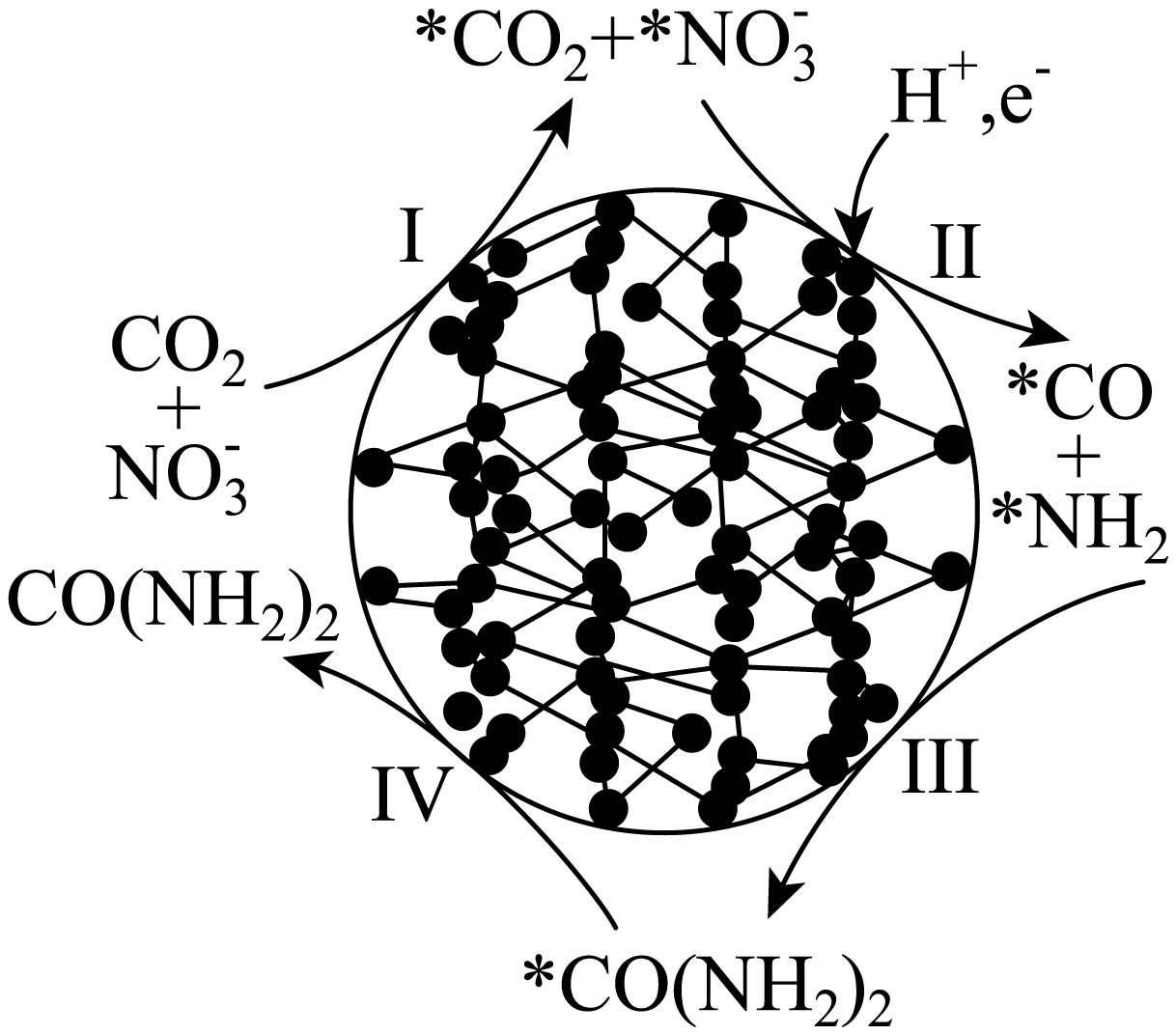
过程Ⅱ和过程Ⅲ都有极性共价键形成
","过程Ⅱ中$\\text{NO}_{3}^{-}$发生了氧化反应
","电催化$\\text{C}{{\\text{O}}_{2}}$与$\\text{NO}_{3}^{-}$生成$\\text{CO}{{\\left( \\text{N}{{\\text{H}}_{2}} \\right)}_{2}}$的反应方程式:$\\text{C}{{\\text{O}}_{2}}+2\\text{NO}_{3}^{-}+18{{\\text{H}}^{+}}\\begin{matrix} \\underline{\\underline{通电}} \\\\催化剂 \\\\\\end{matrix}\\text{CO}{{\\left( \\text{N}{{\\text{H}}_{2}} \\right)}_{2}}+7{{\\text{H}}_{2}}\\text{O}$
","常温常压、无催化剂条件下,$\\text{C}{{\\text{O}}_{2}}$与$\\text{N}{{\\text{H}}_{3}}\\cdot {{\\text{H}}_{2}}\\text{O}$反应可生产$\\text{CO}{{\\left( \\text{N}{{\\text{H}}_{2}} \\right)}_{2}}$
"]$\rm A$.过程Ⅱ为:$\text{*C}{{\text{O}}_{2}}$和$\text{*NO}_{3}^{-}$在酸性条件下被还原为$\text{*CO}$和$\text{*N}{{\text{H}}_{2}}$的反应,生成了$\rm N-H$等极性共价键;过程Ⅲ为$\text{*CO}$与$\text{*N}{{\text{H}}_{2}}$生成$\text{*CO}{{\left( \text{N}{{\text{H}}_{2}} \right)}_{2}}$的反应,生成了$\rm C-N$极性共价键,$\rm A$正确;
$\rm B$.过程Ⅱ是得电子的还原反应,$\rm N$元素的化合价由$+5$降为$-2$,$\rm C$元素的化合价由$+4$降为$+2$,$\rm B$错误;
$\rm C$.所给离子方程式电荷不守恒,根据反应机理图可知,过程Ⅱ需要外界提供电子,则正确的反应方程式为$\text{C}{{\text{O}}_{2}}+2\text{NO}_{3}^{-}+18{{\text{H}}^{+}}+16{{\text{e}}^{-}}\begin{matrix} \underline{\underline{通电}} \\催化剂 \\\end{matrix}\text{CO}{{(\text{N}{{\text{H}}_{2}})}_{2}}+7{{\text{H}}_{2}}\text{O}$,$\rm C$错误;
$\rm D$.常温常压、无催化剂条件下,$\text{C}{{\text{O}}_{2}}$与$\text{N}{{\text{H}}_{3}}\cdot {{\text{H}}_{2}}\text{O}$反应生成${{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{C}{{\text{O}}_{3}}$或$\text{N}{{\text{H}}_{4}}\text{HC}{{\text{O}}_{3}}$,$\rm D$错误;
故选:$\rm A$
高中 | 化学键题目答案及解析(完整版)
