| 杂化轨道理论 题目答案及解析
稿件来源:高途
| 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
以铂钯精矿$\rm ($含$\rm Se$、$\rm Te$、$\rm Au$、$\rm Pt$、$\rm Pd$等$\rm )$为原料,提取贵金属$\rm Au$、$\rm Pt$、$\rm Pd$的工艺流程如图所示;
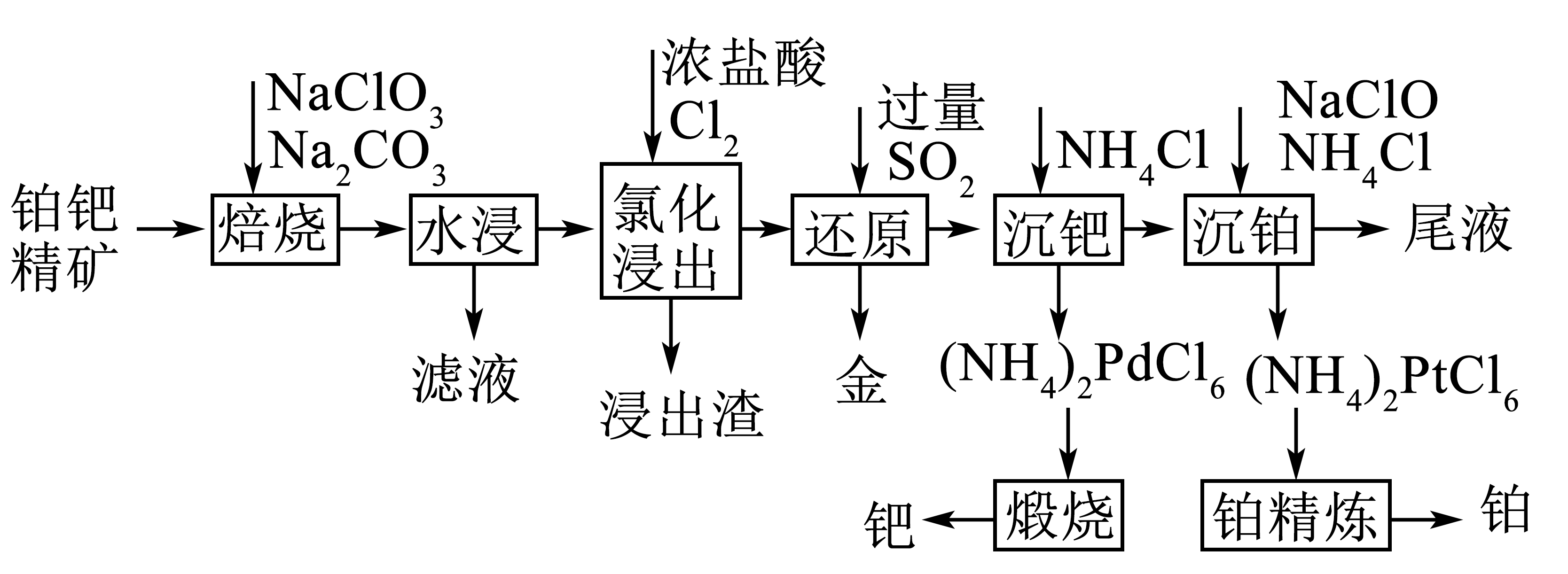
已知;
①“氯化浸出”时,$\text{Au}$、$\text{Pt}$、$\text{Pd}$以$\text{HAuC}{{\text{l}}_{4}}$、${{\text{H}}_{2}}\text{PtC}{{\text{l}}_{6}}$、${{\text{H}}_{2}}\text{PdC}{{\text{l}}_{6}}$形式存在;
②${{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PtC}{{\text{l}}_{6}}$和${{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PdC}{{\text{l}}_{6}}$难溶于水,${{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PtC}{{\text{l}}_{4}}$易溶于水,${{K}_{\text{sp}}}\left[ {{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PdC}{{\text{l}}_{6}} \right]=9.9\times {{10}^{-8}}$,$\sqrt{99}\approx 9.95$;
③离子浓度$\le 1\times {{10}^{-5}}\;\rm \text{mol}\cdot {{\text{L}}^{-1}}$时,认为该离子已沉淀完全。
“水浸”时,需要把焙烧渣粉碎后再加入水,同时在溶液底部鼓入${{\text{N}}_{2}}$,鼓入${{\text{N}}_{2}}$的目的是 。
搅拌,使固体和液体充分接触,加快反应速率,提高浸取率
"]]“水浸”时,需要把焙烧渣粉碎后再加入水,同时在溶液底部鼓入${{\text{N}}_{2}}$,鼓入${{\text{N}}_{2}}$的目的是充分搅拌,使固体和液体充分接触,加快反应速率,提高浸取率。
“焙烧”时,$\text{Se},\text{Te}$单质转化为可溶于水的$\mathrm{Na}_{2} \mathrm{SeO}_{3}$和$\text{N}{{\text{a}}_{2}}\text{Te}{{\text{O}}_{4}}$。消耗等物质的量的$\text{NaCl}{{\text{O}}_{3}}$,转化的$\text{Se},\text{Te}$的物质的量之比 ;根据以下两图判断“焙烧”适宜的条件为 。
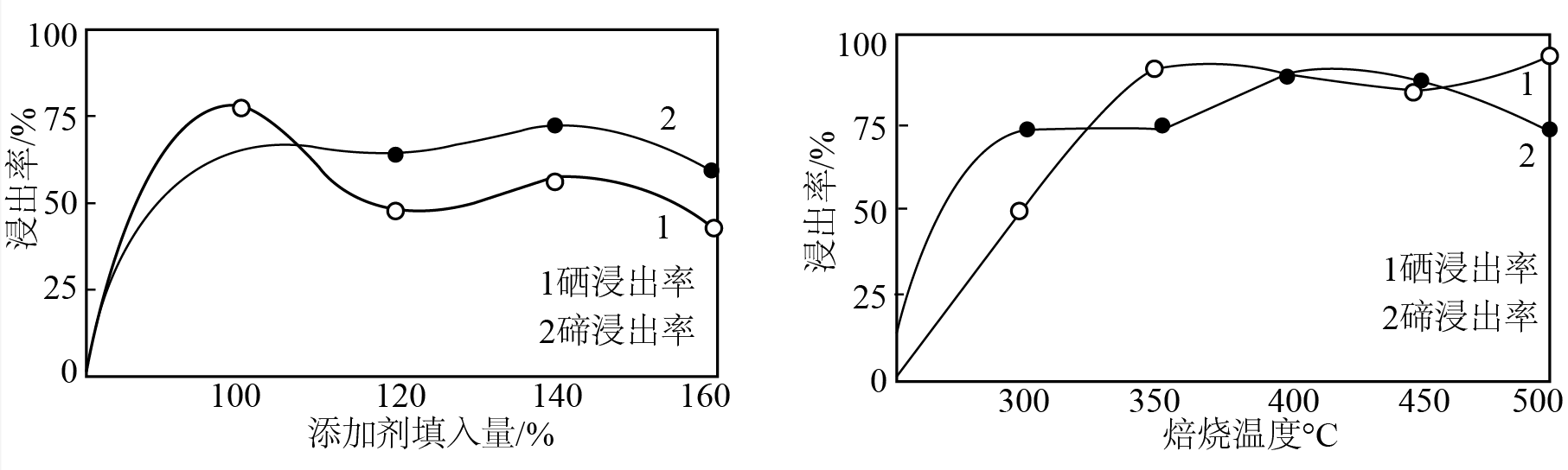
$\\rm 3:2$ ; 添加剂加入量为$\\rm 100\\%$,$\\rm 400$~$\\rm 450\\;\\rm ^\\circ\\rm C$
"]]“焙烧”时,$\text{Se},\text{Te}$单质转化为可溶于水的$\mathrm{Na}_{2} \mathrm{SeO}_{3}$和$\text{N}{{\text{a}}_{2}}\text{Te}{{\text{O}}_{4}}$,$\rm Se$元素化合价由$\rm 0$升高为$\rm +4$、$\rm Te$元素化合价由$\rm 0$升高为$\rm +6$,根据得失电子守恒,消耗等物质的量的$\text{NaCl}{{\text{O}}_{3}}$,转化的$\text{Se},\text{Te}$的物质的量之比$\rm 3:2$;根据图示,添加剂填入量为$\rm 100\%$时,浸出率最高;焙烧温度$\rm 400$~$\rm 450\;\rm ^\circ\rm C$浸出率最高,“焙烧”适宜的条件为添加剂加入量为$\rm 100\%$,$\rm 400$~$\rm 450\;\rm ^\circ\rm C$。
“还原”得到金的反应的化学方程式为 ;加入过量$\text{S}{{\text{O}}_{2}}$除将$\text{HAuC}{{\text{l}}_{4}}$彻底还原得到金外,其另一目的是 。
$\\rm 2HAuCl_{4}+3SO_{2}+6H_{2}O=2Au+3H_{2}SO_{4}+8HCl$ ; 将$\\rm H_{2}PtCl_{6}$还原为$\\rm H_{2}PtCl_{4}$
"]]二氧化硫将把$\text{HAuC}{{\text{l}}_{4}}$还原为金,“还原”得到金的反应的化学方程式为$\rm 2HAuCl_{4}+3SO_{2}+6H_{2}O=2Au+3H_{2}SO_{4}+8HCl$; ${{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PtC}{{\text{l}}_{6}}$难溶于水,${{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PtC}{{\text{l}}_{4}}$易溶于水,为防止“沉钯”时生成${{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PtC}{{\text{l}}_{6}}$沉淀,“沉钯”前需把${{\text{H}}_{2}}\text{PtC}{{\text{l}}_{6}}$还原为${{\text{H}}_{2}}\text{PtC}{{\text{l}}_{4}}$,加入过量$\text{S}{{\text{O}}_{2}}$的目的是将$\rm H_{2}PtCl_{6}$还原为$\rm H_{2}PtCl_{4}$。
常温下,“沉钯”时,若使$2\,\text{L}\,c\left( \text{PdCl}_{6}^{2-} \right)=0.2\,\text{mol}/\text{L}$的溶液中$\text{PdCl}_{6}^{2-}$沉淀完全,需至少加入$\text{N}{{\text{H}}_{4}}\text{Cl}$固体的物质的量为 $\rm ($结果保留$\rm 3$位有效数字$\rm )$。
$\\rm 0.999$ $\\rm mol$
"]]常温下,${{K}_{\text{sp}}}\left[ {{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{PdC}{{\text{l}}_{6}} \right]=9.9\times {{10}^{-8}}$,$\text{PdCl}_{6}^{2-}$沉淀完全时, $c\left( \text{NH}_{4}^{+} \right)=\sqrt{\dfrac{9.9\times {{10}^{-8}}}{1\times {{10}^{-5}}}}=0.0995\,\text{mol/L}$,“沉钯”时,若使$c\left( \text{PdCl}_{6}^{2-} \right)=0.2\,\text{mol}/\text{L}$的溶液中$\text{PdCl}_{6}^{2-}$沉淀完全,需至少加入$\text{N}{{\text{H}}_{4}}\text{Cl}$固体的物质的量为$0.2\,\text{mol/L}\times 2\,\text{L}\times \text{2}+\text{0}\text{.0995}\,\text{mol/L}\times 2\,\text{L}=\text{0}\text{.999}\,\text{mol}$。
“煅烧”时除生成${{\text{N}}_{2}}$、$\text{N}{{\text{H}}_{4}}\text{Cl}$外,还生成一种气体,该气体用少量水吸收后可重复用于“ ”操作单元。
氯化浸出
"]]“煅烧”时$\rm (NH_{3})_{2}PdCl_{6}$分解生成$\rm Pd$、${{\text{N}}_{2}}$、$\text{N}{{\text{H}}_{4}}\text{Cl}$外,根据元素守恒,还生成氯化氢气体,该气体用少量水吸收后可重复用于“氯化浸出”操作单元。
配合物顺铂是临床使用的第一代铂类抗癌药物,其为平面四边形结构$\rm ($如图所示$\rm )$,下列关于顺铂的说法正确的是 。
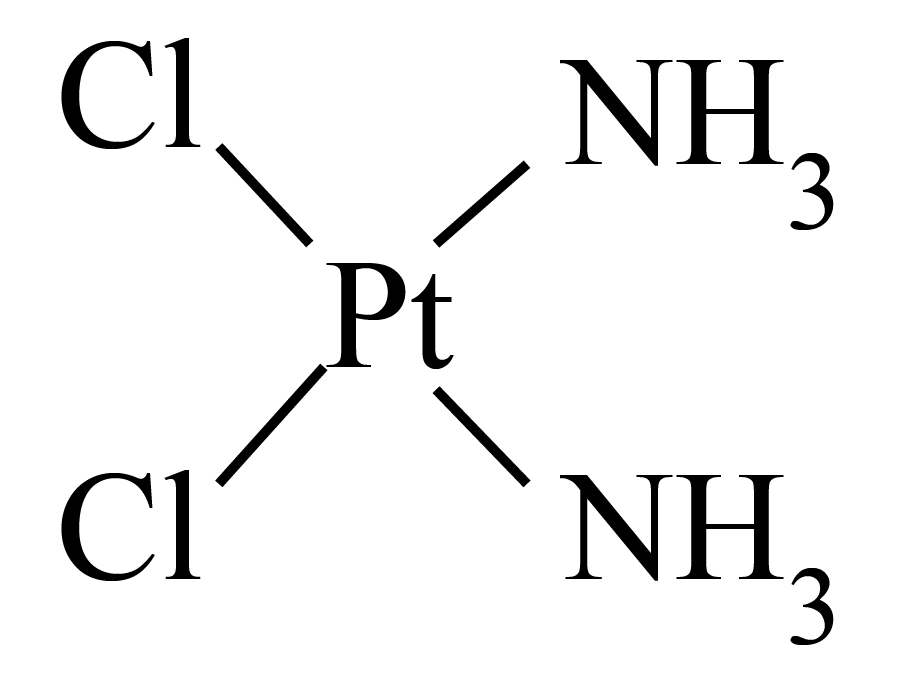
$\rm A$.$\rm Pt$的化合价为$\rm 0$价 $\rm B$.配位原子为$\rm Cl$和$\rm N$
$\rm C$.配位数为$\rm 4$ $\rm D$.$\rm Pt$采取的是$\rm \text{s}{{\text{p}}^{3}}$杂化
$\\rm BC$
"]]$\rm A$. 根据元素化合价代数和等于$\rm 0$,$\rm Pt$的化合价为$\rm +2$价,故$\rm A$错误;
$\rm B$. 根据图示,$\rm Pt$与$\rm Cl$和$\rm N$形成配位键,配位原子为$\rm Cl$和$\rm N$,故$\rm B$正确;
$\rm C$. 根据图示,$\rm Pt$与$\rm Cl$和$\rm N$形成$\rm 4$个配位键,配位数为$\rm 4$,故$\rm C$正确;
$\rm D$.顺铂是平面四边形结构,$\rm Pt$采取的是$\rm dsp^{2}$杂化,故$\rm D$错误;
| 杂化轨道理论题目答案及解析(完整版)
