| 金属矿物的开发及利用 题目答案及解析
稿件来源:高途
| 金属矿物的开发及利用题目答案及解析如下,仅供参考!
必修二
第四章 化学与可持续发展
第一节 开发利用金属矿物和海水资源
金属矿物的开发及利用
在钐钴永磁材料的成型加工过程中,会产生合金渣(含有$\rm Sm$、$\rm Co$、$\rm Cu$、$\rm Fe$)。从该合金渣提取钴$\rm (Co)$和钐$\rm (Sm)$的一种工艺流程如下。
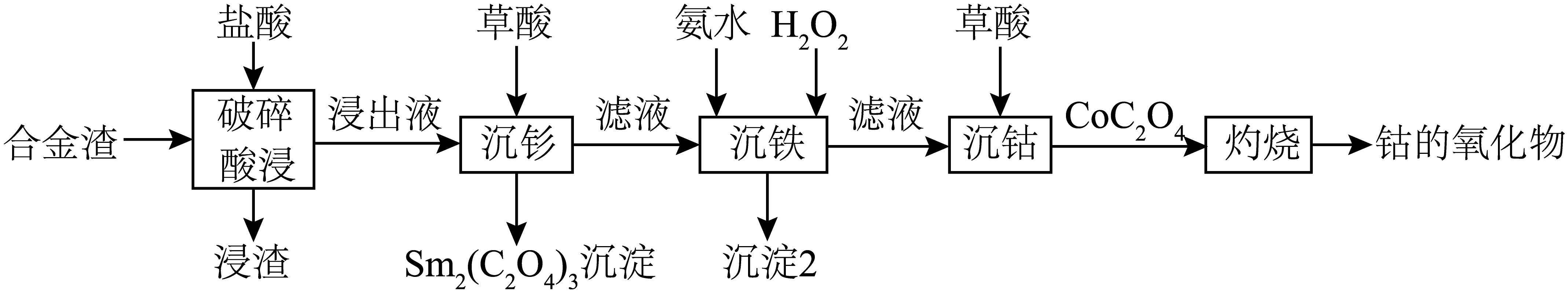
已知:$_{62}\text{Sm}$是一种稀土元素,活动性介于$\rm Na$与$\rm Al$之间。
回答下列问题:
与$\rm Co$同周期同族的元素还有$\rm Fe$和 (填元素符号)。
$\\rm Ni$
"]]$\rm Co$位于第四周期Ⅷ族,与$\rm Co$同周期同族的元素还有$\rm Fe$和$\rm Ni$;
工业上可通过 (填“电解”“热还原”或“热分解”)法制备$\rm Sm$。
电解
"]]$_{62}\text{Sm}$是一种稀土元素,活动性介于$\rm Na$与$\rm Al$之间,可知$\rm Sm$非常活泼,工业上可通过电解法制备$\rm Sm$;
“浸渣”的主要成分是 ;“破碎酸浸”过程中$\rm Sm$发生反应的化学方程式为 。
$\\rm Cu$;$\\rm 2Sm+6HCl=2SmCl_{3}+3H_{2}↑$
"]]“浸渣”的主要成分是$\rm Cu$;根据分析,“破碎酸浸”过程中$\rm Sm$发生反应的化学方程式为$\rm 2Sm+6HCl=2SmCl_{3}+3H_{2}↑$;
“沉铁”过程中加入氨水的主要目的是调节$\rm pH$。结合图中实验数据可知,溶液的最佳$\rm pH$为 。${{\text{H}}_{2}}{{\text{O}}_{2}}$的实际用量通常要大于理论用量,原因是 。
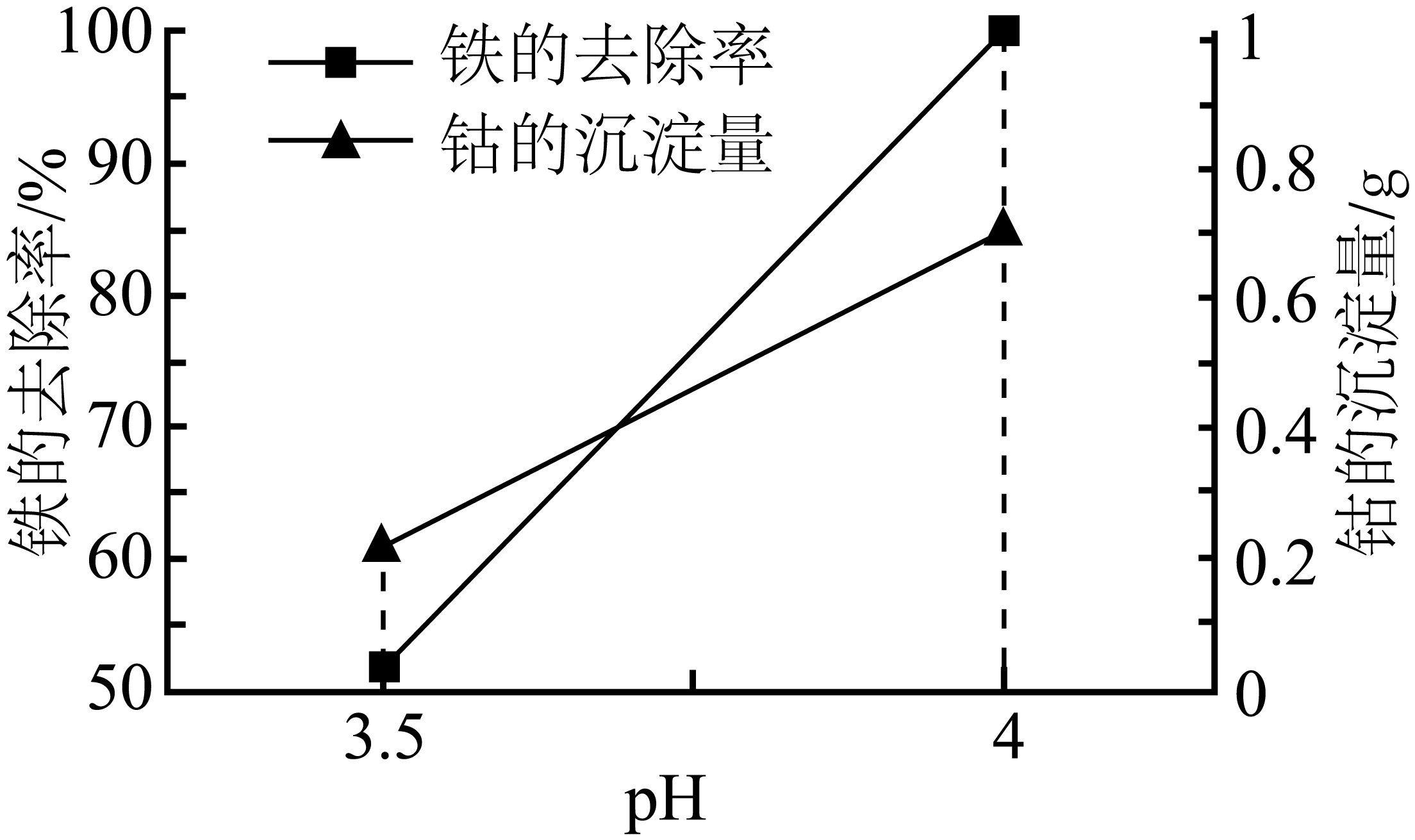
$\\rm 4$;铁离子会催化双氧水分解,消耗部分双氧水
"]]图中实验数据,“调节$\rm pH$”时,$\rm pH$为$\rm 4$时,铁的去除率最高,钴沉淀量不大,溶液的最佳$\rm pH$为$\rm 4$;“氧化”时,双氧水实际用量大于理论用量的原因是:铁离子会催化双氧水分解,消耗部分双氧水;
“$\text{Co}{{\text{C}}_{2}}{{\text{O}}_{4}}$”隔绝空气“灼烧”得$\text{C}{{\text{o}}_{3}}{{\text{O}}_{4}}$,反应的化学方程式为 。
$\\text{3Co}{{\\text{C}}_{2}}{{\\text{O}}_{4}}\\underset{{}}{\\overset{}{\\mathop{=}}}\\,\\text{C}{{\\text{o}}_{3}}{{\\text{O}}_{4}}+2\\text{C}{{\\text{O}}_{2}}\\uparrow +4\\text{CO}\\uparrow $
"]]“$\text{Co}{{\text{C}}_{2}}{{\text{O}}_{4}}$”隔绝空气“灼烧”得$\text{C}{{\text{o}}_{3}}{{\text{O}}_{4}}$,反应的化学方程式为$\text{3Co}{{\text{C}}_{2}}{{\text{O}}_{4}}\underset{}{\overset{{}}{\mathop{=}}}\,\text{C}{{\text{o}}_{3}}{{\text{O}}_{4}}+2\text{C}{{\text{O}}_{2}}\uparrow +4\text{CO}\uparrow $;
$\rm Sm$、$\rm Ni$、$\rm O$形成的稀土镍基氧化物的晶胞结构中$\rm Sm$和$\rm O$如图所示,$\rm Ni$位于$\rm O$形成的正八面体空隙中,则该稀土镍基氧化物的化学式为 。
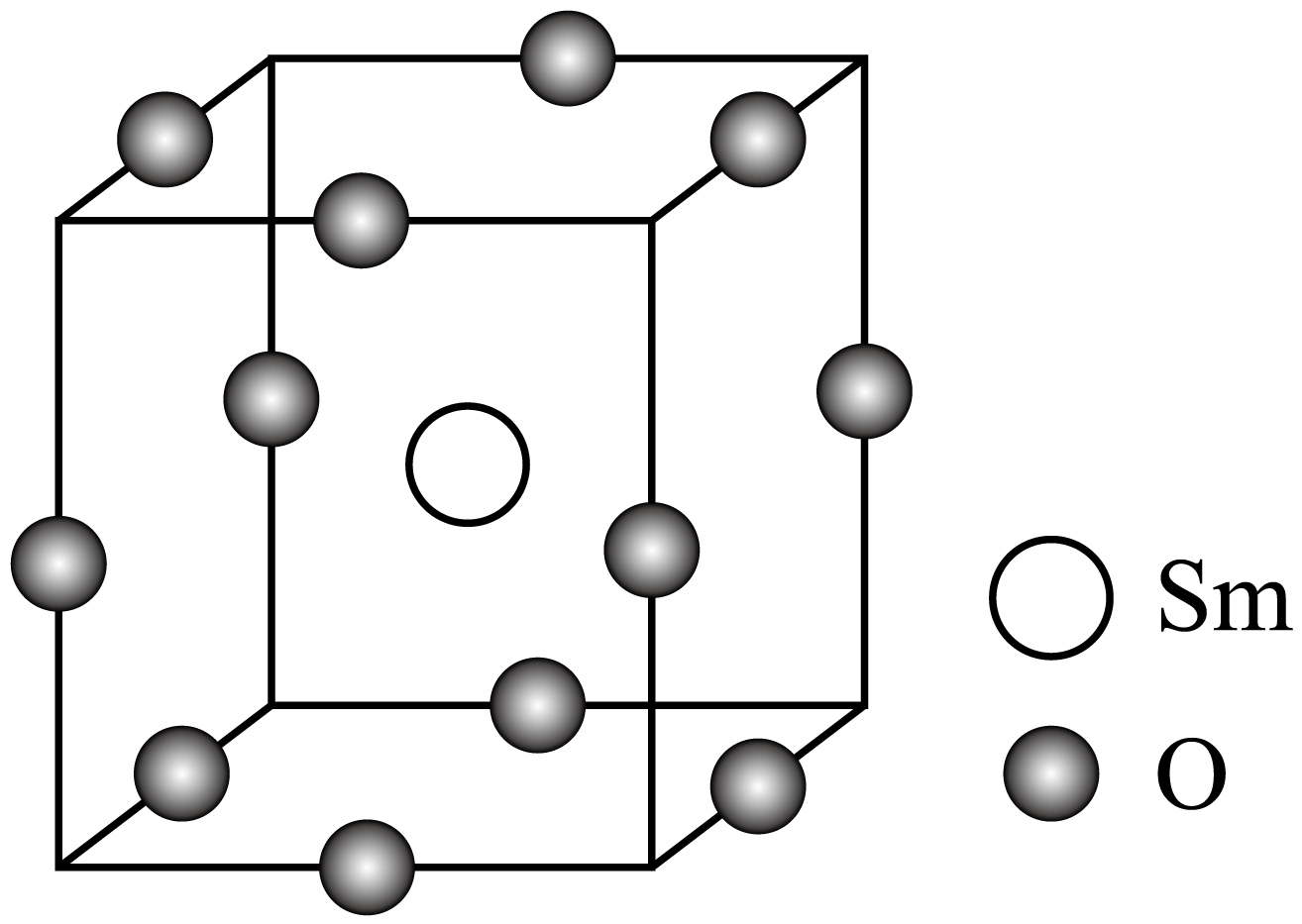
$\\text{SmNi}{{\\text{O}}_{3}}$
"]]$\rm Ni$位于$\rm O$形成的正八面体空隙中,则$\rm Ni$位于晶胞的顶点,该晶胞中含有$\rm 1$个$\rm Sm$原子,$8\times \dfrac{1}{8}\rm =1$个$\rm Ni$原子,$12\times \dfrac{1}{4}\rm =3$个$\rm O$原子,则该稀土镍基氧化物的化学式为$\text{SmNi}{{\text{O}}_{3}}$。
| 金属矿物的开发及利用题目答案及解析(完整版)
