高中 | 离子化合物 题目答案及解析
稿件来源:高途
高中 | 离子化合物题目答案及解析如下,仅供参考!
必修二
第一章 物质结构 元素周期律
第三节 化学键
离子化合物
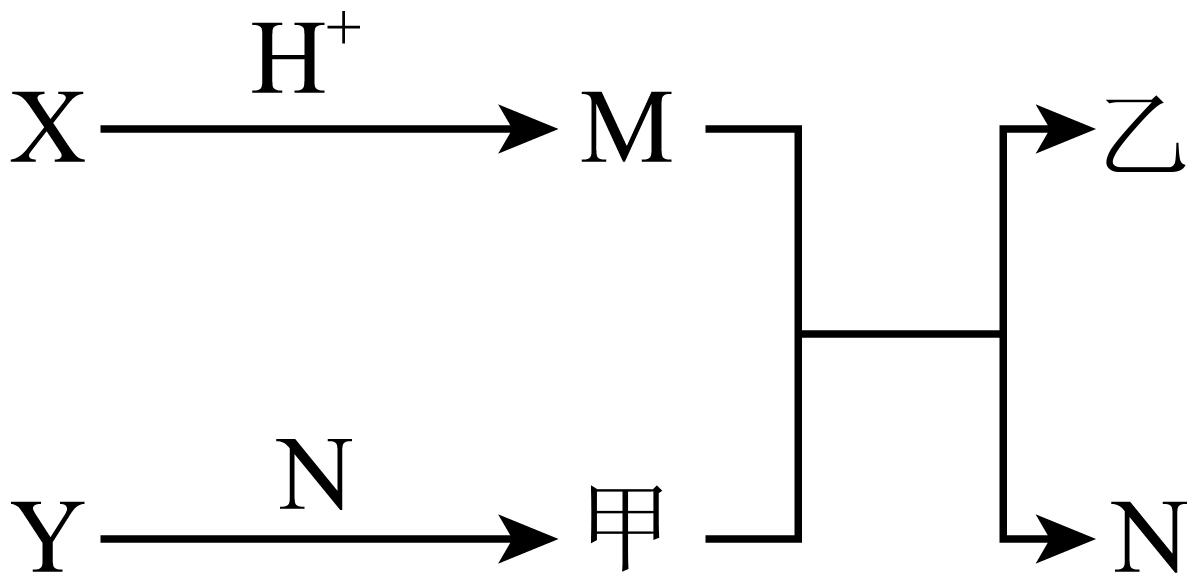
已知$\rm A$、$\rm B$、$\rm C$、$\rm D$为短周期内原子半径依次增大的元素,$\rm X$、$\rm Y$、$\rm M$、$\rm N$分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两种元素对应的单质,若$\rm X$与$\rm Y$、甲与乙摩尔质量相同,$\rm Y$与乙均为淡黄色固体,上述物质之间的转化关系如图所示$\rm ($部分反应物或生成物省略$\rm )$,则下列说法中不正确的是$(\qquad)$
电负性:$\\rm D\\lt C\\lt A\\lt B$
","相对分子质量$\\rm M\\gt N$,沸点$\\rm N\\gt M$
","简单离子半径:${{\\text{C}}^{\\text{2}-}}\\gt {{\\text{B}}^{\\text{2}-}}\\gt {{\\text{D}}^{+}}\\gt {{\\text{A}}^{+}}$
","$\\rm D$与其他元素均能形成离子化合物
"]已知$\rm A$、$\rm B$、$\rm C$、$\rm D$为短周期内原子半径依次增大的元素,$\rm X$、$\rm Y$、$\rm M$、$\rm N$分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两种元素对应的单质。若$\rm X$与$\rm Y$、甲与乙摩尔质量相同,$\rm Y$与乙均为淡黄色固体,$\rm Y$为$\rm Na_{2}O_{2}$,乙为$\rm S$,甲为$\rm O_{2}$,$\rm X$为$\rm Na_{2}S$,结合转化关系图,则$\rm M$为$\rm H_{2}S$,$\rm N$为$\rm H_{2}O$,故$\rm A$为$\rm H$,$\rm B$为$\rm O$,$\rm C$为$\rm S$,$\rm D$为$\rm Na$。
$\rm A$.同周期从左往右元素的电负性递增,同主族从上往下元素的电负性递减,电负性:$\rm Na\lt S\lt O$,又根据$\rm H_{2}S$中$\rm S$显负价,判断出$\rm H$的电负性小于$\rm S$,$\rm A$错误;
$\rm B$.$\rm M$为$\rm H_{2}S$,$\rm N$为$\rm H_{2}O$,水分子间能够形成氢键,沸点高于$\rm H_{2}S$,$\rm B$正确;
$\rm C$.核外电子层数越多离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,简单离子半径:$\rm S^{2-}\gt O^{2-}\gt Na^{+}\gt H^{+}$,$\rm C$正确;
$\rm D$.$\rm Na$属于活泼金属,与$\rm H$、$\rm O$、$\rm S$元素均能形成离子化合物,$\rm D$正确。
故选:$\rm A$
高中 | 离子化合物题目答案及解析(完整版)
