| 氧化还原反应方程式的书写及配平 题目答案及解析
稿件来源:高途
| 氧化还原反应方程式的书写及配平题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应方程式的书写及配平
水体中氨氮含量超标会造成水体富营养化,用次氯酸钙$\left[ \text{Ca}{{\left( \text{ClO} \right)}_{\text{2}}} \right]$除去氨氮的原理如图所示。下列说法不正确的是$(\qquad)$
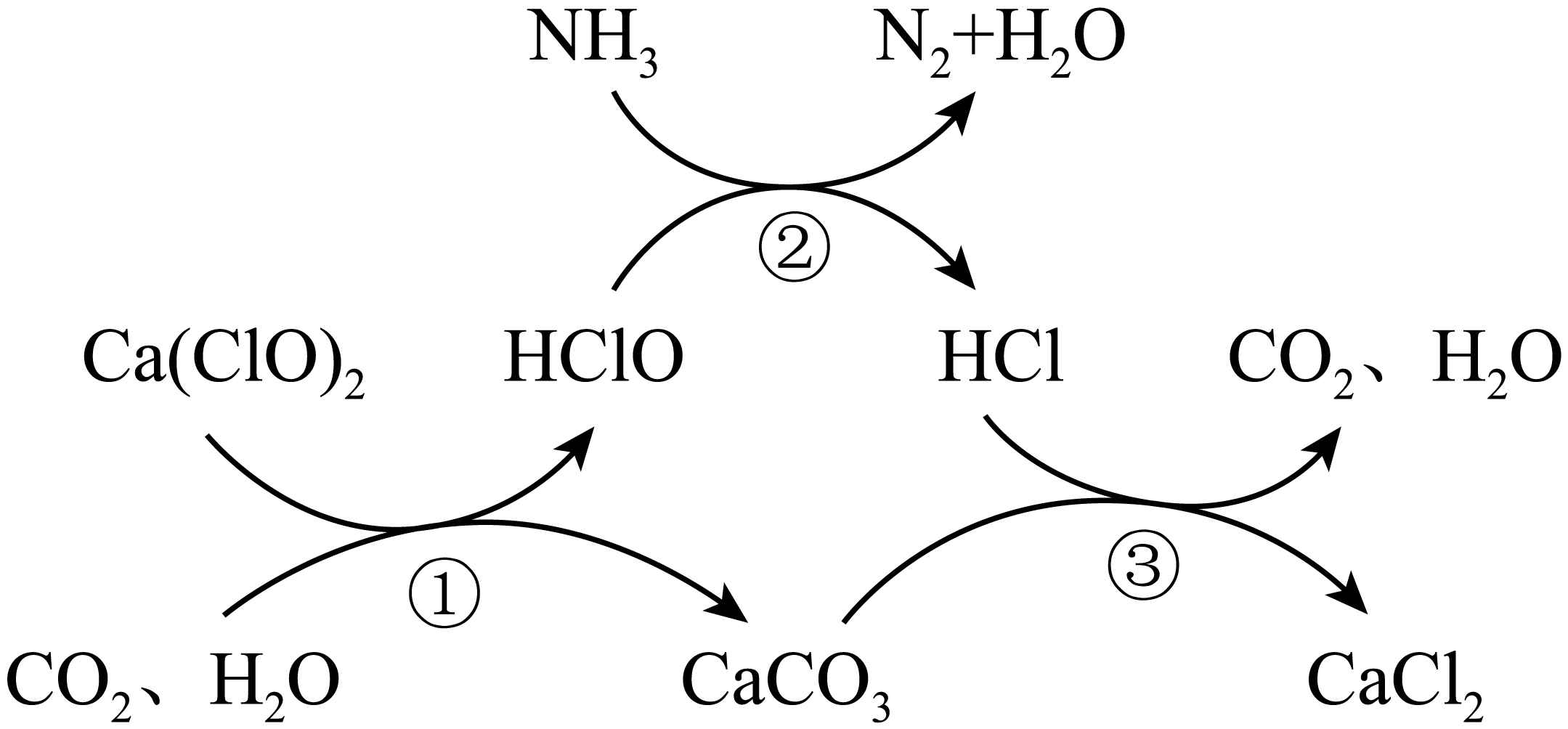
①③属于复分解反应,②属于氧化还原反应
","$\\text{C}{{\\text{O}}_{2}}$、${{\\text{H}}_{2}}\\text{O}$两种物质可循环使用
","每生成$\\rm 1$个${{\\text{N}}_{2}}$,转移$\\rm 3$个电子
","除去氨氮的总反应方程式为$4\\text{N}{{\\text{H}}_{3}}+3\\text{Ca}{{(\\text{ClO})}_{2}}=2{{\\text{N}}_{2}}+3\\text{CaC}{{\\text{l}}_{2}}+6{{\\text{H}}_{2}}\\text{O}$
"]$\rm A$.①③均属于盐和酸反应生成新盐和新酸,故①③属于复分解反应、没有化合价的变化,②中氮元素和氯元素化合价发生变化,属于氧化还原反应,故$\rm A$正确;
$\rm B$.③中生成的$\rm CO_{2}$、$\rm H_{2}O$可以供①使用,这两种物质可循环使用,故$\rm B$正确;
$\rm C$. $\rm NH_{3}$生成$\rm N_{2}$,氮元素从$\rm -3$价升高到$\rm 0$价、氯元素从$\rm +1$价降低到$\rm -1$价,则按得失电子数守恒,每生成$\rm 1\;mol\;N_{2}$,转移$\rm 6\;\rm mol$电子,故$\rm C$错误;
$\rm D$.据图可知,除去氨氮的总反应方程式为:$\rm 4NH_{3}+3Ca(ClO)_{2}=2N_{2}+3CaCl_{2}+6H_{2}O$,故$\rm D$正确。
故选:$\rm C$
| 氧化还原反应方程式的书写及配平题目答案及解析(完整版)
