高中 | 氯气 题目答案及解析
稿件来源:高途
高中 | 氯气题目答案及解析如下,仅供参考!
必修一
第四章 非金属及其化合物
第二节 富集在海水中的元素——氯
氯气
室温下,$\rm 1$体积的水能溶解约$\rm 2$体积的$\rm C{{l}_{2}}$。用试管收集$\rm C{{l}_{2}}$后进行如图所示实验,下列对实验现象的分析或预测正确的是$\rm (\qquad)$
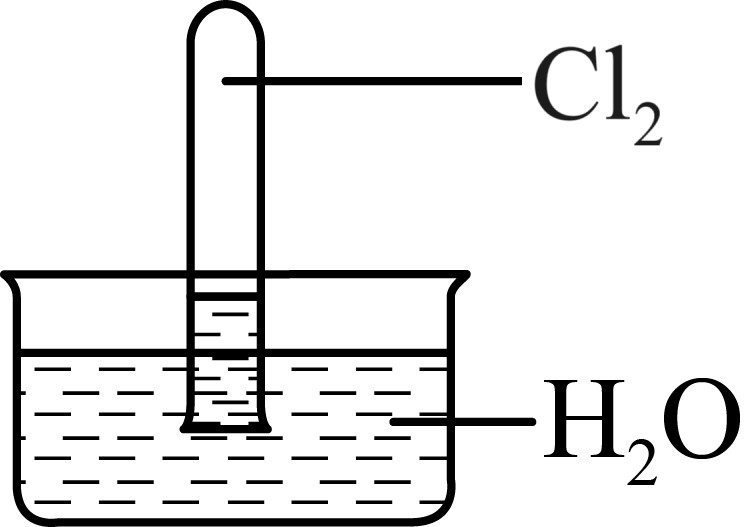
试管内液面上升,证明$\\rm C{{l}_{2}}$与水发生了反应
","取出试管中的溶液,加入少量$\\rm CaC{{O}_{3}}$粉末,溶液漂白能力减弱
","取出试管中的溶液,滴加紫色石蕊溶液,溶液先变红后褪色,加热后颜色又变为红色
","取出试管中的溶液,光照一段时间后$\\rm pH$下降,与反应$\\rm 2HClO\\begin{matrix} \\underline{\\underline{光照}} \\\\ {} \\\\ \\end{matrix}2HCl+{{O}_{2}}\\uparrow $有关
"]$\rm A$.由题目信息可知,氯气能溶于水,也可以使试管内液面上升,不能证明氯气和水发生了反应,$\rm A$错误。
$\rm B$.氯气与水反应的方程式为:$\rm C{{l}_{2}}+{{H}_{2}}O\rightleftharpoons HCl+HClO$,加入少量$\rm CaCO_{3}$粉末会与$\rm HCl$反应,使平衡右移,$\rm HClO$浓度增大,溶液漂白能力增强,$\rm B$错误。
$\rm C$.取出试管中的溶液,滴加紫色石蕊溶液,由于溶液中有$\rm HCl$和$\rm HClO$,所以溶液先变红,次氯酸具有漂白性会使溶液褪色,次氯酸的强氧化性漂白不可逆,加热后颜色不会恢复,$\rm C$错误。
$\rm D$.取出试管中的溶液,光照一段下发生反应:$\rm 2HClO\begin{matrix} \underline{\underline{光照}} \\ {} \\ \end{matrix}2HCl+{{O}_{2}}\uparrow $,生成$\rm HCl$,同时次氯酸浓度下降,可能使$\rm C{{l}_{2}}+{{H}_{2}}O\rightleftharpoons HCl+HClO$平衡右移,$\rm HCl$浓度增大,溶液酸性增强,$\rm pH$下降,$\rm D$正确。
故选:$\rm D$
高中 | 氯气题目答案及解析(完整版)
