高中 | 导电的原因及条件 题目答案及解析
稿件来源:高途
高中 | 导电的原因及条件题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第二节 离子反应
导电的原因及条件
天宫课堂中,王亚平老师用醋酸钠$\rm ($化学式:$\text{C}{{\text{H}}_{3}}\text{COONa}\rm )$的过饱和溶液做了一个“太空冰雪”的趣味实验,在微重力环境下,使一颗“水球”瞬间变成了一颗“冰球”,因此对醋酸和醋酸钠的性质进行深入学习。请回答下列问题:
从物质分类上看,醋酸钠属于$(\quad\ \ \ \ )$。
酸
","碱
","盐
","非电解质
","电解质
","混合物
"]电解质是溶于水或在熔融状态下能够导电的化合物;盐是由金属阳离子或铵根离子和酸根离子构成的化合物;醋酸钠是由钠离子和醋酸根离子构成的,属于盐也属于电解质;醋酸溶液为混合物;
已知:醋酸是一种弱酸,属于弱电解质,在水中不能完全电离。下列图示中不能说明醋酸是弱电解质的是$(\quad\ \ \ \ )$。
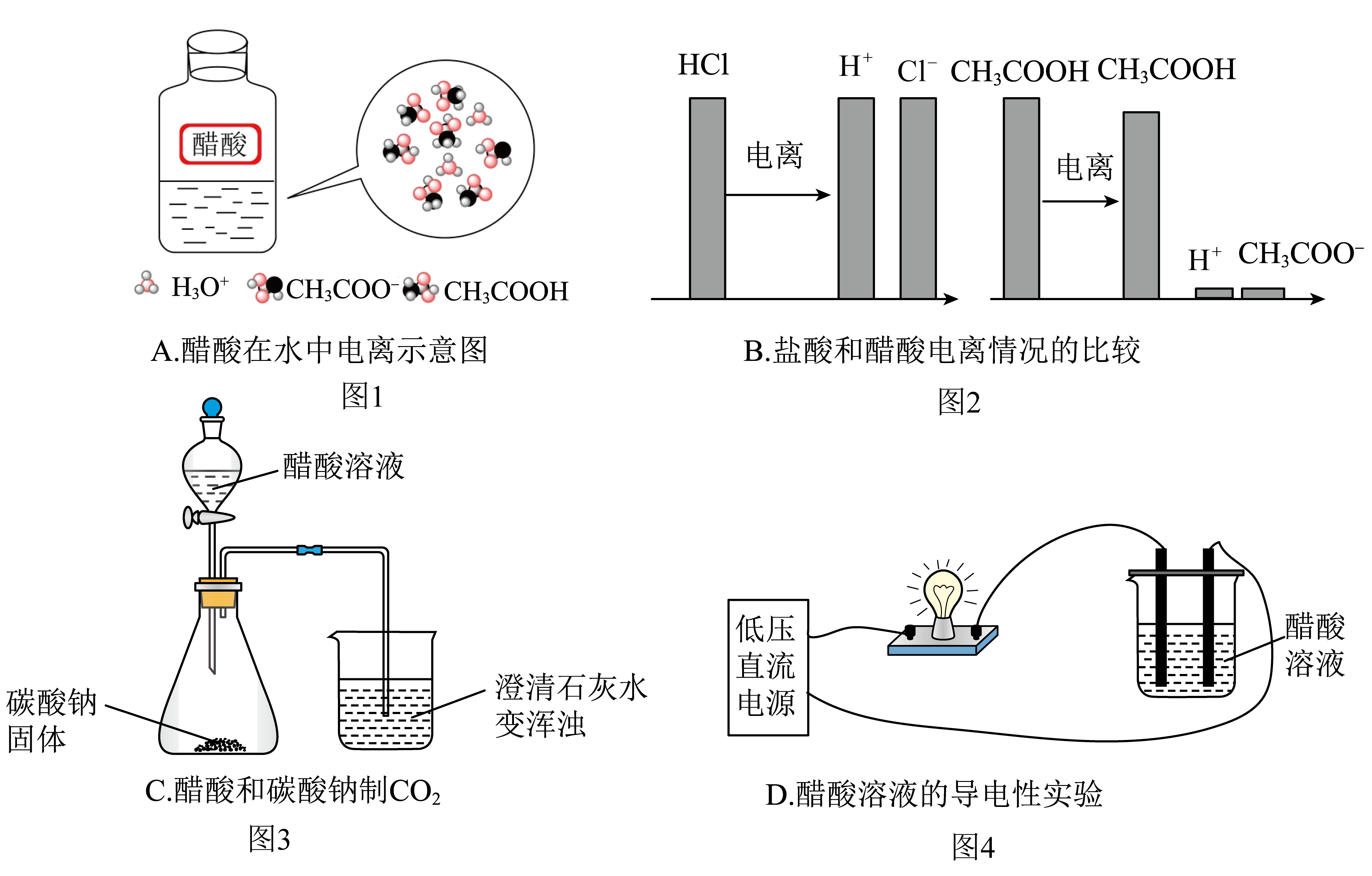
图$\\rm 1$:醋酸在水中电离示意图
","图$\\rm 2$:盐酸和醋酸电离情况的比较
","图$\\rm 3$:醋酸和碳酸钠制$\\text{C}{{\\text{O}}_{2}}$
","图$\\rm 4$:醋酸溶液的导电性实验
"]$\rm A\rm .$ 图$\rm 1$:醋酸在水中电离示意图,可以看出同时存在离子和分子,可知醋酸部分电离,是弱电解质,$\rm A$不符合题意;$\rm B$. 图$\rm 2$:盐酸和醋酸电离情况的比较,可以看出盐酸完全电离,醋酸部分电离,醋酸是弱电解质,$\rm B$不符合题意;$\rm C$. 图$\rm 3$:醋酸和碳酸钠制$\rm \text{C}{{\text{O}}_{2}}$只能能证明醋酸得酸性强于碳酸,无法证明醋酸是强酸还是弱酸,$\rm C$符合题意;$\rm D$. 图$\rm 4$:醋酸溶液的导电性实验,只能证明醋酸是电解质,不能证明是强电解质还是弱电解质,$\rm D$符合题意;答案选$\rm CD$。
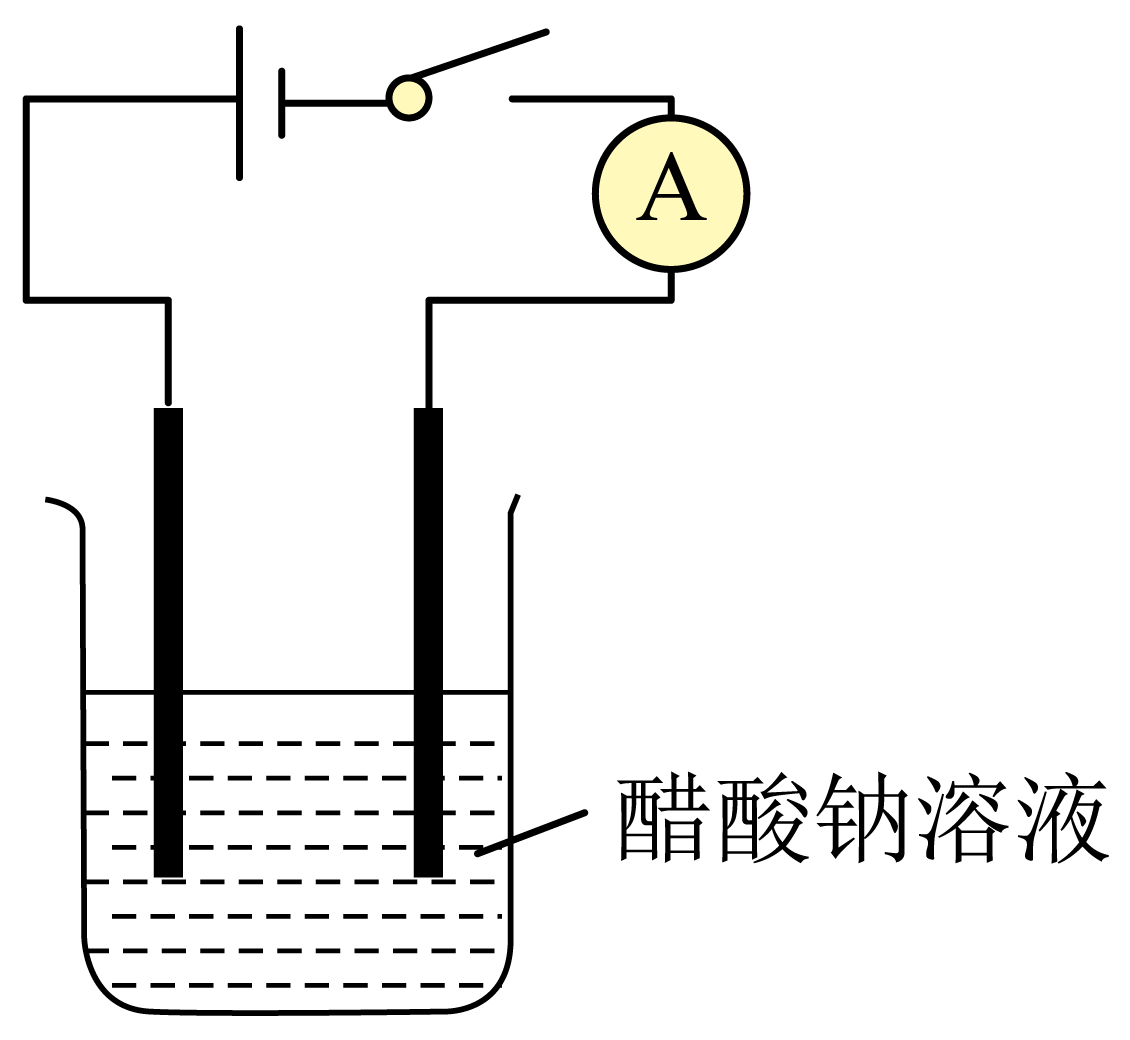
同学们将醋酸钠溶液接入如图所示的电路中,闭合开关,电流表的示数为$\rm 0.10\;A$,继续往溶液中添加适量醋酸钠固体,并用玻璃棒不断搅拌,电流表示数不断增大,最终示数为$\rm 0.24\;A$,据此推测,在醋酸钠水溶液中存在着能导电的微粒是 $\rm ($填微粒符号、不考虑${{\text{H}}^{+}}$、$\text{O}{{\text{H}}^{-}}\rm )$。醋酸钠在水溶液中的电离方程式为 。
$\\text{C}{{\\text{H}}_{3}}\\text{CO}{{\\text{O}}^{-}}$、$\\text{N}{{\\text{a}}^{+}}$;$\\text{C}{{\\text{H}}_{3}}\\text{COONa=C}{{\\text{H}}_{3}}\\text{CO}{{\\text{O}}^{-}}+\\text{N}{{\\text{a}}^{+}}$
"]]溶液或熔融电解质导电的原因是存在自由移动的离子,醋酸钠水溶液中存在着能导电的微粒是醋酸钠电离出的醋酸根离子和钠离子;醋酸钠在水中完全电离出钠离子和醋酸根离子,电离方程式为$\text{C}{{\text{H}}_{3}}\text{COONa=C}{{\text{H}}_{3}}\text{CO}{{\text{O}}^{-}}+\text{N}{{\text{a}}^{+}}$;
①往盛有$\rm NaOH$溶液的烧杯中逐滴滴加等浓度的醋酸溶液,直至过量。请写出醋酸溶液与$\rm NaOH$溶液反应的离子方程式: 。
②随着醋酸的滴入,烧杯中溶液的电导率随滴入醋酸溶液的体积变化趋势与下图一致的是 $\rm ($填字母$\rm )$。
$\rm A$.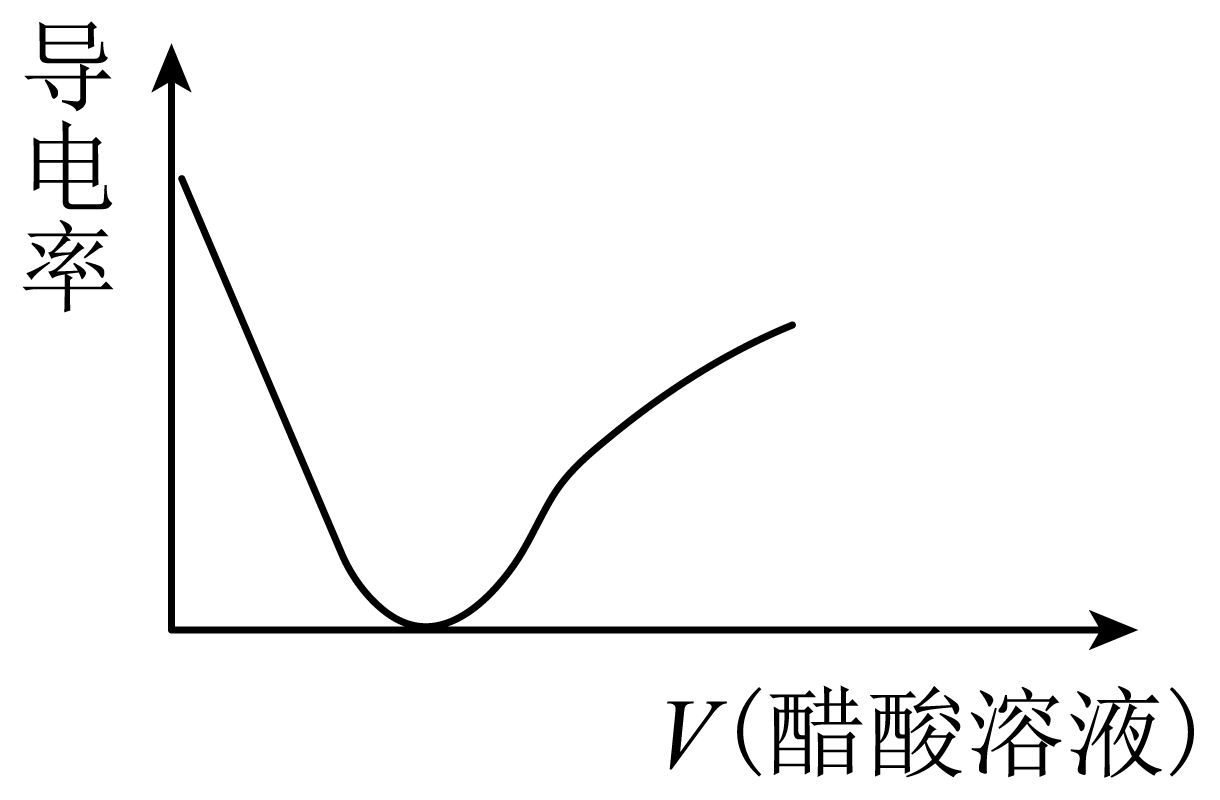 $\rm B$.
$\rm B$.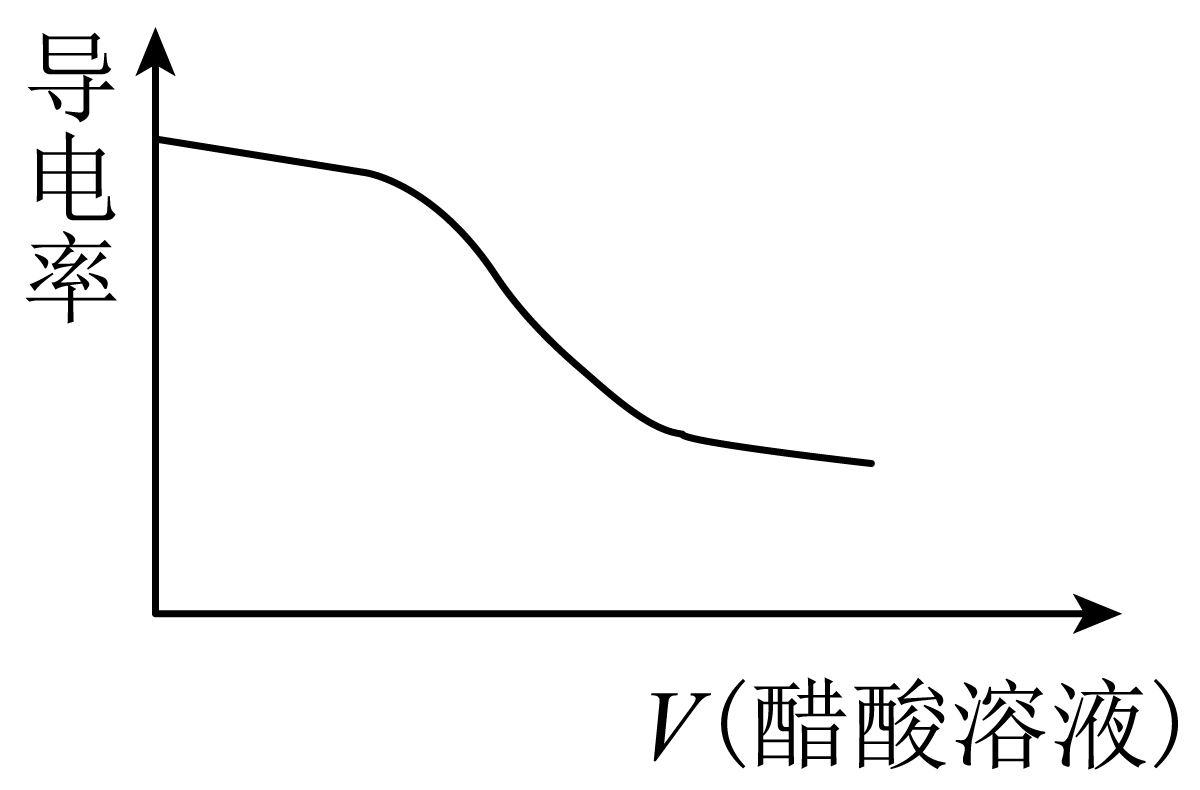 $\rm C$.
$\rm C$.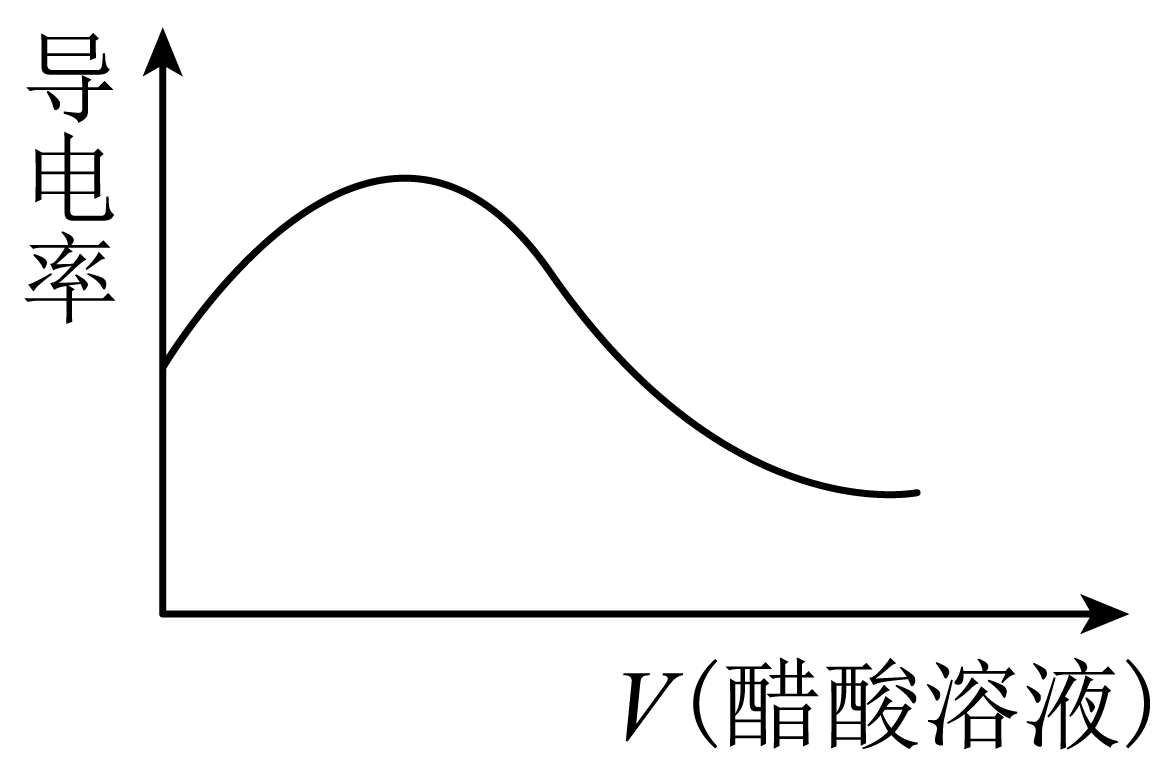 $\rm D$.
$\rm D$.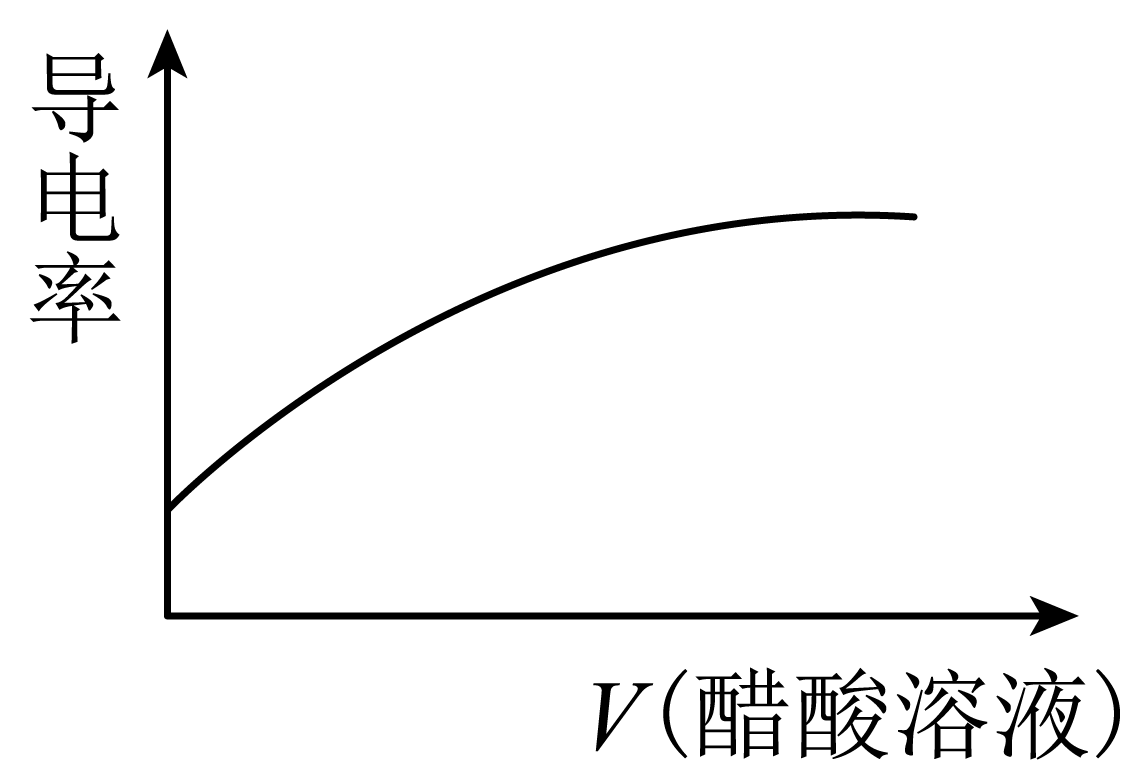
$\\rm \\text{C}{{\\text{H}}_{3}}\\text{COOH+O}{{\\text{H}}^{-}}\\text{=C}{{\\text{H}}_{3}}\\text{CO}{{\\text{O}}^{-}}+{{\\text{H}}_{\\text{2}}}\\text{O}$;$\\rm B$
"]]①醋酸为弱酸,醋酸溶液与$\rm NaOH$溶液反应生成醋酸钠和水,离子方程式为$\rm \text{C}{{\text{H}}_{3}}\text{COOH+O}{{\text{H}}^{-}}\text{=C}{{\text{H}}_{3}}\text{CO}{{\text{O}}^{-}}+{{\text{H}}_{\text{2}}}\text{O}$;②溶液或熔融电解质导电的原因是存在自由移动的离子;往盛有$\rm NaOH$溶液的烧杯中逐滴滴加等浓度的醋酸溶液,两者反应生成与加入醋酸等物质的量的醋酸钠,但是溶液体积增大,溶液中自由移动离子浓度减小,导致其电导率减弱,故选:$\rm B$。
高中 | 导电的原因及条件题目答案及解析(完整版)
