高中 | 氯气 题目答案及解析
稿件来源:高途
高中 | 氯气题目答案及解析如下,仅供参考!
必修一
第四章 非金属及其化合物
第二节 富集在海水中的元素——氯
氯气
不同的温度下,$\text{C}{{\text{l}}_{2}}$通入$\rm NaOH$溶液中主要发生以下两个反应,如图所示。
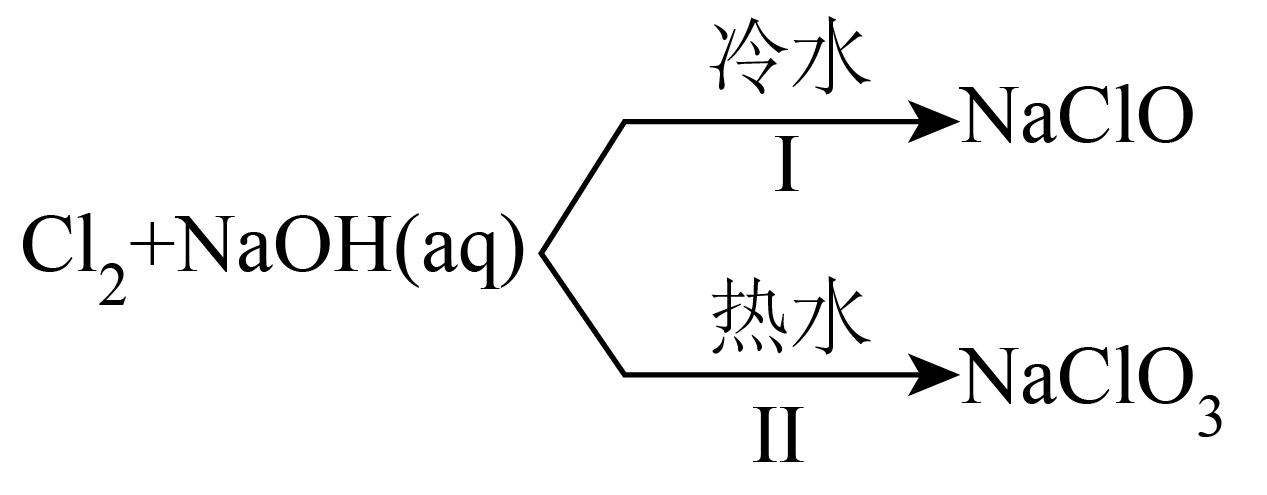
下列说法不正确的是$(\qquad)$
反应Ⅰ和Ⅱ都有$\\rm NaCl$生成
","$\\text{ClO}_{3}^{-}$的空间结构为三角锥形
","反应Ⅰ和Ⅱ中,每$1\\text{molC}{{\\text{l}}_{2}}$参与反应转移的电子数之比为$3:5$
","反应Ⅰ和Ⅱ中,参加反应的$\\text{C}{{\\text{l}}_{2}}$与$\\rm NaOH$的物质的量之比:Ⅰ$\\rm \\lt $Ⅱ
"]由图可知,氯气与氢氧化钠溶液在冷水条件下反应生成氯化钠、次氯酸钠和水,根据化合价升降守恒、原子守恒,反应的化学方程式为$\rm Cl_{2}+2NaOH=NaCl+NaClO+H_{2}O$,在热水条件下反应生成氯化钠、氯酸钠和水,根据化合价升降守恒、原子守恒,反应的化学方程式为$\rm 3Cl_{2}+6NaOH=5NaCl+NaClO_{3}+3H_{2}O$。
$\rm A$.由分析可知,反应Ⅰ和Ⅱ都有氯化钠生成,$\rm A$正确;
$\rm B$.$\text{ClO}_{3}^{-}$里中心原子$\rm Cl$的价层电子对数为$3+\dfrac{7+1-3\times 2}{2}=3+1=4$,孤对电子对数为$\rm 1$,则其空间结构为三角锥形,$\rm B$正确;
$\rm C$.反应Ⅰ中存在关系式:$\text{C}{{\text{l}}_{2}}\sim \text{NaCl}\sim \text{NaClO}\sim {{\text{e}}^{-}}$,$\rm 1\;\rm mol$氯气参加反应,反应转移$\rm 1\;\rm mol$电子,反应Ⅱ中存在关系式:$\text{3C}{{\text{l}}_{2}}\sim 5\text{NaCl}\sim \text{NaCl}{{\text{O}}_{3}}\sim 5{{\text{e}}^{-}}$,$\rm 1\;\rm mol$氯气参加反应,反应转移$\dfrac{5}{3}\ \rm mol$电子,则反应转移的电子数之比为$\rm 3:5$,$\rm C$正确;
$\rm D$.由分析可知,反应Ⅰ和Ⅱ中,参加反应的氯气与氢氧化钠的物质的量之比都为$\rm 1$:$\rm 2$,$\rm D$错误;
故选:$\rm D$
高中 | 氯气题目答案及解析(完整版)
