高中 | 氯气 题目答案及解析
稿件来源:高途
高中 | 氯气题目答案及解析如下,仅供参考!
必修一
第四章 非金属及其化合物
第二节 富集在海水中的元素——氯
氯气
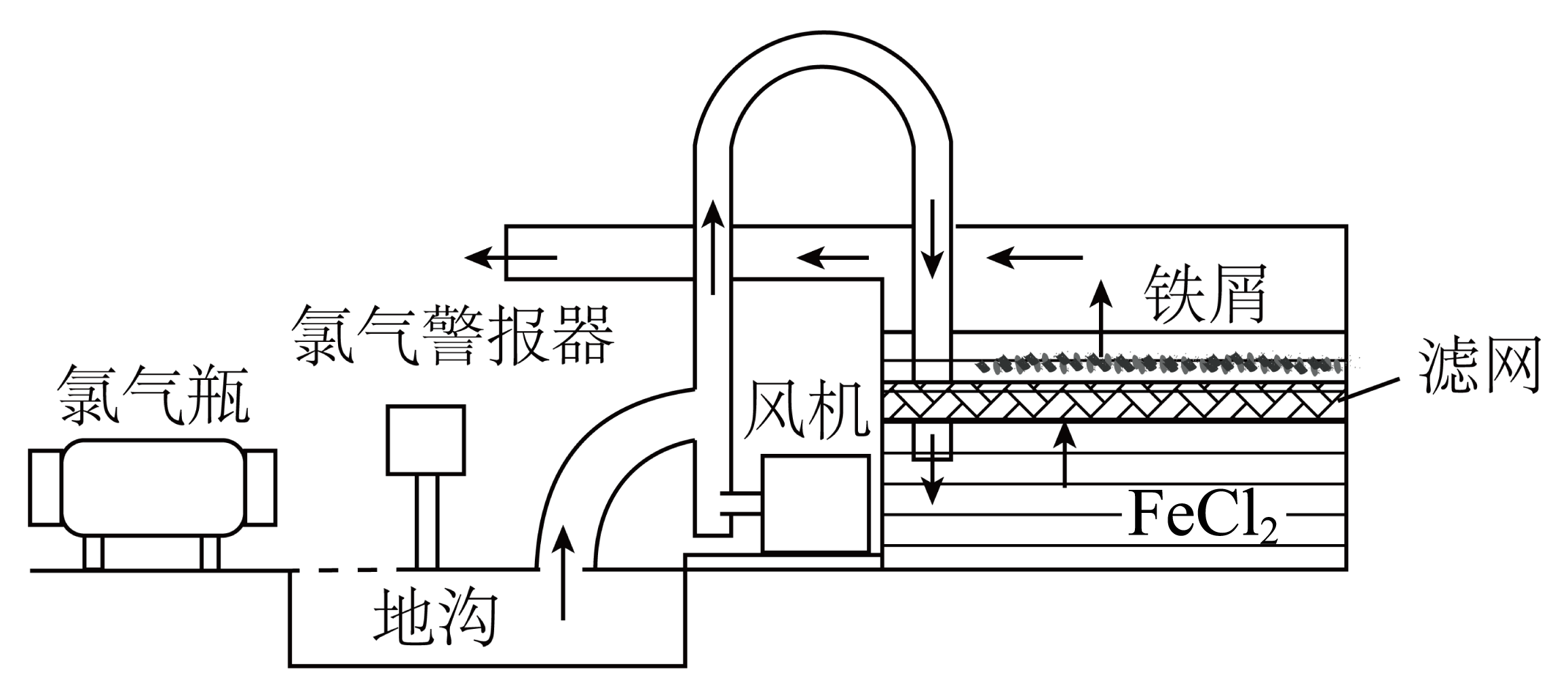
氯气是常用的化工原料,可用作消毒剂和漂白剂;实验室用$\rm Mn{{O}_{2}}$和浓盐酸反应可制取氯气。氯气有毒,泄漏时需要妥善处理。自来水厂一种预防和处理$\rm C{{l}_{2}}$泄漏的方法如图所示。下列有关说法不正确的是$\rm (\qquad)$
$\\rm C{{l}_{2}}$和水反应的离子方程式为$\\rm {{H}_{2}}O+C{{l}_{2}}\\rightleftharpoons C{{l}^{-}}+HCl{{O}^{-}}+{{H}^{+}}$
","铁屑的作用是将$\\rm FeC{{l}_{3}}$还原为$\\rm FeC{{l}_{2}}$
","铁屑耗尽时溶液中可能大量存在:$\\rm F{{e}^{2+}}$、$\\rm F{{e}^{3+}}$、$\\rm Cl{{O}^{-}}$、$\\rm C{{l}^{-}}$
","吸收漏氯的离子方程式为$\\rm 2F{{e}^{2+}}+C{{l}_{2}}=2C{{l}^{-}}+2F{{e}^{3+}}$
"]$\rm A$.$\rm Cl_{2}$和水反应生成盐酸和次氯酸,反应的离子方程式为:$\rm H_{2}O+Cl_{2}\rightleftharpoons Cl^{-}+HClO+H^{+}$,$\rm A$正确。
$\rm B$.$\rm 2FeCl_{3}+Fe=3FeCl_{2}$,铁屑的作用是将$\rm FeCl_{3}$还原为$\rm FeCl_{2}$,$\rm B$正确。
$\rm C$.$\rm ClO^{-}$能把$\rm Fe^{2+}$氧化为$\rm Fe^{3+}$,$\rm Fe^{2+}$、$\rm ClO^{-}$不能大量共存,$\rm C$错误。
$\rm D$.氯化亚铁吸收氯气生成氯化铁,吸收漏氯的离子方程式为:$\rm 2Fe^{2+}+Cl_{2}=2Cl^{-}+2Fe^{3+}$,$\rm D$正确。
故选:$\rm C$
高中 | 氯气题目答案及解析(完整版)
