高中 | 配合物理论 题目答案及解析
稿件来源:高途
高中 | 配合物理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
配合物理论
$\text{N}{{\text{H}}_{3}}$脱$\rm NO$的一种$\text{Mn}{{\text{O}}_{2}}$催化机理如图所示。下列说法错误的是$(\qquad)$
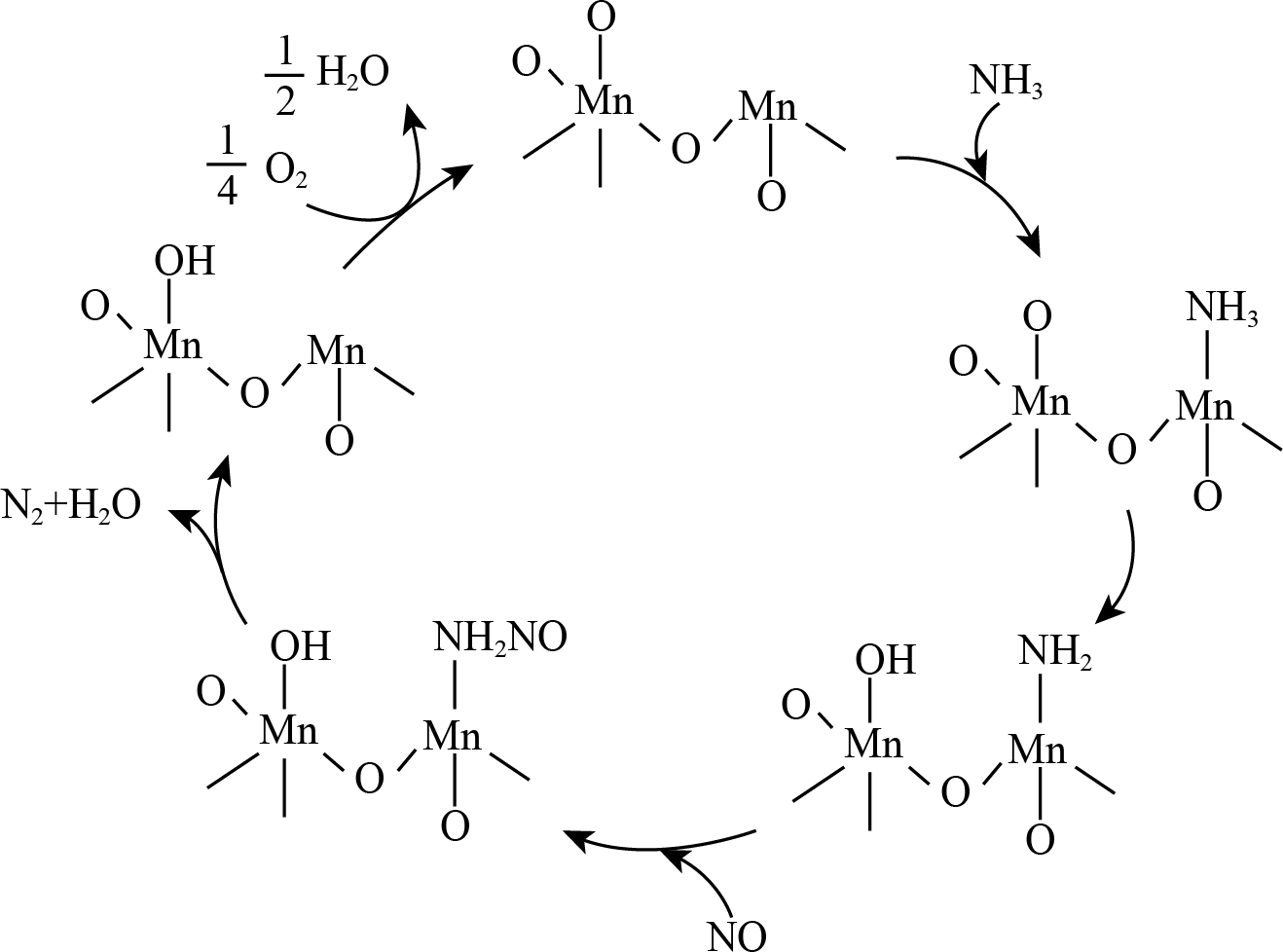
$\\text{Mn}{{\\text{O}}_{2}}$能结合$\\text{N}{{\\text{H}}_{3}}$的原因是$\\rm Mn$有空轨道能接受孤电子对,形成配位键
","催化过程中$\\rm Mn$的配位数和化合价发生了改变
","$\\text{Mn}{{\\text{O}}_{2}}$能加快反应速率,提高$\\text{N}{{\\text{H}}_{3}}$脱$\\rm NO$的平衡转化率
","总反应方程式为:$4\\text{N}{{\\text{H}}_{3}}+4\\text{NO}+{{\\text{O}}_{2}}\\begin{matrix} \\underline{\\underline{催化剂}} \\\\ {} \\\\ \\end{matrix}4{{\\text{N}}_{2}}+6{{\\text{H}}_{2}}\\text{O}$
"]$\rm A$.氨分子中氮原子具有孤对电子,二氧化锰中锰原子具有空轨道,氮原子和锰原子通过形成配位键使二氧化锰和氨分子相互结合,$\rm A$正确;
$\rm B$.从图中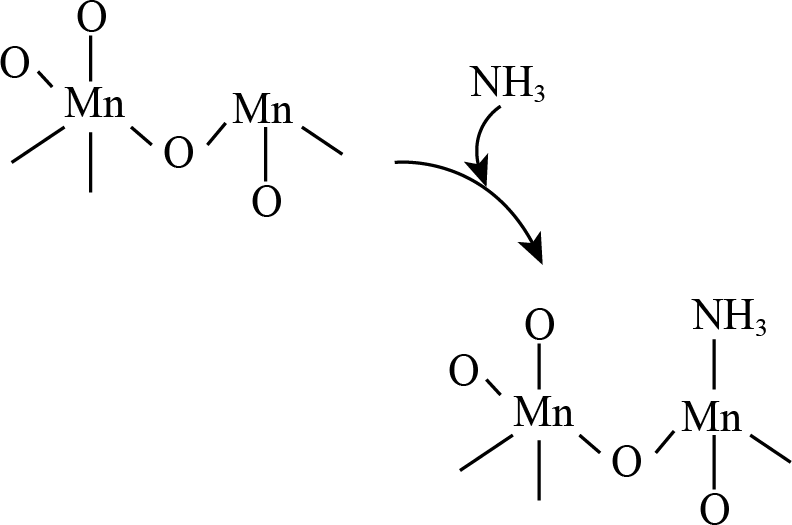 可以看出$\rm Mn$ 所形成的共价键数目变化了,说明其配位数和化合价都有变化,$\rm B$正确;
可以看出$\rm Mn$ 所形成的共价键数目变化了,说明其配位数和化合价都有变化,$\rm B$正确;
$\rm C$.$\rm MnO_{2}$作为反应的催化剂可以加快反应速率,但不该变平衡,不能提高平衡转化率,$\rm C$错误;
$\rm D$.根据示意图可知,反应物有 $\rm NH_{3}$、$\rm NO$、$\rm O_{2}$,产物有$\rm N_{2}$、$\rm H_{2}O$,故反应方程式为$4\text{N}{{\text{H}}_{3}}+4\text{NO}+{{\text{O}}_{2}}\begin{matrix} \underline{\underline{催化剂 }} \\ {} \\ \end{matrix}4{{\text{N}}_{2}}+6{{\text{H}}_{2}}\text{O}$,$\rm D$正确。
故选:$\rm C$
高中 | 配合物理论题目答案及解析(完整版)
