高中 | 配合物理论 题目答案及解析
稿件来源:高途
高中 | 配合物理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
配合物理论
某离子液体结构如图所示,$\rm Q$、$\rm R$、$\rm T$、$\rm X$、$\rm Y$和$\rm Z$是原子序数依次增大的短周期主族元素,基态$\rm T$原子和$\rm Y$原子最外层均有两个单电子,$\rm Q$、$\rm R$、$\rm X$和$\rm Z$质子数均为奇数且和为$\rm 22$。下列说法错误的是$(\quad\ \ \ \ )$
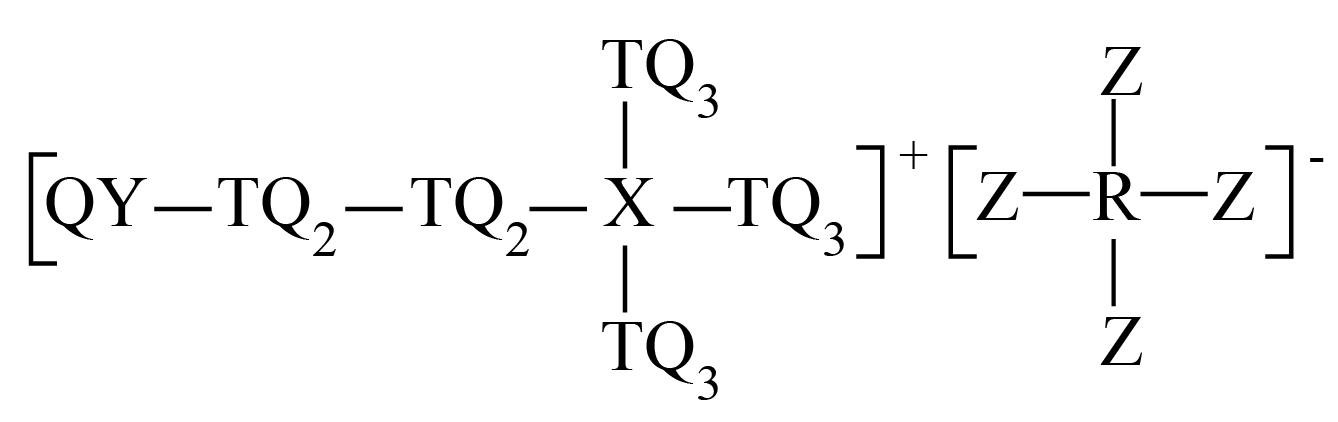
简单氢化物的稳定性:$\\rm Y\\gt X\\gt T$
","该阴离子含有配位键
","$\\text{R}{{\\text{Z}}_{3}}$为极性分子
","该离子液体难挥发,可用作溶剂
"]$\rm Q$、$\rm R$、$\rm T$、$\rm X$、$\rm Y$和$\rm Z$是原子序数依次增大的短周期主族元素,阳离子结构中$\rm Q$只形成$\rm 1$条共价键,可知$\rm Q$处于$\rm IA$族或$\rm VIIA$族,而阴离子中$\rm Z$也形成$\rm 1$条共价键,则$\rm Z$处于$\rm VIIA$族,$\rm Q$、$\rm R$、$\rm X$和$\rm Z$的质子数均为奇数且之和为$\rm 22$,$\rm Q$的原子序数又最小,可知$\rm Q$为$\rm H$元素,而$\rm Z$只能为$\rm F$元素;$\rm R$、$\rm T$、$\rm X$、$\rm Y$均处于第二周期,基态$\rm T$原子和$\rm Y$原子的最外层均有两个单电子,$\rm T$、$\rm Y$的价电子排布式依次为$2{{\text{s}}^{2}}2{{\text{p}}^{2}}$、$2{{\text{s}}^{2}}2{{\text{p}}^{4}}$,故$\rm T$为$\rm C$元素、$\rm Y$为$\rm O$元素;$\rm X$的原子序数介于碳、氧之间,则$\rm X$为$\rm N$元素;$\rm R$的原子序数为$\rm 22-1-7-9=5$,可知$\rm R$为$\rm B$元素,阴离子结构中$\rm R$形成的$\rm 4$条共价键中有$\rm 1$条是配位键,由分析可知,$\rm Q$为$\rm H$元素、$\rm R$为$\rm B$元素、$\rm T$为$\rm C$元素、$\rm X$为$\rm N$元素、$\rm Y$为$\rm O$元素、$\rm Z$为$\rm F$元素,据此分析解题。
$\rm A$.根据同一周期从左往右元素非金属性依次增强,简单氢化物的稳定性:${{\text{H}}_{\text{2}}}\text{O}\gt \text{N}{{\text{H}}_{3}}\gt \text{C}{{\text{H}}_{4}}$,即$\text{Y}\gt \text{X}\gt \text{T}$,$\rm A$正确;
$\rm B$.由信息梳理可知,$\rm R$为$\rm B$,$\rm Z$为$\rm F$,故该阴离子$\text{BF}_{4}^{-}$中含有$\rm B-F$配位键,$\rm B$正确;
$\rm C$.$\text{B}{{\text{F}}_{3}}$的中心原子$\rm B$的价层电子对数为$3+\dfrac{1}{2}\times (3-3\times 1)=3$,空间构型为平面三角形,为非极性分子,$\rm C$错误;
$\rm D$.该离子液体属于离子化合物,沸点高,即难挥发,可用作溶剂,$\rm D$正确;
故选:$\rm C$
高中 | 配合物理论题目答案及解析(完整版)
