| 转化率、产率 题目答案及解析
稿件来源:高途
| 转化率、产率题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
转化率、产率
甘油$\left( {{\text{C}}_{3}}{{\text{H}}_{8}}{{\text{O}}_{3}} \right)$水蒸气重整获得${{\text{H}}_{2}}$过程中的主要反应:
反应Ⅰ ${{\text{C}}_{3}}{{\text{H}}_{8}}{{\text{O}}_{3}}(\text{g})=3\text{CO}(\text{g})+4{{\text{H}}_{2}}(\text{g})\quad \Delta H\gt 0$
反应Ⅱ $\text{CO}(\text{g})+{{\text{H}}_{2}}\text{O}(\text{g})=\text{C}{{\text{O}}_{2}}(\text{g})+{{\text{H}}_{2}}(\text{g})\quad \Delta H\lt 0$
反应Ⅲ $\text{C}{{\text{O}}_{2}}(\text{g})+4{{\text{H}}_{2}}(\text{g})=\text{C}{{\text{H}}_{4}}(\text{g})+2{{\text{H}}_{2}}\text{O}(\text{g})\quad \Delta H\lt 0$
$1.0\times {{10}^{5}}\,\text{Pa}$条件下,$1\,\text{mol}\,{{\text{C}}_{3}}{{\text{H}}_{8}}{{\text{O}}_{3}}$和$9\,\text{mol}\,{{\text{H}}_{2}}\text{O}$发生上述反应达平衡状态时,体系中$\text{CO}$、${{\text{H}}_{2}}$、$\text{C}{{\text{O}}_{2}}$和$\text{C}{{\text{H}}_{4}}$的物质的量随温度变化的理论计算结果如图所示。下列说法正确的是$(\quad\ \ \ \ )$
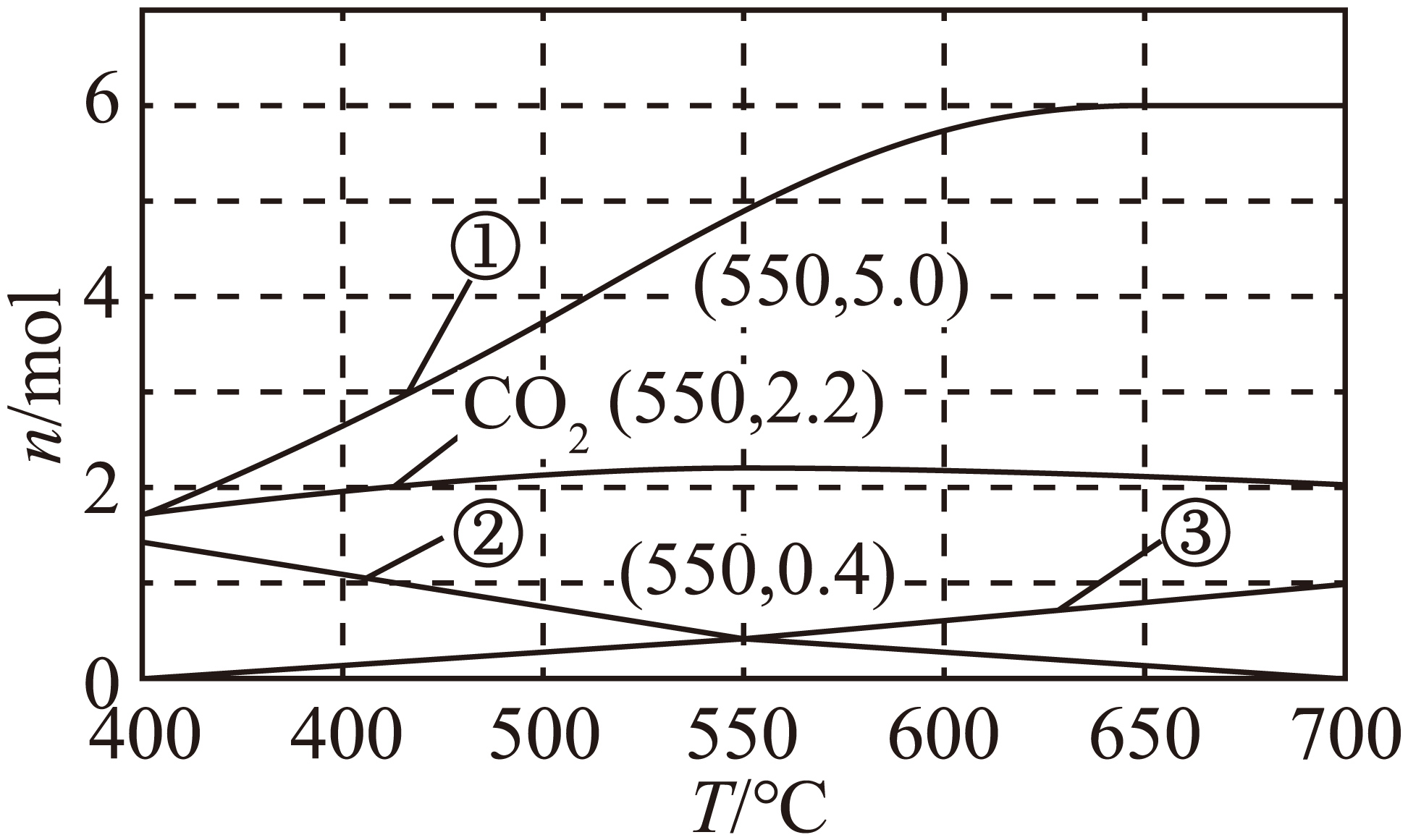
$550\\text{ }{}^\\circ \\text{C}$时,${{\\text{H}}_{\\text{2}}}\\text{O}$的平衡转化率为$\\rm 20\\%$
","$550\\text{ }{}^\\circ \\text{C}$反应达平衡状态时,$n\\left( \\text{C}{{\\text{O}}_{2}} \\right):n(\\text{CO})=11:25$
","其他条件不变,在$400\\sim 550\\text{ }{}^\\circ \\text{C}$范围,平衡时${{\\text{H}}_{\\text{2}}}\\text{O}$的物质的量随温度升高而增大
","其他条件不变,加压有利于增大平衡时${{\\text{H}}_{2}}$的物质的量
"]$\rm 550\;\rm ^\circ\rm C$时,曲线①物质的量是$\rm 5$ $\rm mol$,根据原子守恒,$n\left( \text{C} \right)=3\,\text{mol}$,则其不可能是含碳微粒,故曲线①表示${{\text{H}}_{2}}$,升高温度,反应Ⅰ平衡正移,反应Ⅱ平衡逆向移动,$\rm CO$物质的量增大,则曲线③代表$\rm CO$,温度升高,反应Ⅲ逆向移动,$\text{C}{{\text{H}}_{\text{4}}}$物质的量降低,则曲线②代表$\text{C}{{\text{H}}_{\text{4}}}$,据此解答。
$\rm A$.$550\text{ }{}^\circ \text{C}$时,$n\left( {{\text{H}}_{2}} \right)=5\,\text{mol}$,$n\left( \text{C}{{\text{O}}_{2}} \right)=2.2\,\text{mol}$,$n\left( \text{C}{{\text{H}}_{4}} \right)=n\left( \text{CO} \right)=0.4\,\text{mol}$,根据$\rm C$原子守恒,可得$n\left( {{\text{C}}_{3}}{{\text{H}}_{8}}{{\text{O}}_{3}} \right)=\dfrac{n\left( \text{C} \right)-n\left( \text{C}{{\text{O}}_{2}} \right)-n\left( \text{CO} \right)-n\left( \text{C}{{\text{H}}_{4}} \right)}{3}=0$,根据$\rm O$原子守恒,可得$n\left( {{\text{H}}_{2}}\text{O} \right)=\dfrac{n\left( \text{O} \right)-2n\left( \text{C}{{\text{O}}_{2}} \right)-n\left( \text{CO} \right)-3n\left( {{\text{C}}_{3}}{{\text{H}}_{8}}{{\text{O}}_{3}} \right)}{1}=7.2\,\text{mol}\rm ($也可利用$\rm H$原子守恒计算,结果相同$\rm )$,则$\alpha\left( {{\text{H}}_{2}}\text{O} \right)=\dfrac{9\,\text{mol}-7.2\,\text{mol}}{9\,\text{mol}}\times 100\%=20\%$,$\rm A$正确;
$\rm B$.$550\text{ }{}^\circ \text{C}$时,$n\left( \text{C}{{\text{O}}_{2}} \right)=2.2\,\text{mol}$,$n\left( \text{CO} \right)=0.4\,\text{mol}$,则$n\left( \text{C}{{\text{O}}_{2}} \right):n\left( \text{CO} \right)=11:2$,$\rm B$错误;
$\rm C$.$400\sim550\text{ }{}^\circ \text{C}$范围,随温度升高,反应Ⅱ、Ⅲ平衡均逆向移动,$n\left( \text{C}{{\text{O}}_{2}} \right)$增大,说明反应Ⅲ逆向移动程度更大,则${{\text{H}}_{2}}\text{O}$的物质的量减小,$\rm C$错误;
$\rm D$.增大压强,反应Ⅰ平衡逆向移动,反应Ⅱ平衡不移动,反应Ⅲ平衡正向移动,${{\text{H}}_{2}}$的物质的量减小,$\rm D$错误;
故选:$\rm A$
| 转化率、产率题目答案及解析(完整版)
