高中 | 原电池工作原理 题目答案及解析
稿件来源:高途
高中 | 原电池工作原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第一节 原电池
原电池工作原理
瑞士科学家开发了一种由水激活的一次性印刷纸电池,研究人员先从一张浸入盐水后晾干的纸开始。首先在纸张的一侧涂上含有石墨粉的墨水,背面涂有含有锌粉的墨水,而纸张本身充当隔膜,因此这种特殊的纸张就成为了电池。其结构示意图如图所示。下列有关说法不正确的是$(\qquad)$
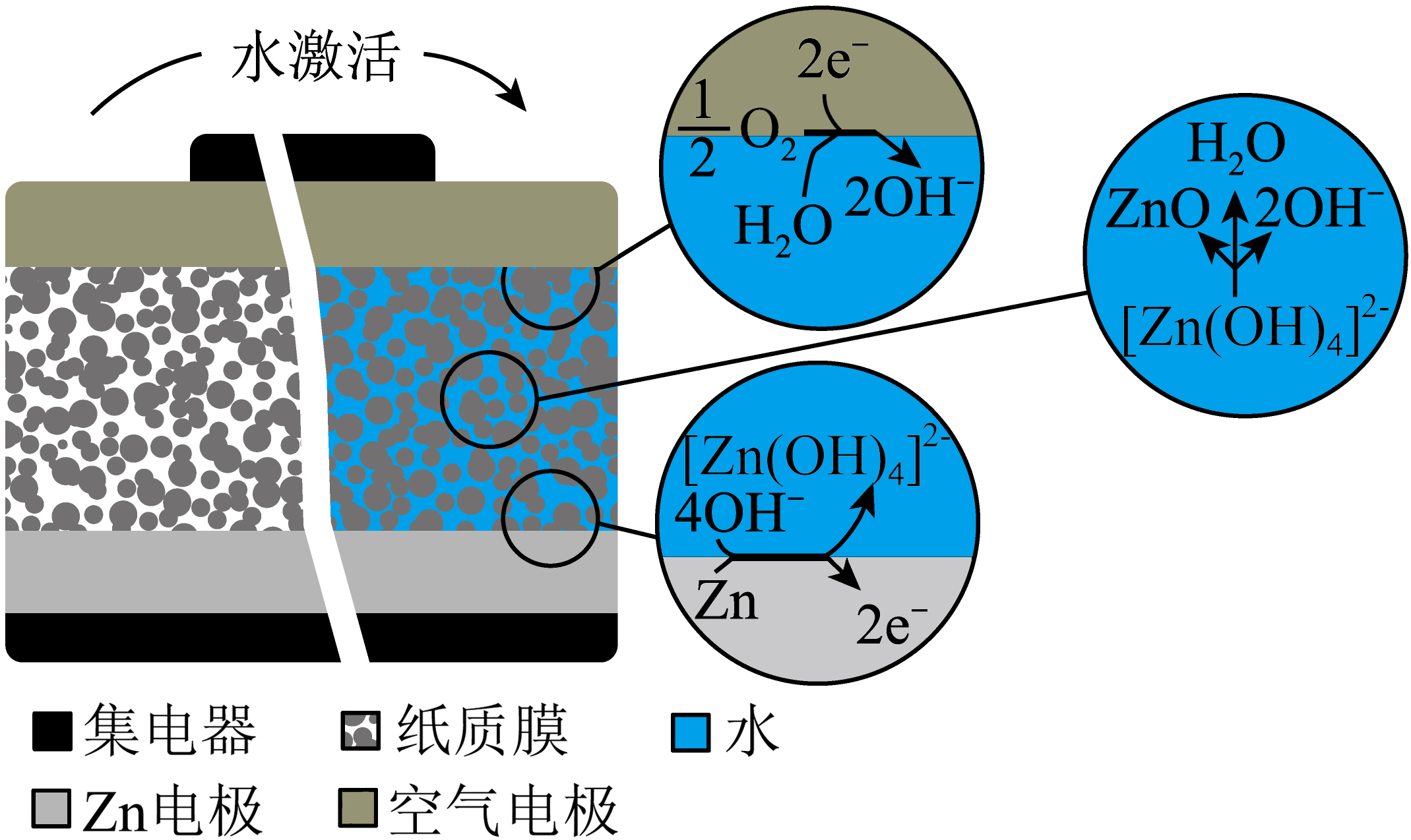
当纸变湿时,纸中的盐会溶解并释放带电离子,从而使电解质具有导电性,起到电解质溶液的作用
","$\\rm Zn$电极作负极,发生的电极反应为$\\text{Zn}-2{{\\text{e}}^{-}}+4\\text{O}{{\\text{H}}^{-}}={{\\left[ \\text{Zn}{{\\left( \\text{OH} \\right)}_{4}} \\right]}^{2-}}$
","该印刷纸电池的总反应为$2\\text{Zn}+{{\\text{O}}_{2}}=2\\text{ZnO}$
","若外电路转移$2 {m\\;\\rm mol}$电子,$\\rm Zn$电极上因$\\rm Zn$损耗减轻的质量为$\\rm 0.065\\;\\rm g$
"]$\rm A$.纸中的盐遇水溶解,形成电解质溶液,可导电,$\rm A$正确;
$\rm B$.由图可知,$\rm Zn$作负极发生氧化反应,电极反应为 $\rm Zn-2{{\text{e}}^{-}}+4O{{H}^{-}}={{\left[ Zn{{\left( OH \right)}_{4}} \right]}^{2-}}$,$\rm B$正确;
$\rm C$.正极反应为$\rm \dfrac{1}{2}{{\text{O}}_{2}}+{{\text{H}}_{2}}\text{O}+2{{\text{e}}^{-}}=2O{{H}^{-}}$,负极生成的$\rm {{\left[ Zn{{\left( OH \right)}_{4}} \right]}^{2-}}$最终转化为$\rm ZnO$、$\rm H_{2}O$、$\rm OH^{-}$,故电池的总反应为$\rm 2\text{Zn}+{{\text{O}}_{2}}=2\text{ZnO}$,$\rm C$正确;
$\rm D$.负极上,$\rm Zn$最终转化成$\rm ZnO$,$\rm Zn$电极质量增加,$\rm D$错误。
故选:$\rm D$
高中 | 原电池工作原理题目答案及解析(完整版)
