高中 | 萃取与分液 题目答案及解析
稿件来源:高途
高中 | 萃取与分液题目答案及解析如下,仅供参考!
必修一
第一章 从实验学化学
第一节 化学实验基本方法
萃取与分液
目前,我国的全钒液流电池储能技术在全球领先。该电池的电解液来自钢铁冶炼后产生的钒钢渣$\rm (CaO$、$\text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{\text{3}}}$和少量$\text{Si}{{\text{O}}_{\text{2}}}$、${{\text{V}}_{\text{2}}}{{\text{O}}_{\text{3}}}\rm )$和钛白废酸$\rm ({{\text{H}}^{+}}$、$\text{F}{{\text{e}}^{\text{2}+}}$、$\text{Ti}{{\text{O}}^{\text{2}+}}$、$\text{SO}_{4}^{2-}\rm )$,实现了“以废治废”。工艺流程如下图:
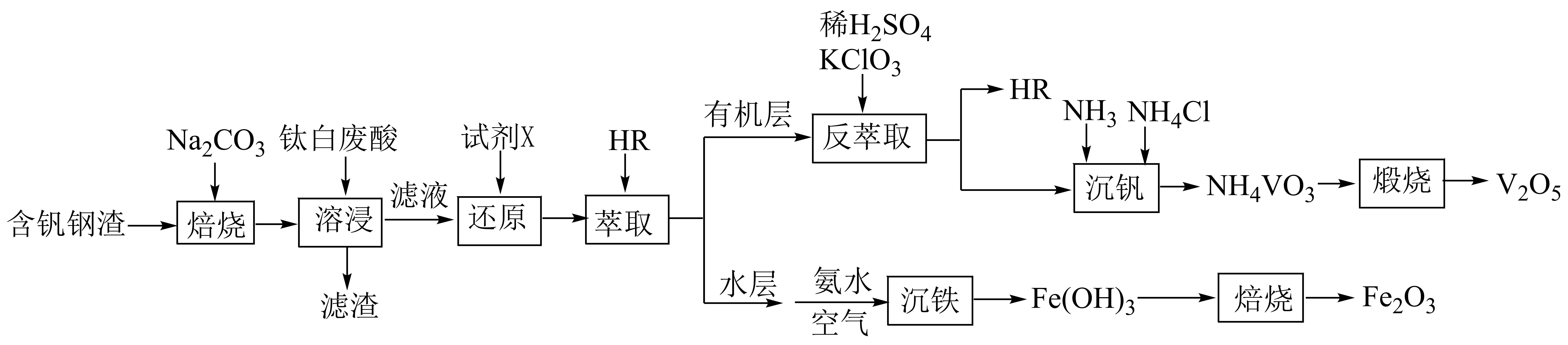
已知:①$\rm V$有多种价态,${{\text{V}}_{\text{2}}}{{\text{O}}_{\text{3}}}$在空气中焙烧时可转化为最稳定的$\rm +5$价;$\rm +5$价$\rm V$在强酸性条件下以$\text{VO}_{2}^{+}$形式存在,在碱性条件下以$\text{VO}_{3}^{-}$形式存在。
②有机萃取剂$\rm HR$的萃取原理为${{\text{M}}^{n+}}\left( \text{aq} \right)+n\text{HR}\left( \text{org} \right)\rightleftharpoons \text{M}{{\text{R}}_{n}}\left( \text{org} \right)+n{{\text{H}}^{+}}\left( \text{aq} \right)$,其中$\rm org$表示有机溶液,酸性条件下$\rm HR$能萃取$\text{F}{{\text{e}}^{\text{3}+}}$而不能萃取$\text{F}{{\text{e}}^{\text{2}+}}$,$\rm HR$对$\rm +4$价钒萃取能力强,而对$\rm +5$价钒的萃取能力较弱。
③$\rm 25\;\rm ^\circ\rm C$时,${{K}_{\text{sp}}}\left( \text{N}{{\text{H}}_{\text{4}}}\text{V}{{\text{O}}_{\text{3}}} \right)=1.6\times {{10}^{-3}}$。
回答下列问题:
“溶浸”时生成的滤渣除了${{\text{H}}_{\text{2}}}\text{Ti}{{\text{O}}_{\text{3}}}$、$\text{CaS}{{\text{O}}_{\text{4}}}$外,还有 $\rm ($填化学式$\rm )$。
${{\\text{H}}_{\\text{2}}}\\text{Si}{{\\text{O}}_{\\text{3}}}$
"]]由分析可知,滤渣的主要成分为${{\text{H}}_{\text{2}}}\text{Ti}{{\text{O}}_{\text{3}}}$、$\text{CaS}{{\text{O}}_{\text{4}}}$、${{\text{H}}_{\text{2}}}\text{Si}{{\text{O}}_{\text{3}}}$。
“还原”中加入的化学试剂$\rm X$可能为 $\rm ($填字母$\rm )$。加入该试剂还原的主要目的是 。
$\rm A$.$\rm \text{C}{{\text{l}}_{\text{2}}}$ $\rm B$.$\rm Fe$ $\rm C$.$\rm \text{N}{{\text{H}}_{\text{3}}}$ $\rm D$.$\rm {{\text{H}}_{\text{2}}}{{\text{O}}_{\text{2}}}$
$\\rm B$;将溶液中的$\\rm +5$价钒和$\\rm \\text{F}{{\\text{e}}^{\\text{3}+}}$分别转化为$\\rm +4$价钒与$\\rm \\text{F}{{\\text{e}}^{\\text{2}+}}$,利于$\\rm +4$价钒的萃取并实现钒和铁元素分离
"]]加入还原剂且不引入新的杂质,则加入铁单质,将$\rm \text{F}{{\text{e}}^{\text{3}+}}$还原为$\rm \text{F}{{\text{e}}^{\text{2}+}}$,选$\rm B$;据提示中②及流程分析可知还原剂的作用是将溶液中的$\rm +5$价钒和$\rm \text{F}{{\text{e}}^{\text{3}+}}$分别转化为$\rm +4$价钒与$\rm \text{F}{{\text{e}}^{\text{2}+}}$,利于$\rm +4$价钒的萃取并实现钒和铁元素分离。
实验室模拟该流程中“萃取”时,共消耗$\rm HR$萃取剂$\rm 45\;\rm mL$,应选用$(\quad\ \ \ \ )$种萃取方式$\rm ($填字母$\rm )$。
单次萃取
","分$\\rm 2$次萃取,每次$\\rm 22.5\\;\\rm mL$
","分$\\rm 3$次萃取,每次$\\rm 15\\;\\rm mL$
"]多次萃取可使萃取率增大,应选$\rm C$。
写出“反萃取”操作中$\text{VO}_{2}^{+}$转化的离子方程式 。
$\\text{6V}{{\\text{O}}^{2+}}+\\text{ClO}_{3}^{-}+\\text{3}{{\\text{H}}_{\\text{2}}}\\text{O}=\\text{6VO}_{2}^{+}+\\text{C}{{\\text{l}}^{-}}+\\text{6}{{\\text{H}}^{+}}$
"]]“反萃取”过程中,$\text{KCl}{{\text{O}}_{\text{3}}}$在酸性条件下将$\text{V}{{\text{O}}^{\text{2}+}}$氧化为$\text{VO}_{2}^{+}$,其离子反应方程式为:$\text{6V}{{\text{O}}^{\text{2}+}}+\text{ClO}_{3}^{-}+\text{3}{{\text{H}}_{\text{2}}}\text{O}=\text{6VO}_{2}^{2+}+\text{C}{{\text{l}}^{-}}+\text{6}{{\text{H}}^{+}}$。
$\rm 25\;\rm ^\circ\rm C$时,测得溶液中$c\left( \text{VO}_{\text{3}}^{-} \right)=0. {2\;\rm mol}\cdot {{\text{L}}^{-\text{1}}}$,为使“沉钒”时,钒元素的沉淀率达到$\rm 98\%$,应调节溶液中$c\left( \text{NH}_{4}^{+} \right)$至少为 $\text{mol}\cdot {{\text{L}}^{-\text{1}}}$。
$\\rm 0.4$
"]]$\rm 25\;\rm ^\circ\rm C$时,“转化”后所得滤液中$c\left( \text{VO}_{3}^{-} \right)=0. {2\;\rm mol}\cdot {{\text{L}}^{-\text{1}}}$,“沉钒”时钒元素的沉淀率为$\rm 98\%$,则“沉钒”后的溶液中$c\left( \text{VO}_{3}^{-} \right)=0.2\times 2\%\; \text{mol}/\text{L}=0.004\;\rm \text{mol}/\text{L}$,应调节溶液中$c\left( \text{NH}_{4}^{+} \right)$至少为$\dfrac{{{ {K}}_{\rm sp}}\left(\rm N{{H}_{4}}V{{O}_{3}} \right)}{ {c}\left(\rm VO_{3}^{+} \right)}=\dfrac{1.6\times {{10}^{-3}}}{0.004\;\rm \text{mol}\cdot {{\text{L}}^{-\text{1}}}}=0. {4\;\rm mol}/\text{L}$。
上述流程中可循环利用的物质除$\text{N}{{\text{H}}_{\text{4}}}\text{Cl}$外,还有 、 $\rm ($填化学式$\rm )$。
$\\rm HR$;$\\text{N}{{\\text{H}}_{3}}$
"]]上述流程中,“反萃取”得到萃取剂$\rm HR$、钒酸铵煅烧分解放出氨气,$\rm HR$可用于“萃取”步骤,氨气可用于“沉钒”、沉铁步骤,可循环利用的物质除$\text{N}{{\text{H}}_{\text{4}}}\text{Cl}$外,还有$\rm HR$、$\text{N}{{\text{H}}_{\text{3}}}$。
全钒液流电池是一种新型的绿色环保储能系统,工作原理如下图所示。该电池放电时,$\rm b$极发生氧化反应,则此时$\rm a$极电极反应式为 。
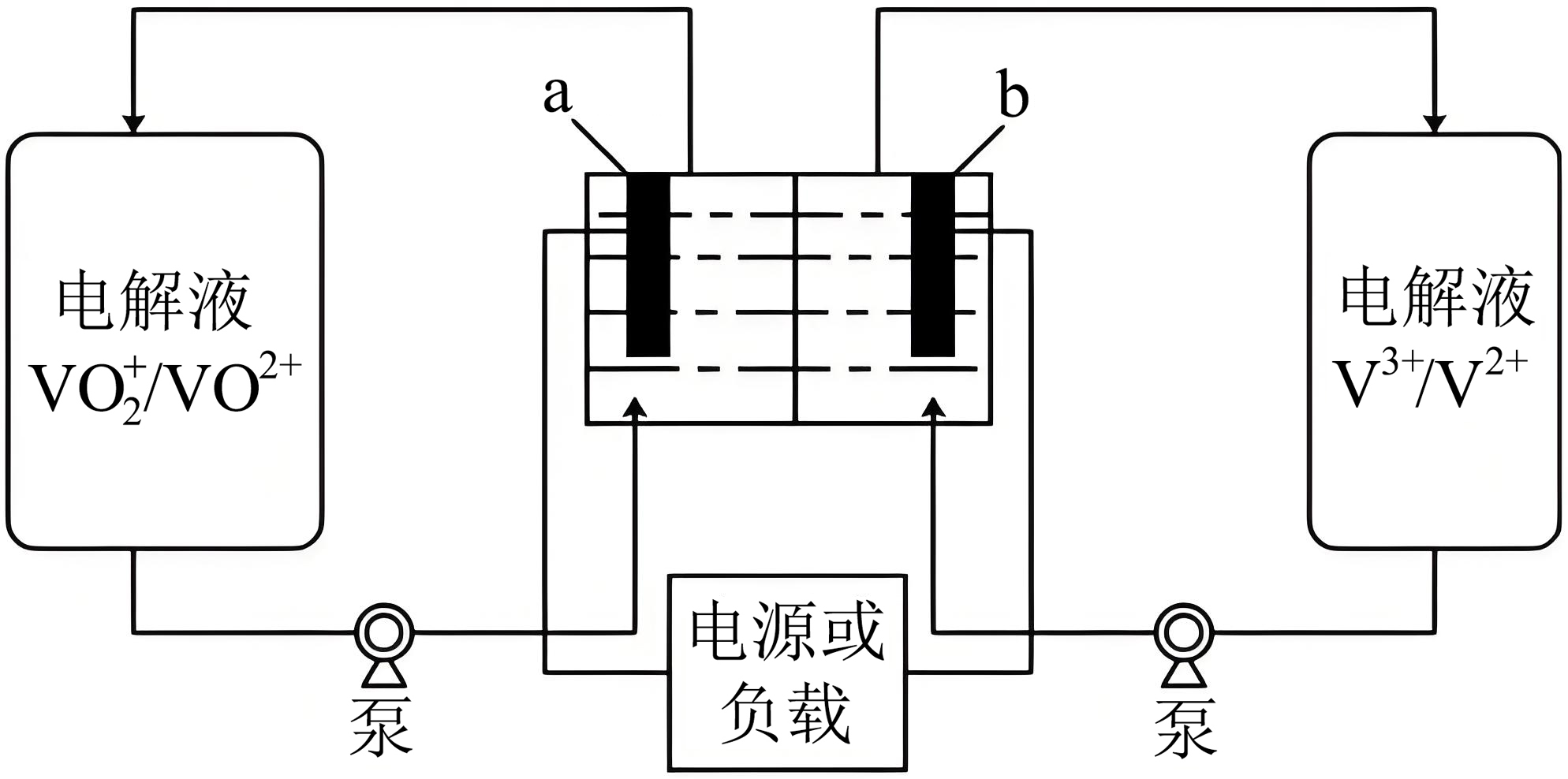
$\\rm \\text{VO}_{\\text{2}}^{+}+{{\\text{e}}^{-}}+\\text{2}{{\\text{H}}^{+}}=\\text{V}{{\\text{O}}^{\\text{2}+}}+{{\\text{H}}_{\\text{2}}}\\text{O}$
"]]全钒液流电池放电时$\rm {{\text{V}}^{\text{2}+}}$发生氧化反应,则$\text{VO}_{2}^{+}$发生还原反应,得电子,正极反应式为:$\text{VO}_{2}^{+}+{{\text{e}}^{-}}+\text{2}{{\text{H}}^{+}}=\text{V}{{\text{O}}^{2+}}+{{\text{H}}_{\text{2}}}\text{O}$。
高中 | 萃取与分液题目答案及解析(完整版)
