高中 | 电解池原理 题目答案及解析
稿件来源:高途
高中 | 电解池原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第三节 电解池
电解池原理
某研究小组设计如下电解池,既可将中性废水中的硝酸盐转化为氨,又可将废塑料$\rm (PET)$碱性水解液中的乙二醇转化为羟基乙酸盐,实现变废为宝。
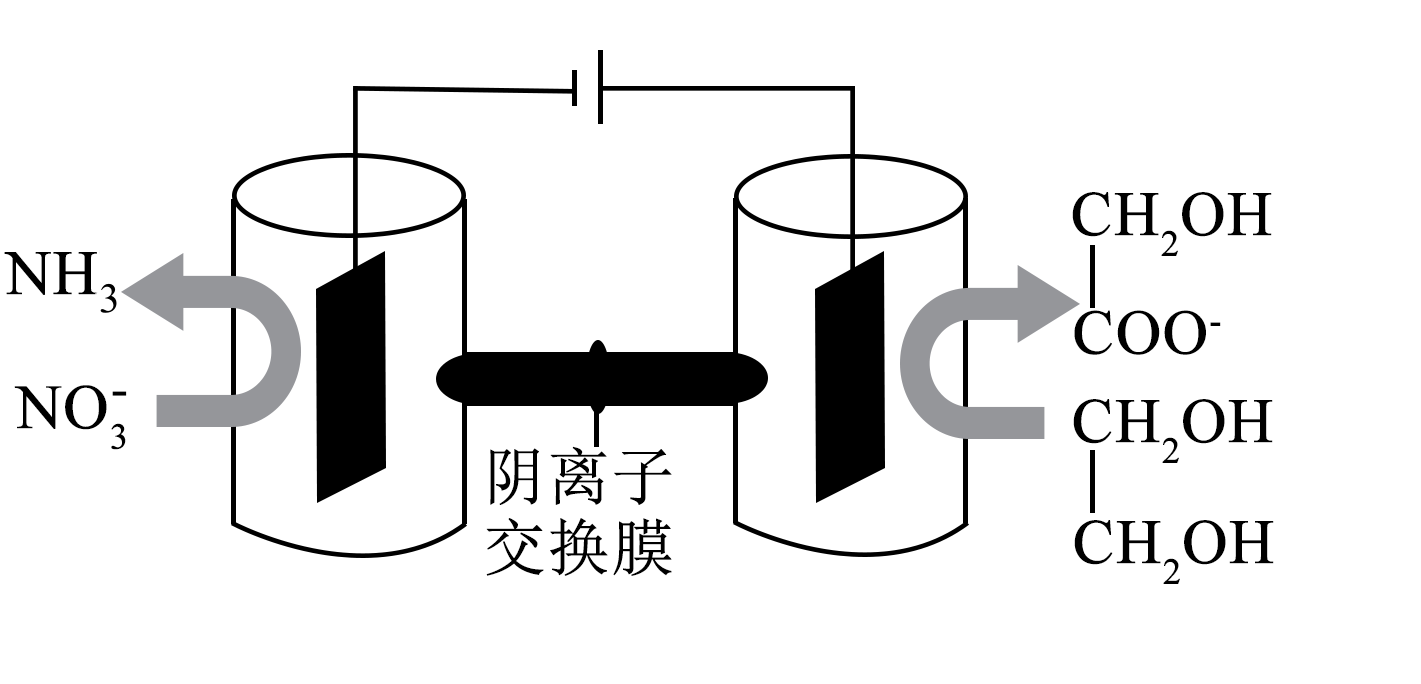
电解时,下列说法错误的是$\rm (\qquad)$
阳极区$\\rm \\text{pH}$下降
","$\\rm \\text{O}{{\\text{H}}^{-}}$从阴极区向阳极区迁移
","阴极发生反应$\\rm \\text{NO}_{\\text{3}}^{-}\\text{+7}{{\\text{H}}_{\\text{2}}}\\text{O+8}{{\\text{e}}^{-}}\\text{=N}{{\\text{H}}_{\\text{3}}}\\cdot {{\\text{H}}_{\\text{2}}}\\text{O+9O}{{\\text{H}}^{-}}$
","阴极转化$\\rm \\text{1\\;\\rm mol NO}_{3}^{-}$,阳极将生成$\\rm \\text{4\\;\\rm mol HOC}{{\\text{H}}_{\\text{2}}}\\text{CO}{{\\text{O}}^{-}}$
"]根据图示,电解时,左侧电极连接电源负极,为阴极区,发生还原反应,电极反应式为:$\rm \text{NO}_{\text{3}}^{-}\text{+7}{{\text{H}}_{\text{2}}}\text{O+8}{{\text{e}}^{-}}\text{=N}{{\text{H}}_{\text{3}}}\cdot {{\text{H}}_{\text{2}}}\text{O+9O}{{\text{H}}^{-}}$;右侧电极连接电源正极,为阳极区,发生氧化反应,电极反应式为:$\rm \text{HOC}{{\text{H}}_{\text{2}}}\text{C}{{\text{H}}_{\text{2}}}\text{OH}-4{{\text{e}}^{-}}\text{+5O}{{\text{H}}^{-}}\text{=HOC}{{\text{H}}_{\text{2}}}\text{CO}{{\text{O}}^{-}}+4{{\text{H}}_{\text{2}}}\text{O}$。
$\rm A$.根据分析,阳极区消耗了$\rm \text{O}{{\text{H}}^{-}}$,$\rm \text{pH}$下降,$\rm A$正确;
$\rm B$.阴极区生成了$\rm \text{O}{{\text{H}}^{-}}$,阳极区消耗了$\rm \text{O}{{\text{H}}^{-}}$,按照离子移动方向,$\rm \text{O}{{\text{H}}^{-}}$从阴极区通过阴离子交换膜向阳极区迁移,$\rm B$正确;
$\rm C$.根据分析阴极发生还原反应,电极反应式为:$\rm \text{NO}_{\text{3}}^{-}\text{+7}{{\text{H}}_{\text{2}}}\text{O+8}{{\text{e}}^{-}}\text{=N}{{\text{H}}_{\text{3}}}\cdot {{\text{H}}_{\text{2}}}\text{O+9O}{{\text{H}}^{-}}$,$\rm C$正确;
$\rm D$.阴极转化$\rm \text{1\;\rm mol NO}_{3}^{-}$,转移$\rm \text{8\;\rm mol}\;{{\text{e}}^{-}}$,此时阳极将生成$\rm \text{2\;\rm mol HOC}{{\text{H}}_{\text{2}}}\text{CO}{{\text{O}}^{-}}$,$\rm D$错误;
故选:$\rm D$
高中 | 电解池原理题目答案及解析(完整版)
