高中 | 离子方程式 题目答案及解析
稿件来源:高途
高中 | 离子方程式题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第二节 离子反应
离子方程式
化学要研究如何合理、高效地开发利用金属矿物。下列有关如图所示流程的判断正确的是$(\qquad)$
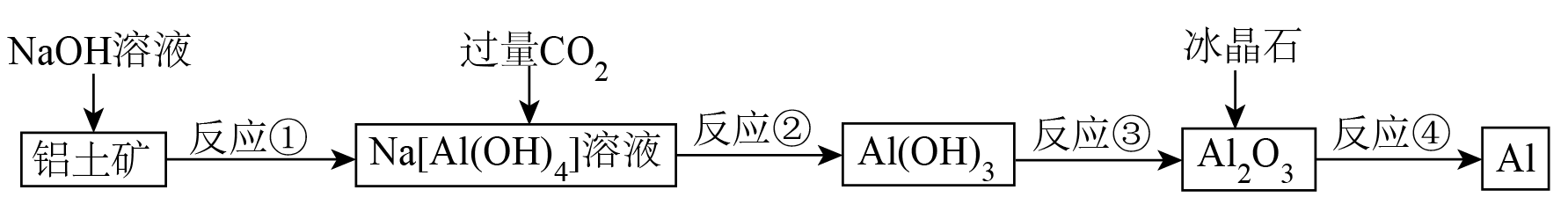
流程中涉及的反应均为非氧化还原反应
","反应①的主要反应的离子方程式为$\\text{A}{{\\text{l}}_{\\text{2}}}{{\\text{O}}_{\\text{3}}}\\text{+2O}{{\\text{H}}^{-}}\\text{+3}{{\\text{H}}_{\\text{2}}}\\text{O=2}{{\\left[ \\text{Al}{{\\left( \\text{OH} \\right)}_{\\text{4}}} \\right]}^{-}}$
","实验室中完成反应③应在蒸发皿中进行
","反应②产生的阴离子主要为$\\text{CO}_{3}^{2-}$
"]氢氧化钠溶液与铝土矿中的氧化铝反应后得到偏铝酸钠溶液,通入过量二氧化碳后,与偏铝酸钠转化为氢氧化铝沉淀和碳酸氢钠,氢氧化铝受热分解得到氧化铝,电解熔融氧化铝得到金属铝。
$\rm A$.根据分析,电解熔融氧化铝得到金属铝的反应为氧化还原反应,$\rm A$错误;
$\rm B$.根据分析,反应①的主要反应的离子方程式为$\text{A}{{\text{l}}_{\text{2}}}{{\text{O}}_{\text{3}}}\text{+2O}{{\text{H}}^{-}}\text{+3}{{\text{H}}_{\text{2}}}\text{O=2}{{\left[ \text{Al}{{\left( \text{OH} \right)}_{\text{4}}} \right]}^{-}}$,$\rm B$正确;
$\rm C$.氢氧化铝受热分解得到氧化铝,实验室中完成反应③应在坩埚中进行,$\rm C$错误;
$\rm D$.反应②中有碳酸氢钠生成,故产生的阴离子主要为$\text{HCO}_{3}^{-}$,$\rm D$错误。
故选:$\rm B$
高中 | 离子方程式题目答案及解析(完整版)
