| 杂化轨道理论 题目答案及解析
稿件来源:高途
| 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
$\text{SiC}{{\text{l}}_{4}}$的水解机理如下图所示$\rm ($“$\rm □$”代表$\text{Si}$的$\rm 3d$轨道$\rm )$。下列说法错误的是$(\qquad)$
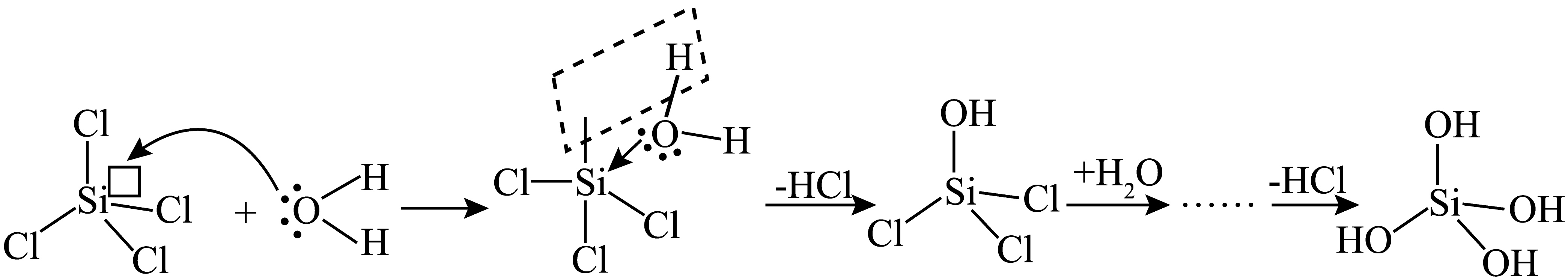
上述过程涉及极性键的断裂和形成
","水解过程中$\\text{Si}$的杂化方式有变化
","$\\text{NC}{{\\text{l}}_{3}}$的水解机理与$\\text{SiC}{{\\text{l}}_{4}}$相同
","相同条件下,$\\text{SiC}{{\\text{l}}_{4}}$比$\\text{CC}{{\\text{l}}_{4}}$易水解
"]$\rm A$.上述过程涉及$\text{Si}-\text{Cl}$极性键的断裂和$\text{Si}-\text{O}$极性键的形成,$\rm A$正确;
$\rm B$.水解过程的第一步中$\text{Si}$原子的成键数目由$\rm 4$增大为$\rm 5$,$\text{Si}$的杂化方式有变化,从最初的$\text{s}{{\text{p}}^{3}}$杂化变为$\text{s}{{\text{p}}^{3}}\text{d}$杂化,$\rm B$正确;
$\rm C$.$\text{NC}{{\text{l}}_{3}}$水解时${{\text{H}}_{2}}\text{O}$中的$\mathrm{H}$原子与$\text{NC}{{\text{l}}_{3}}$上的孤电子对结合,$\mathrm{O}$与$\text{Cl}$结合形成$\text{HClO}$,而$\text{SiC}{{\text{l}}_{4}}$上无孤电子对,故$\text{NC}{{\text{l}}_{3}}$的水解机理与$\text{SiC}{{\text{l}}_{4}}$不相同,$\rm C$错误;
$\rm D$.$\rm C$为第二周期元素,只有$2\text{s}$、$2\text{p}$轨道可以成键,最大配位数为$\rm 4$,无空轨道可以接受水的配位,因此不易水解。所以相同条件下,$\text{SiC}{{\text{l}}_{4}}$比$\text{CC}{{\text{l}}_{4}}$易水解,$\rm D$正确。
故选:$\rm C$
| 杂化轨道理论题目答案及解析(完整版)
