高中 | 杂化轨道理论 题目答案及解析
稿件来源:高途
高中 | 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
一种控制分子是否发光的“分子开关”工作原理如图所示。
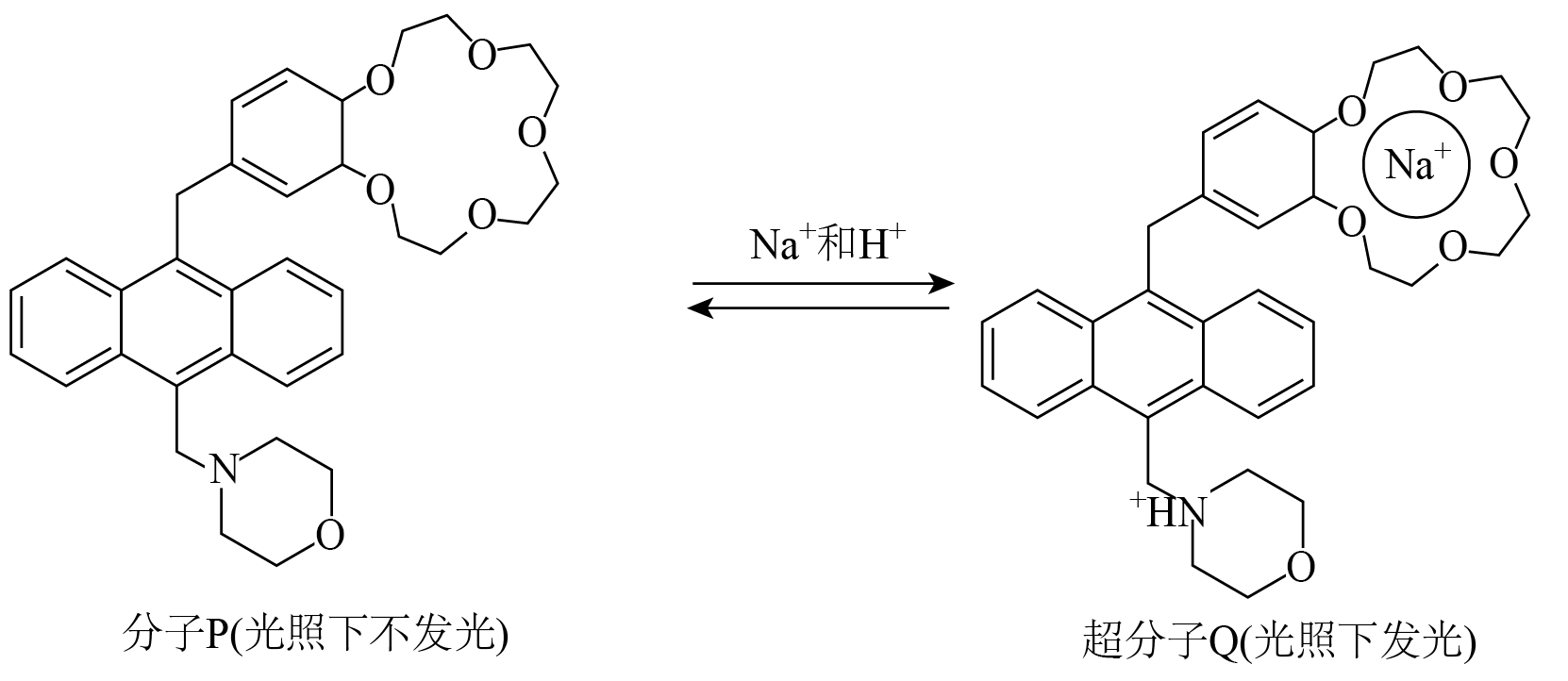
下列说法不正确的是$(\qquad)$
分子$\\rm P$中的$\\rm O$均为$\\mathrm{sp}^2$杂化
","分子$\\rm P$转化为超分子$\\rm Q$时,$\\rm N$与${{\\text{H}}^{+}}$形成配位键
","增大溶液$\\rm pH$并除去$\\text{N}{{\\text{a}}^{+}}$,可使超分子$\\rm Q$转变为分子$\\rm P$
","推测分子$\\rm P$可以增大$\\rm NaCl$在有机溶剂中的溶解度
"]$\rm A$.分子$\rm P$中的$\rm O$均形成$\rm 2$个$\rm \sigma$键、有两对孤电子对,$\rm O$的价层电子对数为$\rm 4$,$\rm O$都采取$\rm sp^{3}$杂化,$\rm A$项错误;
$\rm B$.$\rm N$上有孤电子对,$\rm H^{+}$有空轨道,故分子$\rm P$转化为超分子$\rm Q$时,$\rm N$与$\rm H^{+}$形成配位键,$\rm B$项正确;
$\rm C$.分子$\rm P+Na^{+}+H^{+\rightleftharpoons \rm }$超分子$\rm Q$,增大溶液$\rm pH$并除去$\rm Na^{+}$,消耗$\rm H^{+}$,$\rm H^{+}$和$\rm Na^{+}$的浓度减小,反应逆向进行,超分子$\rm Q$转变为分子$\rm P$,$\rm C$项正确;
$\rm D$.分子$\rm P$为有机物、易溶于有机溶剂,分子$\rm P$能与$\rm Na^{+}$形成超分子,可以增大$\rm NaCl$在有机溶剂中的溶解度,$\rm D$项正确;
故选:$\rm A$
高中 | 杂化轨道理论题目答案及解析(完整版)
