高中 | 化学平衡常数 题目答案及解析
稿件来源:高途
高中 | 化学平衡常数题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
化学平衡常数
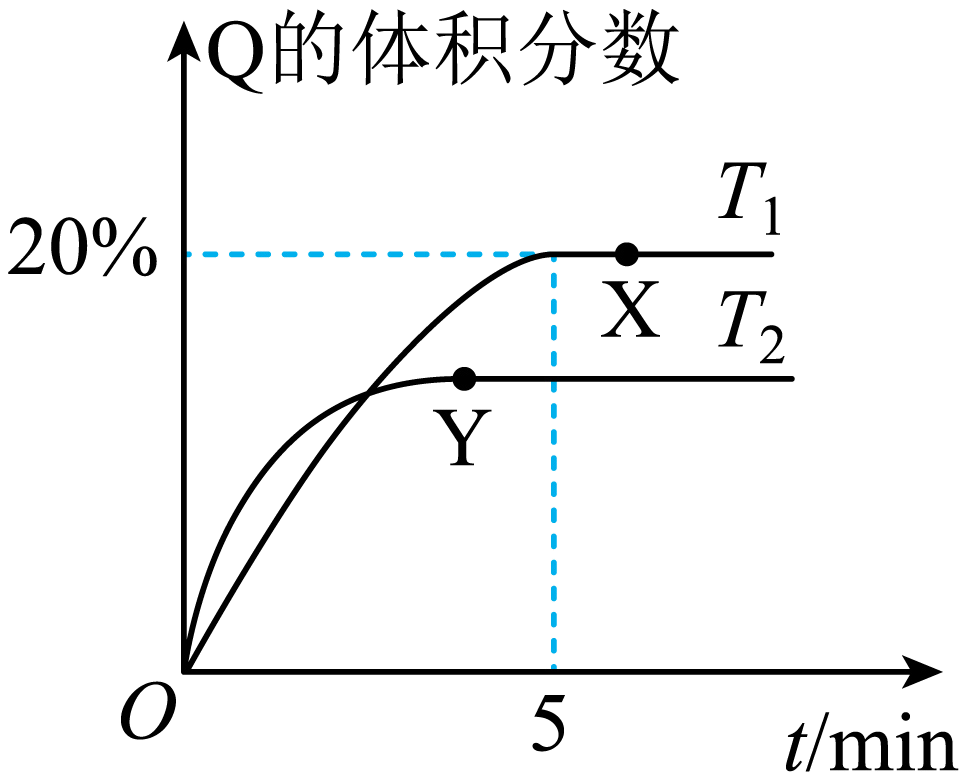
将$\rm 1\ mol\ M$和$\rm 2\ mol\ N$置于体积为$\rm 2\ L$的恒容密闭容器中,发生反应:${\rm M(g)+2N(g)\rightleftharpoons P(g)+Q(g)}\quad\Delta H$。反应过程中测得$\rm Q$的体积分数在不同温度下随时间的变化如图所示。下列结论正确的是$\rm (\qquad)$
$\\Delta H\\gt 0$
","温度:${{T}_{1}}\\gt {{T}_{2}}$
","温度为${{T}_{1}}$时,$\\rm M$的平衡转化率为$\\rm 50\\%$
","若$\\rm X$、$\\rm Y$两点的平衡常数分别为${{K}_{1}}$、${{K}_{2}}$,则$K_{1}\\lt K_{2}$
"]先拐先平数值大,${{T}_{2}}\gt {{T}_{1}}$,温度升高,$\rm Q$的体积分数减小,平衡逆向移动,说明$\Delta H\lt 0$,据此作答。
$\rm A$.温度升高,$\rm Q$的体积分数减小,平衡逆向移动,说明$\Delta H\lt 0$,$\rm A$错误。
$\rm B$.先拐先平数值大,${{T}_{2}}\gt {{T}_{1}}$,$\rm B$错误。
$\rm C$.温度为${{T}_{1}}$时,设$\rm M$的变化量为$x\ \rm mol$,列三段式为:$\rm \begin{matrix} {} & \rm M(g) & + & \rm 2N(g) & \rightleftharpoons & \rm P(g) & + & \rm Q(g) \\ 起始量\rm (mol) & 1 & {} & 2 & {} & 0 & {} & 0 \\ 反应量\rm (mol) & x & {} & 2x & {} & x & {} & x \\ 平衡量\rm (mol) & 1-x & {} & 2-2x & {} & x & {} & x \\ \end{matrix}$,温度为${{T}_{1}}$,平衡时$\rm Q$的体积分数$=\dfrac{x}{3-x}\times 100{ }\%=20\%$,解得$x=0.5$,$\rm M$的平衡转化率为$\rm \dfrac{0.5\ mol}{1\ mol}\times 100\%=50\%$,$\rm C$正确。
$\rm D$.${{T}_{2}}\gt {{T}_{1}}$,对于放热反应,温度越低平衡常数越大,则${{K}_{1}}\gt {{K}_{2}}$,$\rm D$错误。
故选:$\rm C$
高中 | 化学平衡常数题目答案及解析(完整版)
