| 导电的原因及条件 题目答案及解析
稿件来源:高途
| 导电的原因及条件题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第二节 离子反应
导电的原因及条件
某兴趣小组的同学向盛有一定体积的$\text{Ba}{{\left( \text{OH} \right)}_{2}}$溶液的烧杯中逐渐通入$\text{C}{{\text{O}}_{2}}$气体,并测得所得的体系中导电能力随时间变化的曲线如图所示。下列说法正确的是$(\qquad)$
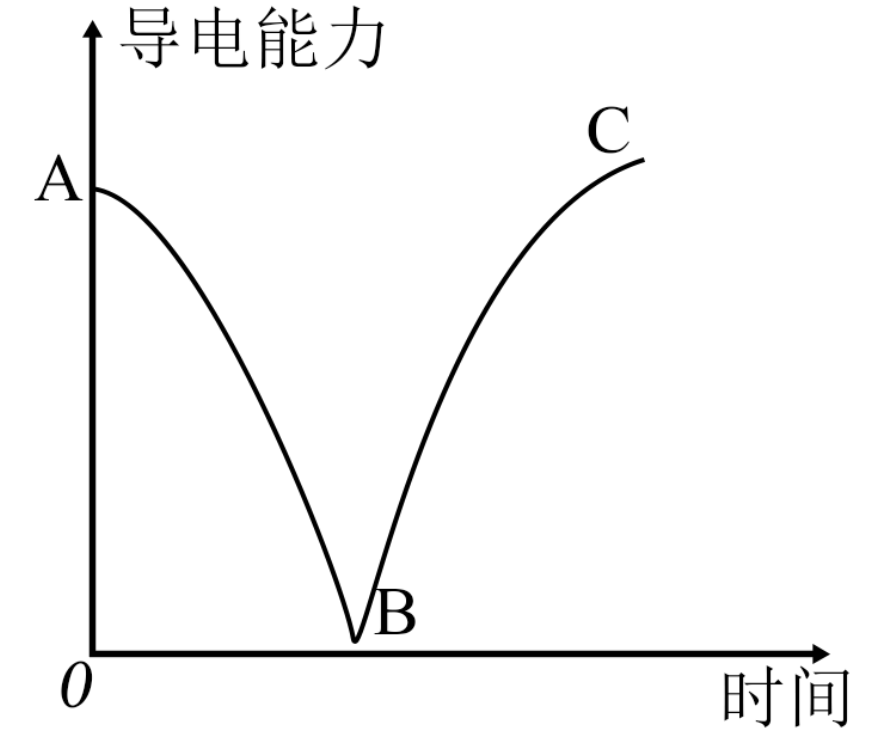
$\\rm AB$段溶液的导电能力不断减弱,说明生成的$\\text{BaC}{{\\text{O}}_{3}}$不是电解质
","$\\rm B$处溶液的导电能力约为$\\rm 0$,说明溶液中几乎没有自由移动的离子
","$\\rm BC$段导电能力不断增强,原因是$\\text{C}{{\\text{O}}_{2}}$溶于水生成了电解质${{\\text{H}}_{2}}\\text{C}{{\\text{O}}_{3}}$
","$\\rm AB$段反应的离子方程式为:$\\text{C}{{\\text{O}}_{2}}+2\\text{O}{{\\text{H}}^{-}}=\\text{CO}_{3}^{2-}+{{\\text{H}}_{2}}\\text{O}$
"]$\rm A$.碳酸钡难溶于水,溶液中离子浓度减小,所以$\rm AB$段溶液的导电能力不断减弱,但$\text{BaC}{{\text{O}}_{3}}$是电解质,$\rm A$错误;
$\rm B$.$\rm B$处溶液的导电能力约为$\rm 0$,说明溶液中几乎没有自由移动的离子,$\rm B$正确;
$\rm C$.过量的二氧化碳与碳酸钡、水反应生成碳酸氢钡,碳酸氢钡是易溶于水的电解质,导致溶液中自由移动离子的浓度变大,溶液导电能力增强,$\rm C$错误;
$\rm D$.$\rm AB$段反应的离子方程式为:$\text{C}{{\text{O}}_{2}}+2\text{O}{{\text{H}}^{-}}+\text{B}{{\text{a}}^{2+}}=\text{BaC}{{\text{O}}_{\text{3}}}\downarrow +{{\text{H}}_{2}}\text{O}$,$\rm D$错误。
故选:$\rm B$
| 导电的原因及条件题目答案及解析(完整版)
