高中 | 配合物理论 题目答案及解析
稿件来源:高途
高中 | 配合物理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
配合物理论
六水合硫酸亚铁铵$\rm {{(N{{H}_{4}})}_{2}}Fe{{(S{{O}_{4}})}_{2}}\cdot 6{{H}_{2}}O$,俗称莫尔盐,易溶于水,难溶于乙醇。其晶体的部分结构如图所示。
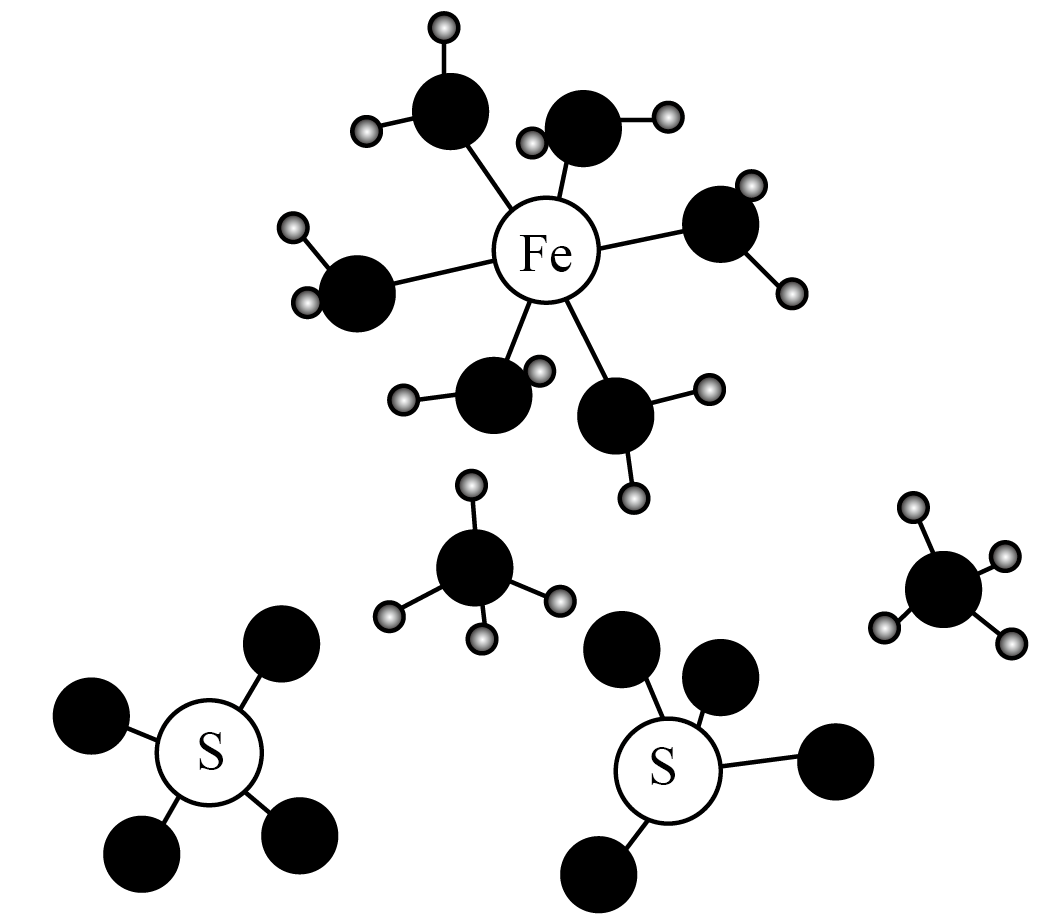
和$\rm F{{e}^{2+}}$价电子排布相同的是 。
$\rm A$.$\rm C{{o}^{3+}}$
$\rm B$.$\rm M{{n}^{2+}}$
$\rm C$.$\rm C{{r}^{3+}}$
$\rm D$.$\rm C{{u}^{2+}}$
$\\rm A$
"]]$\rm F{{e}^{2+}}$价电子排布为$\rm 3d^{6}$,$\rm C{{o}^{3+}}$的价电子排布为$\rm 3d^{6}$,$\rm M{{n}^{2+}}$的价电子排布为$\rm 3d^{5}$,$\rm C{{r}^{3+}}$的价电子排布为$\rm 3d^{3}$,$\rm C{{u}^{2+}}$的价电子排布为$\rm 3d^{9}$,故$\rm A$选。
下列说法正确的是 。
$\rm A$.第一电离能:$\rm O\gt N\gt S$
$\rm B$.铵根和硫酸根微粒的空间结构不同
$\rm C$.晶体中$\rm F{{e}^{2+}}$的配位数为$\rm 6$
$\rm D$.晶体中微粒间的相互作用只有离子键、共价键和配位键
$\\rm C$
"]]$\rm A$.同一周期元素的第一电离能,从左到右增大,$\rm N$处于半充满的稳定状态,其第一电离能大于$\rm O$,同族元素第一电离能从上到下减小,故第一电离能:$\rm O\gt N\gt S$,$\rm A$错误。
$\rm B$.铵根的价层电子对数$\rm 4+ \dfrac{5-1-1 \times 4}{2}=4$,空间结构为正四面体,硫酸根微粒的价层电子对数$\rm 4+\dfrac{6+2-2\times 4}{2}=4$,空间结构为正四面体,二者的空间结构相同,$\rm B$错误。
$\rm C$.由图可知,晶体中$\rm F{{e}^{2+}}$的配位数为$\rm 6$,$\rm C$正确。
$\rm D$.晶体中微粒间的相互作用只有离子键、共价键和配位键,还有分子间作用力、氢键,$\rm D$错误。
制备莫尔盐时,从溶液中结晶析出晶体,过滤,洗涤,干燥。通常用乙醇洗涤除去莫尔盐晶体表面杂质。说明使用乙醇洗涤的其他目的: 。
莫尔盐难溶于乙醇,减少莫尔盐溶解损失;乙醇易挥发,便于更快干燥
"]]因莫尔盐难溶于乙醇,使用乙醇洗涤的其他目的:莫尔盐难溶于乙醇,减少莫尔盐溶解损失;乙醇易挥发,便于更快干燥。
写出检验晶体中$\rm F{{e}^{2+}}$离子的实验方案: 。
取样溶于水,滴入几滴$\\rm KSCN$溶液,无明显变化;再滴入少量氯水$\\rm ($或过氧化氢酸性溶液$\\rm )$,溶液变为血红色,则含$\\rm F{{e}^{2+}}$
"]]取样溶于水,滴入几滴$\rm KSCN$溶液,无明显变化;再滴入少量氯水$\rm ($或过氧化氢酸性溶液$\rm )$,亚铁离子被氧化成铁离子,溶液变为血红色,则含$\rm F{{e}^{2+}}$。
高中 | 配合物理论题目答案及解析(完整版)
